Diferencia entre la reacción base ácida y la reacción de precipitación
El diferencia clave entre la reacción de la base ácida y la reacción de precipitación es que Las reacciones de base de ácido incluyen la neutralización de un ácido de una base o viceversa, mientras que las reacciones de precipitación incluyen la formación de un precipitado después de la finalización de la reacción.
Existen diferentes tipos de reacciones químicas, como reacciones combinadas, descomposición, desplazamiento único y reacciones de doble desplazamiento, combustión, reacciones redox, etc. La base ácida y las reacciones de precipitación son tipos de dos tipos.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es una reacción base ácida?
3. ¿Qué es una reacción de precipitación?
4. Comparación de lado a lado: reacción de base ácida frente a reacción de precipitación de precipitación
5. Resumen
¿Qué es una reacción base ácida??
Una reacción base ácida es una reacción química en la que reacciona un ácido con una base o viceversa. Aquí, ocurre una neutralización; El ácido neutraliza la base o viceversa; Por lo tanto, podemos llamarlo una reacción de neutralización también. Además, el producto final de estas reacciones son sales hechas de aniones de ácido y cationes de la base más moléculas de agua. En esta reacción, puede ocurrir la ruptura de enlaces y la formación de enlaces.
Además, la reacción de la base ácida puede ocurrir de dos maneras: si la reacción ocurre entre un ácido fuerte y una base fuerte, entonces es esencialmente una reacción cuantitativa. Eso significa; La reacción procede hasta que el ácido y/o la base se consuman por completo. Sin embargo, si la reacción ocurre entre un ácido débil y/o una base débil, habrá un equilibrio. Pero, este tipo de reacción no es cuantitativo porque un ácido débil o una base débil es una solución tampón.
Por ejemplo, la reacción entre HCl y NaOH es cuantitativa porque HCl es un ácido fuerte y NaOH es una base fuerte.
HCL(aq) + Na (oh)(aq) → H2O + NaCl(aq)
Pero, la reacción entre la adenina y el fosfato de hidrógeno no es cuantitativa porque el fosfato de hidrógeno es un ácido débil. Entonces el equilibrio es el siguiente:
AH+HPO42− ⇌ A- + H2correos−4
¿Qué es una reacción de precipitación??
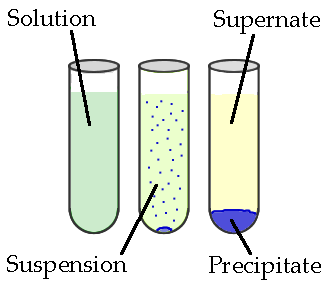
Una reacción de precipitación es un tipo de reacción química en la que se forma un precipitado al final de la reacción. Aquí, los reactivos son dos sales solubles. Estas sales se combinan entre sí para dar una sal insoluble que llamamos el precipitado. Además, el precipitado puede existir de dos maneras diferentes: como una suspensión o una masa sólida que se hunde en el fondo del contenedor.

Si es una suspensión, podemos separarla de la mezcla de reacción a través de la centrifugación, la decantación o la filtración. El líquido restante después de la separación del precipitado se llama sobrenadante.
¿Cuál es la diferencia entre la reacción base ácida y la reacción de precipitación??
La base ácida y las reacciones de precipitación son dos tipos de reacciones químicas. La diferencia clave entre la reacción de la base ácida y la reacción de precipitación es que las reacciones de base ácida incluyen la neutralización de un ácido de una base o viceversa, mientras que las reacciones de precipitación incluyen la formación de un precipitado después de la finalización de la reacción. El proceso de una reacción base ácida incluye la combinación de aniones y cationes para formar una sal y agua, mientras que el proceso de reacción de precipitación incluye la formación de una sal insoluble a partir de sales solubles.

Resumen: reacción de la base ácida frente a la reacción de precipitación
En resumen, la base ácida y las reacciones de precipitación son dos tipos de reacciones químicas. La diferencia clave entre la reacción de la base ácida y la reacción de precipitación es que las reacciones de la base ácida incluyen la neutralización de un ácido de una base o viceversa, mientras que las reacciones de precipitación incluyen la formación de un precipitado después de la finalización de la reacción.
Referencia:
1. Helmenstine, Anne Marie. "Definición de reacción de precipitación."Thinkco, Jan. 22, 2019, disponible aquí.
Imagen de cortesía:
1. "Diagrama de precipitación química" de Zabmilenko - Trabajo propio (dominio público) a través de Commons Wikimedia


