Diferencia entre acidimetría y alcalimetría

El diferencia clave entre acidimetría y alcalimetría es que La acidimetría es la medición de la resistencia de los ácidos, mientras que la alcalimetría es la medición de la resistencia de los compuestos alcalinos.
Acidimetría y alcalimetría son dos tipos de técnicas de análisis volumétrico donde la reacción fundamental del análisis es un tipo de reacción de neutralización.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es la acidimetría
3. ¿Qué es la alcalimetría?
4. Comparación de lado a lado: acidimetría vs alcalimetría en forma tabular
5. Resumen
Que es la acidimetría?
Acidimetría es una técnica analítica especializada utilizada para determinar la resistencia de un ácido. Podemos usar esta técnica en una titulación de base ácida para determinar la concentración de una sustancia básica o alcalina. Sin embargo, necesitamos usar una solución ácida estándar para esta determinación. Implica una reacción de neutralización. Este tipo de técnicas de reacción es útil en procesos de análisis volumétricos.
En acidimetría, el ácido estándar que estamos usando debe tener una concentración conocida; de lo contrario, no podemos determinar la concentración de la base. Dado que casi todos los ácidos y bases que típicamente estamos usando en un proceso de titulación de base ácida son incoloros, necesitamos usar un indicador que ayude a determinar el punto final de la titulación.
Después de realizar la titulación ácida-base, podemos usar la siguiente relación para la determinación de la concentración de la base.
C1V1= C2V2
Cuando C1 es la concentración del ácido estándar, V1 es el volumen del ácido reaccionado con la muestra de analito, C2 es la concentración desconocida de la base (que vamos a descubrir) y V2 es el volumen de la muestra de analito (base).
¿Qué es la alcalimetría??
La alcalimetría es una técnica analítica especial que podemos usar para determinar la resistencia de una base o un compuesto alcalino. En esta técnica, podemos determinar la concentración de una sustancia básica o alcalina si estamos utilizando la reacción en un proceso de titulación de base ácida. Implica una reacción de neutralización.

Figura 01: el uso de un indicador de fenolftaleína para determinar el punto final de una titulación de base ácida, le da un color rosa
En la alcalimetría, la base estándar que utilizamos debe tener una concentración conocida; Si no, no podemos determinar la concentración del ácido. Dado que casi todos los ácidos y bases que típicamente usamos en un proceso de valoración de base ácida son incoloros, necesitamos usar un indicador que ayude a determinar el punto final de la titulación.
¿Cuál es la diferencia entre acidimetría y alcalimetría??
En química analítica, es muy importante conocer la fuerza de los ácidos y las bases que estamos utilizando en un análisis. Acidimetría y alcalimetría son útiles para determinar estas fortalezas. La diferencia clave entre la acidimetría y la alcalimetría es que la acidimetría es la medición de la resistencia de los ácidos, mientras que la alcalimetría es la medición de la resistencia de los compuestos alcalinos. Además, la acidimetría mide la tendencia de un ácido a disociarse, formando protones y un anión, mientras que la alcalimetría mide la tendencia de una base a aceptar protones de otra especie química.
Además, la siguiente infografía resume la diferencia entre acidimetría y alcalimetría en forma tabular.
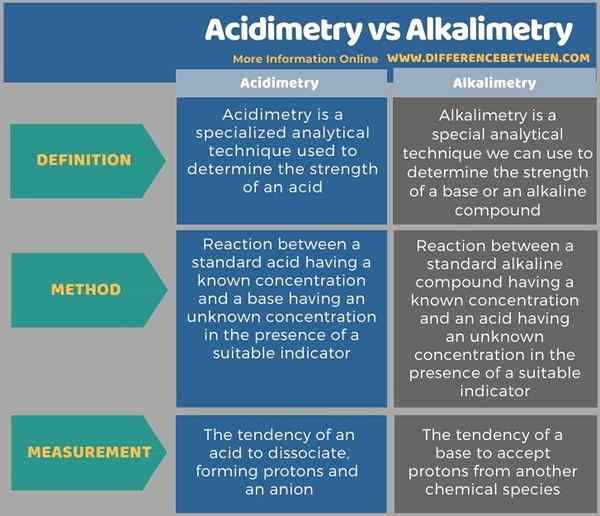
Resumen -Acidimetría vs alcalimetría
En química analítica, es muy importante conocer la fuerza de los ácidos y las bases que estamos utilizando en un análisis. Acidimetría y alcalimetría son dos tipos de técnicas de análisis volumétrico donde la reacción fundamental del análisis es un tipo de reacción de neutralización. La diferencia clave entre la acidimetría y la alcalimetría es que la acidimetría es la medición de la resistencia de los ácidos, mientras que la alcalimetría es la medición de la resistencia de los compuestos alcalinos.
Referencia:
1. "Fuerza base." Bibliotecas de química, Libretexts, 24 de agosto. 2020, disponible aquí.
Imagen de cortesía:
1. "Phenolphthalein in Flask" por 384 - Trabajo propio (CC By -SA 4.0) a través de Commons Wikimedia


