Diferencia entre aminas alifáticas y aromáticas
Aliphatic vs aminas aromáticas
La mejor y la diferencia más significativa entre las aminas alifáticas y aromáticas es la diferencia estructural entre los dos compuestos. Las aminas alifáticas son los compuestos de amina en los que el nitrógeno está unido solo a grupos alquilo, y las aminas aromáticas son los compuestos de amina en los que el nitrógeno está unido a al menos uno de los grupos arilo. Esta diferencia estructural conduce a todas las demás diferencias en sus propiedades, como la reactividad, la acidez y la estabilidad.
¿Qué son las aminas alifáticas??
En aminas alifáticas, El nitrógeno se une directamente a solo grupos alquilo y átomos de hidrógeno. El número de grupos alquilo varía de uno a tres. Dependiendo del número de grupos alquilo adjuntos, se llaman "aminas primarias"(Solo un grupo alquilo -1O), "aminas secundarias”(Dos grupos alquilo - 2O), y "aminas terciarias”(Tres grupos alquilo - 3O).
Todas las aminas alifáticas son bases débiles como el amoníaco, pero son bases ligeramente más fuertes que el amoníaco. Todos tienen casi la misma fuerza base de PKB = 3-4. La basicidad aumenta a medida que los grupos de hidrógeno en el átomo de nitrógeno son reemplazados por grupos alquilo. Las aminas terciarias son más básicas que las aminas primarias y secundarias.
Cuando el nitrógeno es uno de los átomos en un anillo, se les llama aminas heterocíclicas. Piperidina y pirolidina son dos ejemplos para aminas heterocíclicas alifáticas.
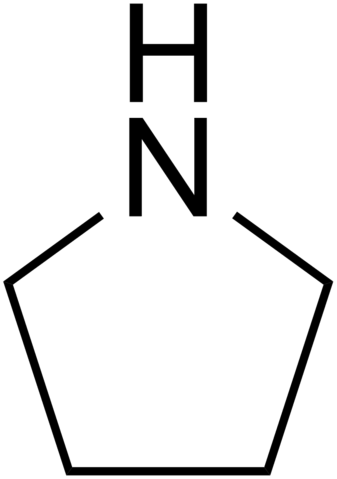
Pirolidina
¿Qué son las aminas aromáticas??
En aminas aromáticas, El nitrógeno está directamente unido a al menos un anillo de benceno. Dependiendo del número de grupos unidos al átomo de nitrógeno, se clasifican como aminas "primarias", "secundarias" y "terciarias". "Arilo aminas"Es otro nombre para aminas aromáticas. Similar a las aminas alifáticas, las aminas aromáticas primarias y secundarias pueden formar enlaces de hidrógeno intermoleculares. Por lo tanto, los puntos de ebullición de las aminas primarias y secundarias son relativamente más altos que las aminas terciarias.
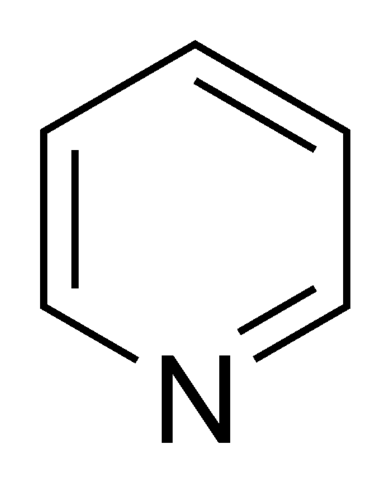
Hay aminas aromáticas heterocíclicas; Pyrrol y Pyrydine son dos ejemplos para ellos.

Pirydine
¿Cuál es la diferencia entre aminas alifáticas y aromáticas??
• Estructura:
• Las aminas alquílicas no contienen anillos de benceno que están directamente unidos al átomo de nitrógeno.
• Pero, en aminas aromáticas, hay al menos un anillo de benceno directamente unido al átomo de nitrógeno.
• Las aminas alifáticas pueden tener anillos aromáticos mientras el nitrógeno esté directamente unido a un átomo de carbono.
• Basicidad:
• Las aminas alifáticas son bases más fuertes que las aminas aromáticas. Esto se debe básicamente a la estabilidad del catión que se forma después de la ionización. En otras palabras, los iones de amonio alquilo son más estables que los iones de amonio aril. Porque, los grupos alquilo son grupos liberadores de electrones y, por lo tanto, delocalizan parcialmente la carga positiva en el átomo de nitrógeno.

• Las aminas heterocíclicas alifáticas también son bases más fuertes que las aminas heterocíclicas aromáticas.
• Ejemplos
• Los ejemplos de aminas heterocíclicas alifáticas son la piperidina y la pirolidina.
• Los ejemplos de aminas aromáticas heterocíclicas son pirrol y pyrydine.
Imágenes cortesía: pirolidina y piridina a través de wikicommons (dominio público)


