Diferencia entre álcali y base

El diferencia clave entre álcali y base es que el Los elementos del grupo 1 se clasifican como elementos alcalinos, mientras que cualquier elemento o compuesto que tenga propiedades básicas se clasifica como base.
A menudo usamos la palabra álcali indistintamente para abordar soluciones altamente básicas y metales alcalinos. En este contexto, el álcali se remite a los metales alcalinos del grupo 1 de la tabla periódica de elementos. Sin embargo, el término base puede referirse a cualquier elemento, molécula, ion, etc. que tienen propiedades básicas.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es alcali
3. Que es la base
4. Comparación de lado a lado - Alkali vs base en forma tabular
5. Resumen
Que es alcali?
El álcali es un término que comúnmente usamos para los metales en el grupo 1 de la tabla periódica. Estos también se conocen como metales alcalinos. Aunque H también está en este grupo, es algo diferente; Tiene un comportamiento diferente de otros miembros de este grupo. Por lo tanto, el litio (Li), el sodio (NA), el potasio (K), el rubidio (RB), el cesio (CS) y el Francium (FR) son miembros de este grupo.
Los metales alcalinos son metales suaves, brillantes y plateados. Todos tienen solo un electrón en su carcasa externa, y les gusta eliminar esto y formar +1 cationes. Cuando la mayoría de los electrones externos se excita, regresa al estado fundamental mientras emite radiación en el rango visible. La emisión de este electrón es fácil; Por lo tanto, los metales alcalinos son muy reactivos. Además, la reactividad aumenta el grupo 1 de la tabla periódica.

Figura 01: hidróxido de sodio: un hidróxido de un metal alcalino
Estos metales forman compuestos iónicos con otros átomos electronegativos. Más exactamente, el término alcalino se refiere al carbonato o al hidróxido de un metal álcali. También tienen propiedades básicas. Son de sabor amargo, resbaladizo y reaccionan con ácidos, para neutralizarlos.
Que es la base?
Definiciones
Varios científicos definieron "base" de manera diferente. Arrhenius lo define como una sustancia que dona ohas a la solución. Bronsted-Lowry define una base como una sustancia que puede aceptar un protón. Según Lewis, cualquier donante de electrones es una base. Según la definición de Arrhenius, un compuesto debe tener un anión hidróxido y la capacidad de donarlo como un ion hidróxido para ser una base. Sin embargo, según Lewis y Bronsted-Lowry, puede haber moléculas, que no poseen hidróxidos, pero pueden actuar como base. Por ejemplo, NH3 es una base de Lewis, porque puede donar el par de electrones en nitrógeno. Del mismo modo, na2CO3 es una base de bronsted-Lowry sin grupos de hidróxido, pero puede aceptar hidrógenos.
Propiedades
Las bases tienen un jabón resbaladizo como la sensación y un sabor amargo. Reaccionan fácilmente con ácidos que producen agua y moléculas de sal. Los refrescos cáusticos, el amoníaco y el bicarbonato de sodio son algunas de las bases comunes. Podemos clasificar estos compuestos en dos grupos, dependiendo de su capacidad para disociar y producir iones de hidróxido. Son bases fuertes y débiles. Bases fuertes como NaOH, KOH, pueden ionizarse completamente en una solución, para dar iones. Bases débiles como NH3 disociar parcialmente y dar menos cantidades de iones de hidróxido.

Figura 02: Hidróxido de bario: una base del elemento del grupo 2 Bario
Además, Kb es la constante de disociación base. Indica la capacidad de perder iones de hidróxido de una base débil. Para verificar si una sustancia es una base o no, podemos usar varios indicadores como papel de fuego o papel de ph. Estos compuestos muestran un valor de pH superior a 7, y se convierte en rojo tornasol a azul.
¿Cuál es la diferencia entre álcali y base??
Los metales del Grupo 1 se denominan álcali, o con mayor precisión, sus carbonatos e hidróxidos se denominan álcali como álcali. Sin embargo, tienen propiedades básicas; Por lo tanto, son un subconjunto de bases. La diferencia clave entre álcali y base es que los elementos del Grupo 1 se clasifican como elementos álcali, mientras que cualquier elemento o compuesto que tenga propiedades básicas se clasifica como base. Por lo tanto, todos los álcalis son bases, pero no todas las bases son álcalis. Otra diferencia significativa entre álcali y base es que el álcali forma sales iónicas, mientras que las bases no son necesariamente tan.
La siguiente infografía sobre la diferencia entre álcali y base muestra estas diferencias en forma tabular.
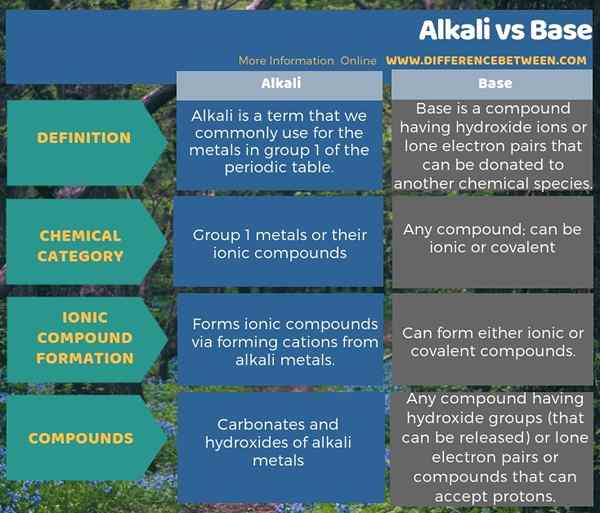
Resumen -Alkali vs Base
A menudo usamos los dos términos álcali y base indistintamente, pero son dos términos diferentes. La diferencia clave entre álcali y base es que los elementos del Grupo 1 se clasifican como elementos álcali, mientras que cualquier elemento o compuesto que tenga propiedades básicas se clasifica como base.
Referencia:
1. Britannica, los editores de Encyclopedia. "Álcali."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 14 de enero. 2014. Disponible aquí
2. "Base (Química)."Wikipedia, Fundación Wikimedia, 27 de noviembre. 2018. Disponible aquí
Imagen de cortesía:
1."Imagen de hidróxido de sodio" de Walkerma - Trabajo propio, (dominio público) a través de Commons Wikimedia
2."BA (OH) 2 Octahydrate" de Leiem - Trabajo propio, (CC By -Sa 4.0) a través de Commons Wikimedia


