Diferencia entre amoníaco y amonio
El diferencia clave entre amoníaco y amonio es que El amoníaco es una molécula polar no cargada que existe como gas a temperatura ambiente, mientras que los iones de amonio se cargan y existen como iones libres en solución o como compuestos de sal cristalizados.
Hay pocas imágenes e incluso ciertos olores que nuestras mentes se asocian inmediatamente con amoníaco o amonio; Estos incluyen los de fertilizantes, desechos nitrogenados, jabones e incluso explosivos. Además, la mayoría de las personas suponen que no hay diferencia entre el amoníaco y el amonio. La alta similitud entre estos dos y el uso de la palabra amoníaco con mayor frecuencia como un término general para los compuestos de amoníaco puro y de amonio es lo que provoca esta confusión.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es amoníaco
3. Que es amonio
4. Comparación de lado a lado: amoníaco vs amonio en forma tabular
5. Resumen
Que es amoníaco?
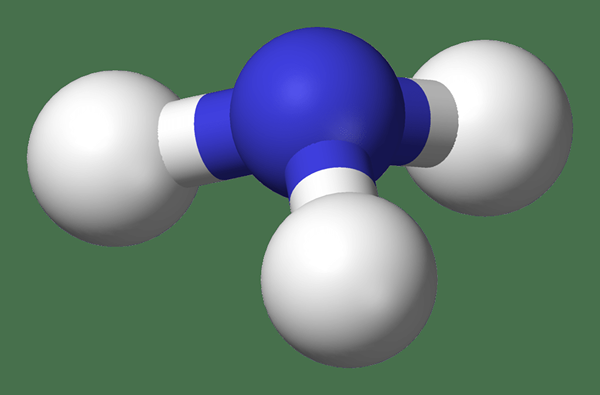
El amoníaco es un compuesto de nitrógeno e hidrógeno con la fórmula NH3. No está cargado y una molécula por sí misma; Existe como un gas a temperatura ambiente y presión atmosférica, y como líquido a temperaturas muy bajas y altas presiones. Llamamos a esta forma pura de amoníaco anhidro de amoníaco (sin agua). El gas de amoníaco es incoloro y tiene un olor agudo e intensamente irritante. Además, es tóxico.

Figura 01: molécula de amoníaco
El amoníaco, como el agua, es polar debido a su distribución de electrones desigual. Esta polaridad lo hace soluble en agua. Un punto importante a tener en cuenta es que el amoníaco solubilizado o acuoso está en forma de hidróxido de amonio, que se disocia aún más para formar iones de amonio e ión hidróxido. Esta disociación depende de la temperatura y el pH de la solución (la disociación aumenta con el aumento de la temperatura y la disminución del pH).
Que es amonio?
El catión de amonio es un ion poliatómico cargado positivamente con la fórmula química NH4+. Este es un ion que podría existir como iones libres en soluciones, o como un compuesto de sal iónico que forma una estructura de celosía con un anión; Por ejemplo, cloruro de amonio.
Por lo tanto, generalmente no usamos el término amonio como una palabra por sí misma; Siempre precede a las palabras 'ion ", sal' o el ion cargado negativamente respectivo. Por ejemplo, tiene que ser iones de amonio, hidróxido de amonio, nitrato de amonio, sulfato de amonio, etc., Y no solo el amonio.
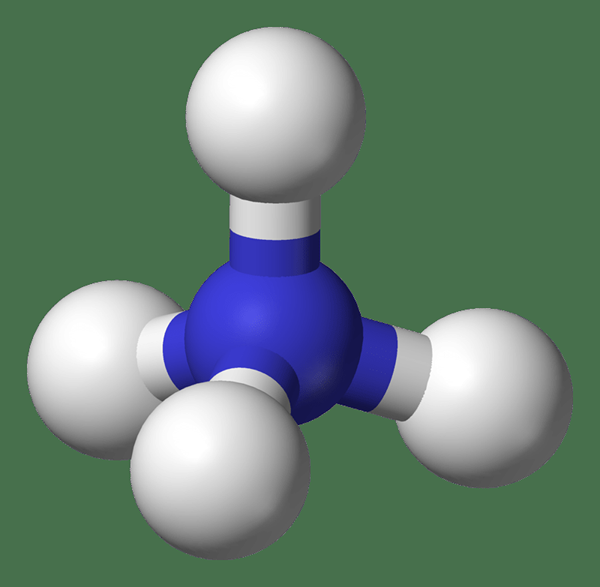
Figura 02: ion amonio
Los iones de amonio no tienen olores característicos; Sin embargo, las sales de amonio cuando están en solución acuosa con disociación lenta, dan a los olores característicos del amoníaco.
¿Cuál es la diferencia entre amoníaco y amonio??
El amonio es el catión principal que se origina en el amoníaco. La diferencia clave entre el amoniaco y el amonio es que el amoníaco es una molécula polar no cargada pero existente como un gas a temperatura ambiente, mientras que los iones de amonio se cargan y existen como iones libres en solución o como compuestos de sal cristalizados. Además, el amoníaco tiene un olor agudo e intensamente irritante, mientras que el ion amonio en sí no tiene un olor característico.
Al considerar la toxicidad, el amoníaco es tóxico pero los iones de amonio libres por sí mismos no son tóxicos. Sin embargo, los compuestos de amonio pueden ser tóxicos. Además, el amoníaco tiene un conjunto de características por sí misma, pero las características de los compuestos de amonio dependen del anión asociado, también.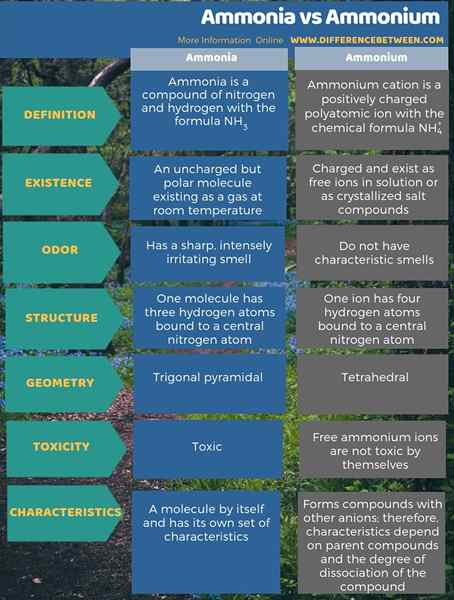
Resumen -Amoníaco vs amonio
En resumen, el amonio es el catión principal que se origina en el amoníaco. La diferencia clave entre el amoniaco y el amonio es que el amoníaco es una molécula polar no cargada pero existente como un gas a temperatura ambiente, mientras que los iones de amonio se cargan y existen como iones libres en solución o como compuestos de sal cristalizados.
Referencia:
1. "Pasos de proceso de producción de amoníaco."Amoníaco, PP. 65-176., doi: 10.1002/9783527613885.CH04.
Imagen de cortesía:
1. "Amoníaco-3D-balls" (dominio público) a través de Commons Wikimedia
2. "Amonio-3D-Balls" (dominio público) a través de Commons Wikimedia


