Diferencia entre amoníaco e hidróxido de amonio
El diferencia clave entre amoníaco e hidróxido de amonio es que El amoníaco ocurre como un gas, mientras que el hidróxido de amonio ocurre como líquido a temperatura ambiente.
Amoníaco e hidróxido de amonio tienen muchos usos para nosotros. Todos sabemos que el amoníaco es un gas de olfato picante con una fórmula química NH3. Cuando entra en contacto con el agua, lo que obtenemos es el hidróxido de amonio. Por lo tanto, a veces nombramos hidróxido de amonio como la "solución de amoníaco".
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es amoníaco
3. ¿Qué es el hidróxido de amonio?
4. Comparación lado a lado: amoníaco vs hidróxido de amonio en forma tabular
5. Resumen
Que es amoníaco?
El amoníaco es una sustancia gaseosa que tiene la fórmula química NH3. Es un compuesto inorgánico y también es el hidruro de pnictogen más simple. Es un gas incoloro pero tiene un olor picante e irritante. Además, el nombre IUPAC de amoníaco es Azano.
Algunos hechos químicos importantes sobre esta sustancia son los siguientes:
- La fórmula química es NH3
- La masa molar es 17.03 g/mol.
- Aparece como un gas incoloro
- El punto de fusión es −77.73 ° C
- El punto de ebullición es −33.34 ° C
Al considerar la ocurrencia de este compuesto, ocurre naturalmente pero en pequeñas cantidades. Eso es como producto de la materia nitrogenada de animales y vegetales. A veces, también podemos encontrar amoníaco en el agua de lluvia. Dentro de nuestro cuerpo, los riñones secretan amoníaco para neutralizar el exceso de ácido.

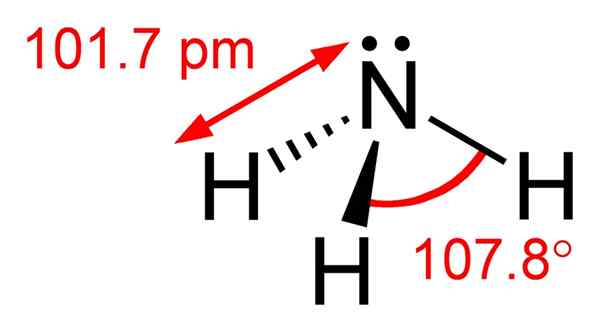
Figura 01: Estructura química de la molécula de amoníaco
En la estructura química de la molécula de amoníaco, tiene un átomo de nitrógeno unido a tres átomos de hidrógeno. Dado que hay cinco electrones en la cubierta de electrones más externa de nitrógeno, hay un par solitario de electrones en el átomo de nitrógeno de la molécula de amoníaco. Por lo tanto, la geometría de la molécula de amoníaco es trigonal piramidal. Además, podemos licuar este compuesto fácilmente. Esto se debe a que es capaz de formar enlaces de hidrógeno entre las moléculas de amoníaco, ya que también hay enlaces N-H y pares de electrones solitarios.
¿Qué es el hidróxido de amonio??
El hidróxido de amonio es una sustancia líquida que tiene la fórmula química NH4OH. También es un compuesto inorgánico. Podemos llamarlo como solución de amoníaco porque este compuesto se forma cuando el gas de amoníaco reacciona con agua. Por lo tanto, podemos denotarlo como NH3(aq). Aunque el nombre de hidróxido de amonio implica la existencia de un compuesto alcalino, en realidad es imposible aislar el compuesto químico hidróxido de amonio.
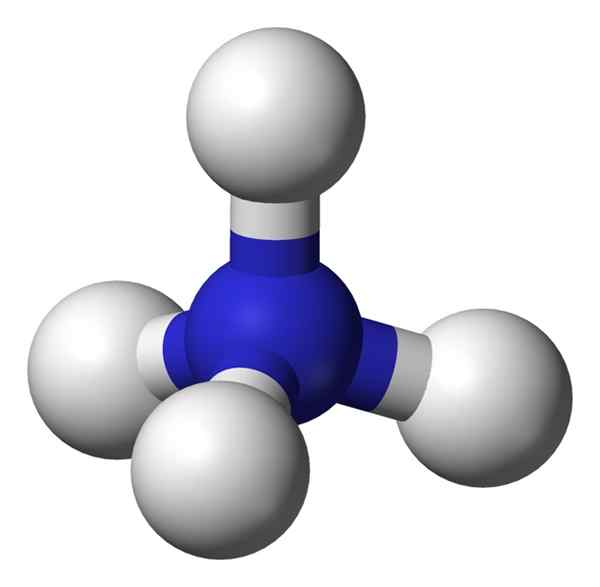
Figura 02: Modelo de pelota y palo para iones de amonio
Algunos hechos químicos importantes sobre este compuesto son los siguientes:
- La fórmula química es NH4OH
- La masa molar es 35.04 g/mol.
- Aparece como un líquido incoloro.
- Tiene un olor muy picante.
- El punto de fusión es −57.5 ° C
- El punto de ebullición es 37.7 ° C
Al considerar las aplicaciones de este líquido, es útil como un limpiador doméstico, como precursor de alquilo, para fines de tratamiento de agua, y muchas otras aplicaciones están ahí.
La reacción para la formación de este compuesto es la siguiente:
NUEVA HAMPSHIRE3 + H2O -> nh4+ + OH-
¿Cuál es la diferencia entre amoníaco e hidróxido de amonio??
El amoníaco es una sustancia gaseosa que tiene la fórmula química NH3, mientras que el hidróxido de amonio es una sustancia líquida que tiene la fórmula química NH4OH. Por lo tanto, la diferencia clave entre el amoníaco y el hidróxido de amonio existe en sus estados físicos. Es decir, la diferencia entre amoníaco e hidróxido de amonio es que el amoníaco ocurre como un gas, mientras que el hidróxido de amonio ocurre como un líquido a temperatura ambiente. Dado que se forma hidróxido de amonio cuando el gas amoníaco se disuelve en agua, también llamamos a este compuesto como solución de amoníaco o amoníaco líquido. Además, otra diferencia entre el amoníaco y el hidróxido de amonio es que el amoníaco es anhidro, mientras que el hidróxido de amonio es hidratado.

Resumen -Amoníaco vs hidróxido de amonio
Forma de hidróxido de amonio a partir de la disolución de gas amoníaco en agua. Por lo tanto, el hidróxido de amonio en realidad es una solución acuosa de amoníaco. Sin embargo, la diferencia clave entre el amoníaco y el hidróxido de amonio es que el amoníaco ocurre como un gas, mientras que el hidróxido de amonio ocurre como un líquido a temperatura ambiente.
Referencia:
1. "Amoníaco."Wikipedia, Fundación Wikimedia, 16 de octubre. 2018. Disponible aquí
2. "Solucion de amoniaco."Wikipedia, Fundación Wikimedia, 17 de octubre. 2018. Disponible aquí
Imagen de cortesía:
1.Amonia-Dimensiones de Greenwood & Earnshaw-2d ”por Ben Mills-Trabajo propio, (Dominio Público) a través de Commons Wikimedia
2."Amonio-3D-Balls" (dominio público) a través de Commons Wikimedia


