Diferencia entre elementos atómicos y moleculares

El diferencia clave entre elementos atómicos y moleculares es que el El elemento atómico es una especie química que existe como átomos independientes, mientras que el elemento molecular es una sustancia molecular que consta de dos o más átomos de un solo elemento.
Los elementos atómicos son los elementos químicos más estables; principalmente los gases nobles. Por lo tanto, pueden existir como átomos independientes. Pero también pueden someterse a reacciones químicas para formar compuestos. En contraste, los elementos moleculares son compuestos químicos que contienen al menos dos átomos del mismo elemento químico. Estos átomos se unen entre sí a través de la formación de enlaces químicos entre los átomos.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué son los elementos atómicos?
3. ¿Qué son los elementos moleculares?
4. Comparación de lado a lado - Elementos atómicos vs moleculares en forma tabular
5. Resumen
¿Qué son los elementos atómicos??
Los elementos atómicos son las especies químicas que pueden existir como átomos independientes. Esto se debe a su alta estabilidad. Solo hay un átomo en la fórmula química de estos elementos. Por lo tanto, no hay subíndices numéricos con el símbolo de los elementos atómicos.

Figura 01: diferentes gases nobles
Gases nobles
Los gases nobles son los elementos del Grupo 8 de la tabla periódica que tiene configuraciones de electrones completas. Debido a esta configuración completa de electrones, estos átomos pueden existir como átomos individuales sin formar ningún enlace químico. Pero con las condiciones específicas proporcionadas, pueden formar enlaces químicos. Los gases nobles que conocemos son Helium (He), Neon (NE), Argón (AR), Krypton (KR), Xenon (Xe) y Radon (RA).
¿Qué son los elementos moleculares??
Los elementos moleculares son las especies químicas que tienen al menos dos átomos del mismo elemento químico unidos entre sí a través de la unión química. Estos son diferentes de los compuestos químicos porque un compuesto químico contiene dos o más átomos de diferentes elementos químicos.
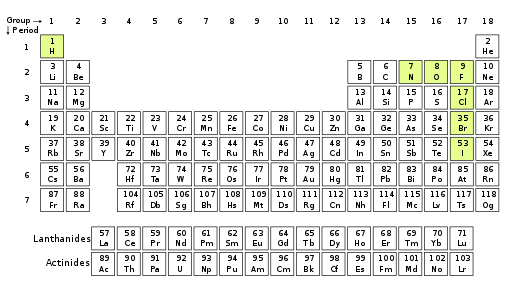
Figura 01: Elementos químicos capaces de formar moléculas diatómicas con dos átomos del mismo elemento químico.
Además, la fórmula química de los elementos moleculares contiene un símbolo químico con un subíndice numérico que indica el número de átomos presentes en la molécula, algunos ejemplos comunes incluyen o2, H2, norte2, CL2, etc.
¿Cuál es la diferencia entre los elementos atómicos y moleculares??
Elementos atómicos y moleculares, ambos términos describen la presencia de un solo tipo de elemento químico en esas especies químicas. Sin embargo, la diferencia clave entre los elementos atómicos y moleculares es que un elemento atómico es una especie química de átomos que contiene el mismo número de protones en los núcleos atómicos, mientras que un elemento molecular es una sustancia molecular que consiste en un solo elemento. Al considerar sus fórmulas químicas, podemos identificar una diferencia entre los elementos atómicos y moleculares. Es decir, el elemento atómico tiene solo un símbolo químico sin subíndices numéricos, mientras que los elementos moleculares tienen un símbolo químico con un subíndice numérico.
La siguiente infografía presenta la diferencia entre los elementos atómicos y moleculares en forma tabular.
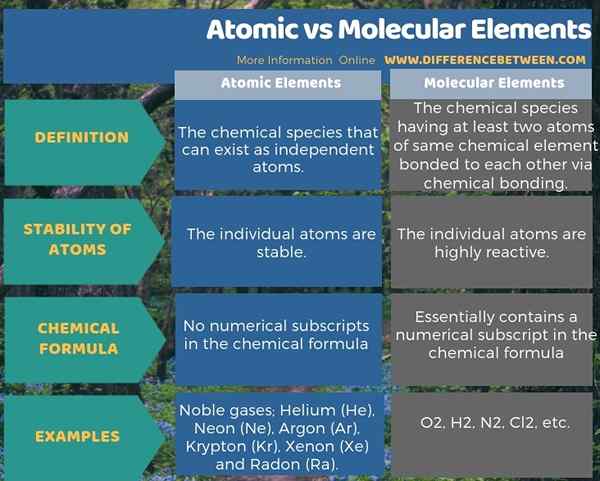
Resumen -Elementos Atomic vs Moleculares
Ambos términos, elementos atómicos y moleculares, describen las especies químicas que tiene un solo tipo de elemento químico en lugar de diferentes elementos químicos. La diferencia clave entre el elemento atómico y molecular es que un elemento atómico es una especie química de átomos que contiene el mismo número de protones en los núcleos atómicos, mientras que un elemento molecular es una sustancia molecular que consiste en un solo elemento.
Referencia:
1. Bibliotecas. "5.4: Una vista molecular de elementos y compuestos."Bibliotecas de química, Librettexts, 4 de mayo de 2018. Disponible aquí
2. "Moléculas y átomos."Propiedades de fósforo. Disponible aquí
Imagen de cortesía:
1.Edelgase en Entladungsroehren ”por Alchemist-HP-Trabajo propio, (CC By-SA 2.0 de) a través de Commons Wikimedia
2."Moléculas diatómicas de la tabla periódica" por White_Periodic_Table.SVG (dominio público) a través de Commons Wikimedia


