Diferencia entre el número de Azimutal y el principal
El diferencia clave Entre el número cuántico azimutal y principal es que El número cuántico azimutal describe el momento angular de un electrón en un átomo, mientras que el número cuántico principal describe el tamaño de un orbital de electrones.
Los números cuánticos son valores que son importantes para describir los niveles de energía de un átomo. Hay cuatro números cuánticos que podemos usar para describir la posición de un electrón en un átomo. Son el número cuántico principal, el número cuántico azimutal, el número cuántico magnético y el número cuántico giratorio.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el número cuántico azimutal?
3. ¿Qué es el número cuántico principal?
4. Comparación de lado a lado - Número cuántico Azimutal vs principal en forma tabular
5. Resumen
¿Qué es el número cuántico azimutal??
El número cuántico azimutal es el número cuántico que describe el momento angular de un electrón en un átomo. Por lo tanto, también podemos llamarlo el número cuántico de momento angular orbital. La carta "l"Denota el número cuántico azimutal. Además, este número cuántico determina las formas de un orbital en el que existe un electrón. Es el segundo del conjunto de cuatro números cuánticos. Por lo tanto, podemos nombrarlo como el segundo número cuántico también (porque los cuatro números cuánticos describen el estado cuántico de un electrón en un átomo). La ecuación que puede relacionar el número cuántico azimutal con el momento angular es la siguiente:
L2Ψ =H2l(l+1) ψ
Donde l2 es el operador de momento angular orbital, ψ es la función de onda del electrón y H es la constante de tabla reducida. Aquí, I es siempre un entero positivo. Según la mecánica cuántica, cada nivel de energía tiene diferentes subshells. Estas subshells difieren entre sí en su forma y orientación. Las subshells de un nivel de energía se nombran como -I, 0 y +l.
| Número azimutal | Denotación | Número de orbitales | Número máximo de electrones |
| 0 | s | 1 | 2 |
| 1 | pag | 3 (= -1, 0, +1) | 6 |
| 2 | d | 5 (= -2, -1, 0, +1, +2) | 10 |
| 3 | F | 7 (= -3, -2, -1, 0, +1, +2, +3) | 14 |

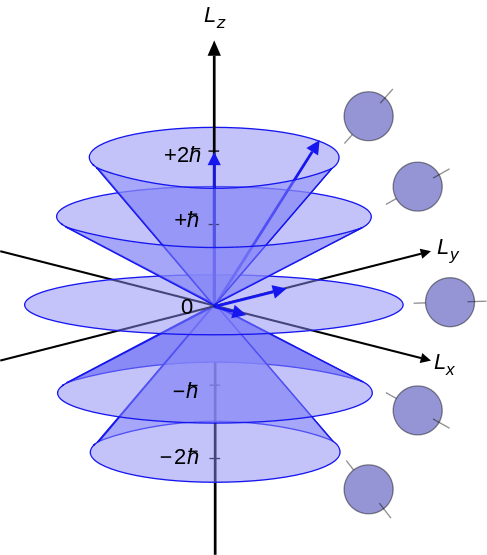
Figura 02: números cuánticos azimutales que van desde -l, 0 a +l
¿Qué es el número cuántico principal??
Un número cuántico principal es un número cuántico que describe el nivel de energía principal en el que existe un electrón. Podemos denotarlo como "n". Ya que es el primero de cuatro números cuánticos diferentes; Podemos llamarlo el primer número cuántico también. El valor del número cuántico principal es un entero positivo a partir de 1, i.mi. n = 1, 2, 3, ..
Mayor el valor del número cuántico principal, mayor la energía de un electrón; Por lo tanto, el electrón está unido libremente al átomo. Eso significa; Los altos valores "n" se refieren a niveles de energía más altos. Además, para cada valor "n", existen valores separados para el número cuántico azimutal, el número cuántico magnético y el número cuántico de giro. Es porque cada nivel de energía tiene sus propias subshells, orbitales y pares de electrones, respectivamente.
¿Cuál es la diferencia entre el número cuántico azimutal y principal??
Los números cuánticos son valores que son importantes para describir los niveles de energía de un átomo. Hay cuatro números cuánticos diferentes, y los dos primeros son el número cuántico principal y el número cuántico azimutal. La diferencia clave entre el número cuántico azimutal y principal es que el número cuántico azimutal describe el momento angular de un electrón en un átomo, mientras que el número cuántico principal describe el tamaño de un electrón orbital. Podemos denotar el número cuántico azimutal como "l"Y el número cuántico principal como" n ".
Además, el número cuántico azimutal describe el momento angular y la forma de un orbital, mientras que el número cuántico principal describe el nivel de energía en el que existe un electrón.
A continuación, la infografía resume la diferencia entre el número cuántico azimutal y principal.
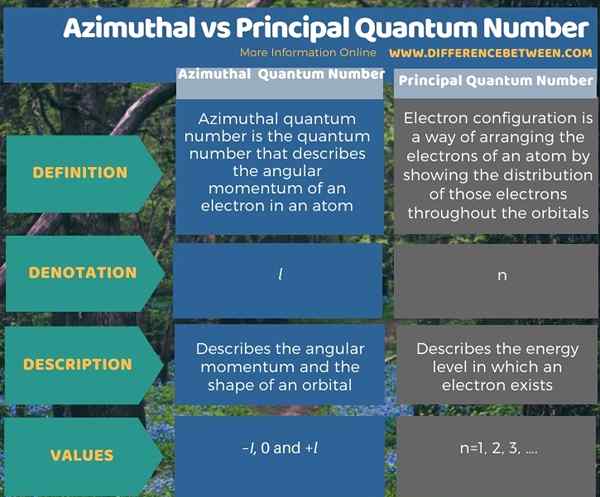
Resumen -Azimutal vs Número cuántico principal
Los números cuánticos son valores que describen los niveles de energía de un átomo. Hay cuatro números cuánticos diferentes, y los dos primeros son el número cuántico principal y el número cuántico azimutal. La diferencia clave entre el número cuántico azimutal y principal es que el número cuántico azimutal describe el momento angular de un electrón en un átomo, mientras que el número cuántico principal describe el tamaño de un electrón orbital.
Referencia:
1. Helmenstine, Anne Marie. "Definición de número cuántico azimutal."Thinkco, junio. 22, 2018, disponible aquí.
2. Helmenstine, Anne Marie. "Definición de número cuántico principal."Thinkco, nov. 6, 2019, disponible aquí.
Imagen de cortesía:
1. "Modelo vectorial del momento angular orbital" por Maschen - Trabajo propio (dominio público) a través de Commons Wikimedia


