Diferencia entre el punto de ebullición y el punto de fusión

El diferencia clave entre el punto de ebullición y el punto de fusión es que El punto de ebullición es la temperatura a la que un estado líquido cambia a su estado gaseoso, mientras que el punto de fusión es la temperatura a la que un estado sólido cambia a un estado líquido.
Hay tres estados de materia: estado sólido, estado líquido y estado gaseoso. Las sustancias pueden cambiar de un estado en particular a otro si variamos la temperatura de esa sustancia. Al calentar, generalmente un cambio sólido en su estado líquido; y al calentar aún más, se transforma en su estado gaseoso. Por el contrario, si nos enfriamos un compuesto gaseoso, cambia en el estado líquido, seguido de un estado sólido al enfriar más. Sin embargo, hay algunas sustancias sólidas que pueden ir directamente al estado gaseoso sin pasar por el estado líquido (llamamos a esto sublimación) y viceversa.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es el punto de ebullición
3. Que es el punto de fusión
4. Comparación de lado a lado: punto de ebullición vs punto de fusión en forma tabular
6. Resumen
Que es el punto de ebullición?
El punto de ebullición es una propiedad de un líquido. El punto de ebullición es la temperatura a la que la presión de vapor del líquido es igual a la presión externa sobre el líquido. La presión es un factor importante que afecta el punto de ebullición; mayor la presión externa sobre una sustancia, más alto el punto de ebullición. Por lo tanto, esta es la teoría simple detrás de las cocinas a presión. Una olla a presión es una olla que atrapa el vapor del agua calentada dentro de ella. La gran cantidad de vapor dentro del contenedor hace que la presión externa sobre el líquido sea mayor. En consecuencia, esta alta presión da como resultado un punto de ebullición más alto. Además, esta teoría es muy útil, especialmente en altitudes más altas. Por lo general, el agua hierve a 1000C. Dado que la presión atmosférica es menor a altitudes más altas, el agua hervirá entre 80 0C - 90 0C. Y esto causará comidas poco cocidas.

Figura 01: agua hirviendo en el punto de ebullición
Un líquido hierve cuando excede su temperatura de saturación a la presión de saturación correspondiente. La temperatura de saturación es la temperatura correspondiente a la energía térmica más alta que el líquido puede contener sin cambiar su estado a vapor a la presión dada. La temperatura de saturación también es equivalente al punto de ebullición del líquido. La ebullición ocurre cuando la energía térmica del líquido es suficiente para romper los enlaces intermoleculares. El punto de ebullición normal es la temperatura de saturación a presión atmosférica. Además, el punto de ebullición varía solo entre el punto triple y el punto crítico del líquido.
Que es el punto de fusión?
El punto de fusión es una propiedad de un sólido. El punto de fusión es la temperatura a la que el sólido se convierte en un líquido. Más precisamente, el punto de fusión es la temperatura cuando el estado líquido y el estado sólido permanecen en equilibrio térmico entre sí.

Figura 2: hielo derretido
El punto de fusión y el punto de congelación de una sustancia podrían no ser el mismo. Por ejemplo, el agar se derrite a los 85 0C, pero se solidifica a los 31 0C a 40 0C. Los enlaces intermoleculares y el peso molecular definen principalmente el punto de fusión. Algunos sólidos como el vidrio no tienen un punto de fusión específico. Simplemente se someten a una transición suave de sólido a líquido.
¿Cuál es la diferencia entre el punto de ebullición y el punto de fusión??
El punto de ebullición y el punto de fusión son propiedades de las sustancias. La diferencia clave entre el punto de ebullición y el punto de fusión es que el punto de ebullición es la temperatura a la que un estado líquido cambia a su estado gaseoso, mientras que el punto de fusión es la temperatura a la que un estado sólido cambia a un estado líquido. Por lo tanto, el punto de ebullición se define para un estado líquido, mientras que el punto de fusión se define para un estado sólido.
La siguiente información Graphic presenta más detalles sobre la diferencia entre el punto de ebullición y el punto de fusión.
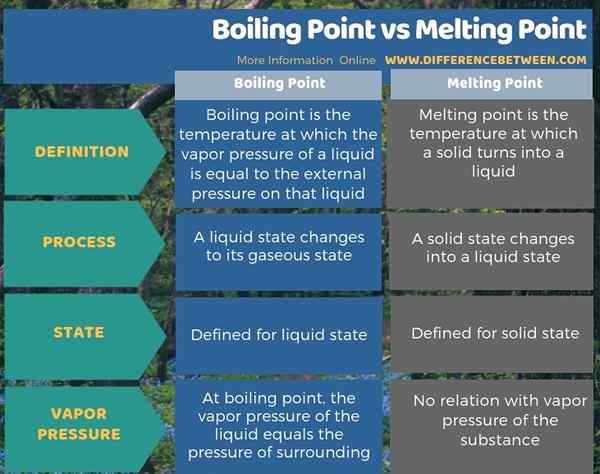
Resumen -Punto de ebullición vs Punto de fusión
Tanto el punto de ebullición como el punto de fusión son propiedades de la materia. Juegan un papel muy importante cuando se trata de describir un material. La diferencia clave entre el punto de ebullición y el punto de fusión es que el punto de ebullición es la temperatura a la que un estado líquido cambia a su estado gaseoso, mientras que el punto de fusión es la temperatura a la que un estado sólido cambia a un estado líquido.
Referencia:
1. "Punto de ebullición."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 20 de febrero. 2018, disponible aquí.
2."Punto de fusion."Wikipedia, Fundación Wikimedia, 12 de mayo de 2019, disponible aquí.
Imagen de cortesía:
1. "Agua hirviendo" de Scott Akerman (CC por 2.0) a través de Flickr
2. "Termómetro de hielo de derretimiento" de Ulflund - Trabajo propio (CC0) a través de Commons Wikimedia


