Diferencia entre boro y bórax

El diferencia clave Entre Boron y Borax es que el Boron es un elemento químico, mientras que el bórax es un compuesto químico. Además, Borax es un compuesto que contiene Boron, y es un mineral.
Aunque los nombres de Boron y Borax suenan casi similares, son diferentes entre sí de acuerdo con la naturaleza química. Discutamos más detalles sobre ellos.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es Boron
3. Que es bórax
4. Comparación de lado a lado - Boron vs bórax en forma tabular
5. Resumen
Que es Boron?
Boron es un elemento químico que tiene el símbolo B y el número atómico 5. Su abundancia en la corteza terrestre es muy baja, y también es un elemento traza en el sistema solar. Es un metaloide y la mayoría de las veces, y no ocurre naturalmente. Además, Boron está en el Grupo 13 y el período 2 de la tabla periódica. Por lo tanto, es el primer miembro del bloque P. Esto se debe a que tiene un solo electrón en el orbital 2p. A presión y temperatura estándar, existe como un sólido. El punto de fusión y el punto de ebullición son 2076 ° C y 3927 ° C respectivamente.

Figura 01: Estructuras moleculares de boro
Boron puede formar redes moleculares similares al carbono. Estas estructuras tienen enlaces covalentes entre los átomos de boro. Estas estructuras son las alotropas de Boron. El comportamiento químico de este elemento se asemeja al silicio. El boro cristalino es muy poco reactivo; Por lo tanto, no reacciona con HF o HCl al calentar. Además, el boro forma óxidos, sulfuros, nitruros y haluros con su estado de oxidación más común; +3 estado de oxidación.
Que es bórax?
El bórax es un compuesto inorgánico que tiene la fórmula química na2B4O7· 10h2O. Es una sal de ácido bórico. Existe como un sólido blanco consisten en cristales suaves e incoloros. Estos cristales son solubles en agua. Por lo general, este compuesto existe como la forma de Decahydrate. El nombre de IUPAC de este compuesto es el decahidrato tetraborado de sodio. La masa molar de la forma de decahidrato es 381.4 g/mol. El punto de fusión y los puntos de ebullición son 743 ° C y 1.575 ° C respectivamente.

Figura 02: Cristales bórax
El nombre de bórax se refiere a una colección de compuestos que incluye formas anhidro e hidratadas de bórax. Ej: forma de pentahidrate, forma de decahydrate. Reacciona con ácido HCl que forma ácido bórico.
N / A2B4O7· 10h2O + 2 HCL → 4 H3Bo3 + 2 NaCl + 5 H2O
Este compuesto ocurre naturalmente en los depósitos de evaporita; Estos depósitos se forman debido a la evaporación repetida de los lagos estacionales. Podemos refinar este compuesto a través de la recristalización. Además de eso, este compuesto es útil como agente de limpieza, para hacer amortiguadores, como fuente de iones de borato para actuar como agente co-complejo, etc.
¿Cuál es la diferencia entre boro y bórax??
Boron es un elemento químico que tiene el símbolo B y el número atómico 5, mientras que el bórax es un compuesto inorgánico que tiene la fórmula química na2B4O7· 10h2O. Por lo tanto, la diferencia clave es que el boro es un elemento químico, mientras que el bórax es un compuesto químico. Además, el punto de fusión y los puntos de ebullición del boro son 2076 ° C y 3927 ° C respectivamente. Por otro lado, el punto de fusión y los puntos de ebullición del bórax son 743 ° C y 1.575 ° C respectivamente. La siguiente infografía presenta más detalles sobre la diferencia entre Boron y Borax.
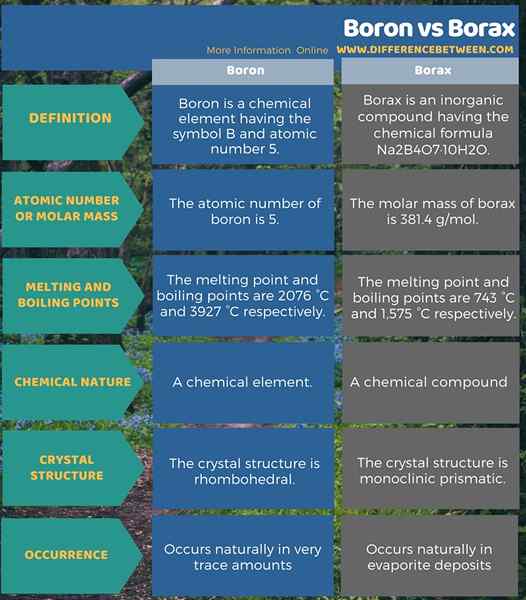
Resumen -Boron vs bórax
Bórax es un compuesto de boro. Sin embargo, son muy diferentes entre sí en la naturaleza química. La diferencia clave entre Boron y Borax es que el boro es un elemento químico, mientras que el bórax es un compuesto químico.
Referencia:
1. "Boro."Wikipedia, Fundación Wikimedia, 24 de julio de 2018. Disponible aquí
2. "Bórax."Wikipedia, Fundación Wikimedia, 23 de julio de 2018. Disponible aquí
Imagen de cortesía:
1.'Boron R105' por James L Marshall (CC por 3.0) a través de Commons Wikimedia
2.'Cristales de borax' por Aram Dulyan (Usuario: Aramgutang) - Trabajo propio, (dominio público) a través de Commons Wikimedia


