Diferencia entre la reducción carbotérmica y metalotérmica
El diferencia clave entre la reducción carbotérmica y metalotérmica es que En la reducción carbotérmica, el agente reductor es el carbono, mientras que, en la reducción metalotérmica, el agente reductor es un metal.
La reducción carbotérmica y la reducción metalotérmica son reacciones muy importantes para obtener metal puro. Estas reacciones se aplican principalmente en procesos industriales.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la reducción carbotérmica?
3. ¿Qué es la reducción metalotérmica?
4. Comparación lado a lado: reducción carbotérmica frente a metalotérmica en forma tabular
5. Resumen
¿Qué es la reducción carbotérmica??
La reacción de reducción carbotérmica es un tipo de reacción química en la que se produce la reducción de sustancias como el óxido de metal en presencia de carbono. Aquí, el carbono tiende a actuar como el agente reductor. Por lo general, este tipo de reacciones químicas ocurre a temperaturas muy altas. Estas reacciones de reducción carbotérmica son muy importantes en la producción de las formas elementales de muchos elementos. Podemos predecir fácilmente la capacidad de los metales para participar en reacciones carbotérmicas utilizando diagramas de Ellingham.
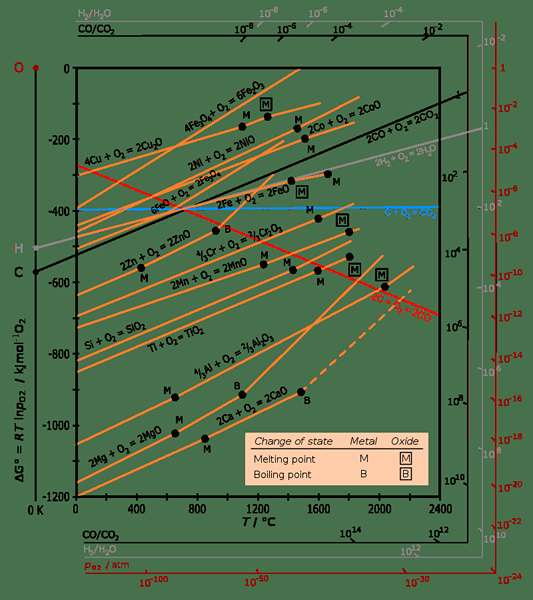
El diagrama de Ellingham es un gráfico que muestra la dependencia de la temperatura de la estabilidad de los compuestos. En general, este análisis es útil para elevar la facilidad de reducción de óxidos metálicos y sulfuros. El nombre proviene de su descubrimiento de Harold Ellingham en 1944.

Figura 01: un diagrama de Ellingham
Las reacciones de reducción carbotérmica pueden producir monóxido de carbono e incluso dióxido de carbono a veces. Podemos describir la conversión de los reactivos en los productos con respecto al cambio de entropía. En esta reacción, dos compuestos sólidos (óxido de metal y carbono) se convierten en un nuevo compuesto sólido (metal) y un gas (monóxido de carbono o dióxido de carbono). La última reacción tiene una alta entropía.
Hay muchas aplicaciones de reacciones de reducción carbotérmica, incluida la fundición del mineral de hierro como la principal aplicación. Aquí, el mineral de hierro se reduce en presencia de carbono como agente reductor. Esta reacción proporciona metal de hierro y dióxido de carbono como productos. Otro ejemplo importante es el proceso de Leblanc donde reacciona el sulfato de sodio con el carbono, dando sulfuro de sodio y dióxido de carbono.
¿Qué es la reducción metalotérmica??
La reacción de reducción metalotérmica es un tipo de reacción química que se realiza para obtener un metal objetivo o una aleación de material de alimentación como óxidos o cloruros mediante el uso de un metal como agente reductor. La mayoría de los metales reactivos se obtienen a través de este proceso de reducción. mi.gramo. metal de titanio.
Un ejemplo común de este tipo de reacción es la purificación del metal de Niobium. En esta reacción de reducción, el óxido de niobio se reduce mediante metal de aluminio para dar metal de niobio y óxido de aluminio. Es una reacción exotérmica donde las impurezas de óxido se escoren, y podemos eliminarlas del metal de niobio fundido.
¿Cuál es la diferencia entre la reducción carbotérmica y metalotérmica??
La reducción carbotérmica y la reducción metalotérmica son reacciones muy importantes para obtener un metal puro. La reacción de reducción carbotérmica es un tipo de reacción química en la que se produce la reducción de sustancias como el óxido de metal en presencia de carbono. Una reacción de reducción metalotérmica, por otro lado, es un tipo de reacción química para obtener un metal objetivo o una aleación de material de alimentación como óxidos o cloruros mediante el uso de un metal como agente reductor. La diferencia clave entre la reducción carbotérmica y metalotérmica es que en la reducción carbotérmica el agente reductor es el carbono, mientras que en la reducción metalotérmica el agente reductor es un metal.
A continuación, la infografía resume las diferencias entre la reducción carbotérmica y metalotérmica en forma tabular.

Resumen -Reducción carbotérmica vs metalotérmica
La reducción carbotérmica y la reducción metalotérmica son reacciones muy importantes para obtener un metal puro. La diferencia clave entre la reducción carbotérmica y metalotérmica es que en la reducción carbotérmica, el agente reductor es el carbono, mientras que, en la reducción metalotérmica, el agente reductor es un metal.
Referencia:
1. "Reducción metalotérmica."Science Direct, disponible aquí.
Imagen de cortesía:
1. "Ellingham Richardson-Diagram English" de Dersilberspiegel-hecho a sí mismo con la mayoría de los datos de aquí [1] (CC by-sa 4.0) a través de Commons Wikimedia


