Diferencia entre la reacción química y física

Diferencia clave: reacción química versus física
La reacción química y física son dos tipos de cambios en la materia y el diferencia clave entre la reacción química y la reacción física es que Cuando una sustancia se somete a una reacción química, ya no es el compuesto original eso fue allí antes de la reacción mientras, Una sustancia que sufre una reacción física sigue siendo la sustancia original mientras su estado o la forma cambia. Sin embargo, en las reacciones químicas y físicas, la energía total permanece constante.
¿Qué es una reacción química??
Se produce una reacción química cuando se combinan dos o más sustancias para formar una sustancia completamente nueva o para cambiar las propiedades originales de los compuestos iniciales. Durante una reacción química, se cambian las propiedades químicas de los compuestos iniciales. Esto implica romper o hacer enlaces químicos.
Las sustancias presentes al comienzo de la reacción se denominan "reactivos" y las sustancias recién formadas se denominan "productos". El número de elementos presentes en los reactivos es igual al número de elementos presentes en los productos.
Ejemplo 1: Combustión de combustibles fósiles
2C2H6 + 7O2 → 4 CO2 + 6 h2O
(Reactivos) (productos)

La explosión de los fuegos artificiales es un ejemplo de reacción química.
¿Qué es una reacción física??
Las reacciones físicas en las sustancias también se conocen como "cambios físicos". Para comprender la reacción física, es esencial tener una idea clara sobre las propiedades físicas del asunto. Las propiedades físicas son las propiedades que no cambian la naturaleza química del asunto. Esas propiedades se pueden medir sin cambiar la composición de la materia. Las propiedades físicas incluyen apariencia, textura, color, olor, punto de fusión, punto de ebullición, densidad, solubilidad, etc.
Las reacciones físicas implican un cambio en la forma de materia o forma, pero no hay cambios en su composición.
Ejemplo 1: Mezcla de azúcar en agua
Esta es una reacción física. Porque no se crea nada nuevo mezclando azúcar con agua. El resultado es solo azúcar en el agua. Si evapora la mezcla, puede obtener los compuestos iniciales.
Ejemplo2: Congelación de agua, fusión de hielo y evaporación del agua.
Todos estos tres procesos son cambios físicos del agua. En cualquiera de estos, los cambios no implican los cambios en la composición. Es agua en diferentes formas.
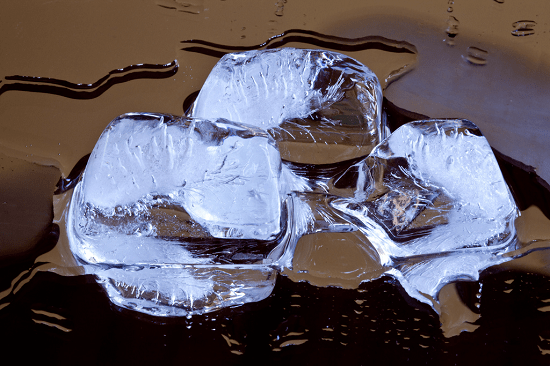
La fusión del hielo es un ejemplo de una reacción física
¿Cuál es la diferencia entre la reacción química y física??
Definición de reacción química y física
Reacción química: La reacción química es cualquier cambio que resulte en la formación de nuevas sustancias químicas.
Reacción física:La reacción física es un cambio que afecta la forma de una sustancia química, pero no su composición química.
Características de la reacción química y física
Cambios en los compuestos y la composición originales
Reacción química: Las reacciones químicas dan como resultado un cambio de las propiedades originales de los compuestos iniciales o forman una (s) compuesta (s) completamente nueva (s).
Reacción física: Las reacciones físicas no cambian la composición de los elementos o los compuestos, pero resulta en un cambio en el estado.
| Cambios físicos | Cambios químicos |
| Ruptura de vidrio | Una bicicleta oxidada |
| Mostar madera juntos | comida podrida |
| Mantequilla de derretimiento para palomitas de maíz | metal corroído |
| Separar la arena de la grava | blanqueando tu cabello |
| Cortar el césped | fuegos artificiales explotando |
| Sprepling naranjas para hacer jugo de naranja. | Hojas ardientes |
| Hacer agua salada para hacer gárgaras con | Tostada quemada |
| Helado derretido | Freír un huevo |
Reversibilidad
Reacción química: La mayoría de las reacciones químicas son irreversibles.
Reacción física: Las reacciones físicas son reversibles.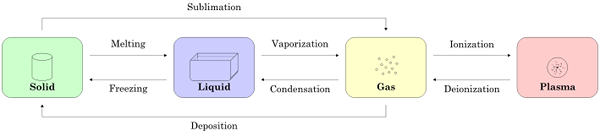
Cambios de propiedades
Reacción química: Al menos uno de los siguientes cambios tiene lugar en una reacción química.
Cambios en una reacción química:
- Cambio de color
- Formación de un sólido (reacciones de precipitación)
- Formación de gas o olfato (reacciones de efervescencia)
- Cambio de energía (reacción endotérmica o exotérmica)
Reacción física: Una sustancia que experimenta una reacción física; cambia su forma o la fase, permaneciendo la sustancia tal como está.
Requisito de energía
Reacción química: Hay una cierta barrera de energía que debe superarse para someterse a una reacción química. Se llama "energía de activación".
Reacción física:No existe tal requisito de energía en las reacciones físicas.
Imagen cortesía: "Física Matter State Transition 1 EN" de Elfqrin - Trabajo propio. (GFDL) a través de Wikimedia Commons derritiendo cubitos de hielo por jar [o] [CC por 2.0] a través de Flickr

