Diferencia entre clorato y perclorato
El diferencia clave entre clorato y perclorato es que El clorato es el anión derivado de la disociación del ácido clórico, mientras que el perclorato es el anión derivado de la disociación del ácido perclórico.
El clorato y el perclorato son oxianiones que contienen átomos de cloro y oxígeno. En general, estos términos se usan también para nombrar las sales de ácido clórico y perclórico respectivamente. En otras palabras, el término clorato puede referirse a cualquier compuesto que contenga anión de clorato con otro catión.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es el clorato
3. ¿Qué es el perclorato?
4. Comparación de lado a lado: clorato vs perclorato en forma tabular
5. Resumen
Que es el clorato?
El clorato es un anión que tiene la fórmula química clo3-. El estado de oxidación del átomo de chorina es +5. Sin embargo, los compuestos químicos que contienen este anión también se denominan clorates como un término general. Este anión es la sal del ácido quórico. La estructura de este anión es la siguiente:
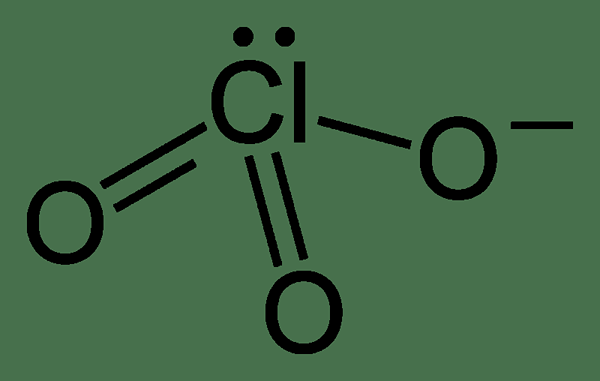
La geometría de este anión es trigonal piramidal. Además, los compuestos que contienen este anión son oxidizadores fuertes. Por lo tanto, tenemos que mantenerlos alejados de los materiales fácilmente oxidados. Este anión puede mostrar resonancia; Por lo tanto, la estructura real del clorato es una estructura híbrida, que tiene todo el enlace CL-O con la misma longitud. Además, el átomo de cloro aquí es hipervalente. Esto significa que el átomo de cloro tiene más de ocho electrones a su alrededor.
Al considerar la preparación, en el laboratorio, podemos producir cloratos agregando cloro a hidróxidos calientes, i.mi. Koh. En la escala industrial, podemos producirlo a partir de la electrólisis del cloruro de sodio acuoso.
¿Qué es el perclorato??
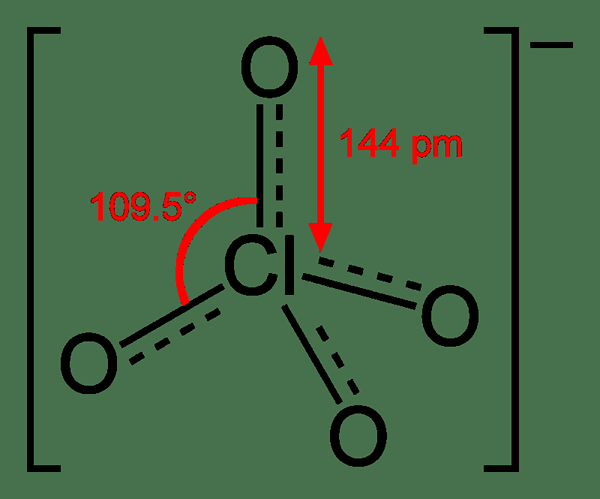
El perclorato es un anión que tiene la fórmula química clo4-. Se origina en el ácido perclórico. En general, este término puede referirse a cualquier compuesto que contenga anión por perclorato. El estado de oxidación del átomo de chorina en este compuesto es +7. Es la forma menos reactiva entre otros clorates. La geometría de este ion es tetraédrica.

Principalmente, los compuestos que contienen este anión existen como sólidos incoloros que son solubles en agua. Este anión se forma cuando los compuestos de perclorato se disocian en agua. En la escala industrial, podemos producir este ion a través del método de electrólisis; Aquí, se produce la oxidación del clorato de sodio acuoso.
¿Cuál es la diferencia entre clorato y perclorato??
La diferencia clave entre clorato y perclorato es que el clorato es el anión derivado de la disociación del ácido clórico, mientras que el perclorato es el anión derivado de la disociación del ácido perclórico. Además, el estado de oxidación del átomo de cloro en el clorato es +5 y el estado de oxidación del perclorato es +7. Al considerar la geometría de estos aniones, el anión clorato tiene geometría piramidal trigonal y el anión perclorato tiene geometría tetraédrica.
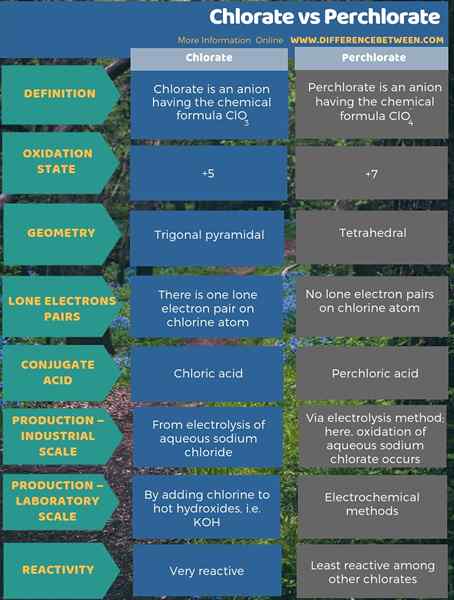
Resumen -Clorato vs perclorato
El clorato y el perclorato son básicamente oxianiones de chorino. La diferencia clave entre clorato y perclorato es que el clorato es el anión derivado de la disociación del ácido clórico, mientras que el perclorato es el anión derivado de la disociación del ácido perclórico.
Referencia:
1. "Clorato."Wikipedia, Fundación Wikimedia, 27 de agosto. 2019, disponible aquí.
Imagen de cortesía:
1. "Clorato-2d" por Benjah-BMM27-Trabajo propio (dominio público) a través de Commons Wikimedia
2. "Perclorato-2d-dimensiones" por Benjah-BMM27-Trabajo propio (dominio público) a través de Commons Wikimedia


