Diferencia entre cloro y cloramina

El diferencia clave entre el cloro y la cloramina es que El cloro es un compuesto gaseoso que consta de dos átomos de cloro por molécula, mientras que la cloramina es una clase de compuestos gaseosos que consisten en moléculas de amoníaco con sustituciones de cloro.
El gas de cloro tiene el Fórmula química CL2. La fórmula química de la cloramina varía con la sustitución del cloro; Uno, dos o los tres átomos de hidrógeno de amoníaco se pueden sustituir con átomos de cloro.

CONTENIDO
1. Descripción general y diferencia de claves
2. Que es el cloro
3. Que es la cloramina
4. Comparación lado a lado: cloro vs cloramina en forma tabular
5. Resumen
Que es el cloro?
El cloro es un compuesto gaseoso que tiene un color amarillo verde y un olor irritante. En términos químicos, se refiere al elemento químico que tiene el número atómico 17. Se encuentra entre los halógenos de la tabla periódica de elementos (los elementos del grupo 7 se denominan halógenos). Pero en términos generales, el término cloro se refiere al gas de cloro.
El gas de cloro es un agente oxidante fuerte. La masa molar de este gas es de 70 g/mol y la fórmula química es CL2. Por lo tanto, es un gas diatómico. Este gas se usa comúnmente como desinfectante y agente de limpieza. Y también, es un potente irritante para los ojos y los pulmones. La inhalación del gas de cloro es tóxica. Este gas es ligeramente soluble en agua y el gas se puede licuar fácilmente aplicando presión (a temperatura ambiente).

Figura 01: Gas de cloro en una botella
El gas de cloro no es inflamable, pero puede soportar la quema (como lo hace el gas oxígeno). El vapor de este gas es más pesado que el aire normal. Por lo tanto, si este gas está en un recipiente con aire normal, permanece en la parte inferior del contenedor (se hunde hacia el fondo ya que es relativamente pesado). El gas de cloro se puede usar para purificar el agua en piscinas y spa. Además, puede blanquear la pulpa de madera. Además, este gas se usa para hacer otros productos químicos que contienen cloro.
Que es la cloramina?
La cloramina es un compuesto gaseoso que tiene el Fórmula química NH2CL. Este compuesto pertenece a una clase de compuestos que tiene uno, dos o los tres átomos de hidrógeno de una molécula de amoníaco sustituido con átomos de cloro (monocloramina cloramina, NH2Cl, dicloramina NHCL2, y tricloruro de nitrógeno NCL3). Allí, el término monocloramina se refiere al término general "cloramina".
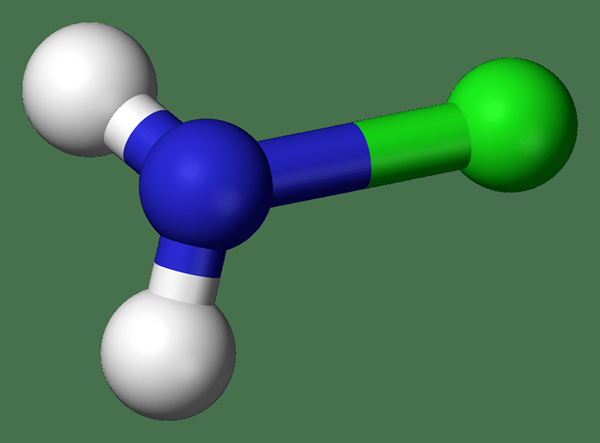
Figura 02: Estructura de cloramina (azul - nitrógeno, hidrógeno blanco, verde - cloro)
La masa molar de este gas es 51.47 g/mol. Es un gas incoloro. El punto de fusión de la cloramina es -66 ° CAT que, este gas se convierte en un estado líquido inestable. Sin embargo, el manejo de este compuesto es como una solución acuosa diluida; Por lo tanto, a veces puede actuar como un desinfectante. Dado que el estado líquido es muy inestable, es difícil medir el punto de ebullición de la cloramina. Es útil en desinfección del agua. Además, es favorable que el gas de cloro porque es menos agresivo y más estable contra la luz.
¿Cuál es la diferencia entre cloro y cloramina??
Cloro vs cloramina | |
| El cloro es un compuesto gaseoso que tiene un color amarillo verde y un olor irritante. | La cloramina es un compuesto gaseoso que tiene la fórmula química NH2CL. |
| Color | |
| El gas tiene un color amarillo verdoso. | Es un gas incoloro. |
| Fórmula química | |
| CL2 | NUEVA HAMPSHIRE2CL |
| Masa molar | |
| 70 g/mol | 51.47 g/mol |
| Toxicidad | |
| Un gas tóxico | Relativamente menos tóxico |
Resumen -Cloro vs cloramina
El cloro y la cloramina son gases que esencialmente tienen átomos de cloro en su estructura química. La diferencia entre el cloro y la cloramina es que el cloro es un compuesto gaseoso que consta de dos átomos de cloro por molécula, mientras que la cloramina es una clase de compuestos gaseosos que consisten en moléculas de amoníaco con sustituciones de cloro.
Referencia:
1. "CLORINE - Información de elementos, propiedades y usos | Tabla periódica."Royal Society of Chemistry - Avance de excelencia en las ciencias químicas. Disponible aquí
2. "Cloro."Centro Nacional de Información de Biotecnología. Base de datos de compuestos de pubChem, u.S. Biblioteca Nacional de Medicina. Disponible aquí
3. "Cloramina."Wikipedia, Fundación Wikimedia, 10 de mayo de 2018. Disponible aquí
Imagen de cortesía:
1.'Cloro en botella' por w. Oelen (CC BY-SA 3.0) a través de Commons Wikimedia
2.'Balls de cloramina-3D' por Jynto y Ben Mills (dominio público) a través de Commons Wikimedia


