Diferencia entre cromado y dicromato

El diferencia clave entre el cromato y el dicromato es que El cromato aparece en un color amarillo brillante, mientras que el dicromato aparece en un color naranja brillante.
El cromato y el dicromato son aniones que contienen átomos de cromo y oxígeno. Por lo tanto, son oxianiones de cromo. A menudo usamos estos términos como términos generales para nombrar los compuestos que contienen estos aniones. Estos dos aniones tienen estructuras químicas muy similares; El cromato tiene un anión cromato, mientras que el dicromato tiene dos aniones de cromato en combinación entre sí. Pero tienen diferentes apariciones.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es el cromado
3. Que es dicromato
4. Comparación de lado a lado: cromato vs dicromato en forma tabular
5. Resumen
Que es el cromado?
El cromato es un oxianión de cromo que tiene la fórmula química Cro42-. En general, usamos este término para nombrar los compuestos que contienen este anión colectivamente como un grupo, yo.mi. Los compuestos que contienen el anión cromato se nombran como cromatos. Por lo general, los cromatos tienen un color amarillo brillante. El átomo de cromo en este anión está en un estado de oxidación de +6. Es un agente oxidante moderadamente fuerte. La masa molar de este anión es 115.99 g/mol.
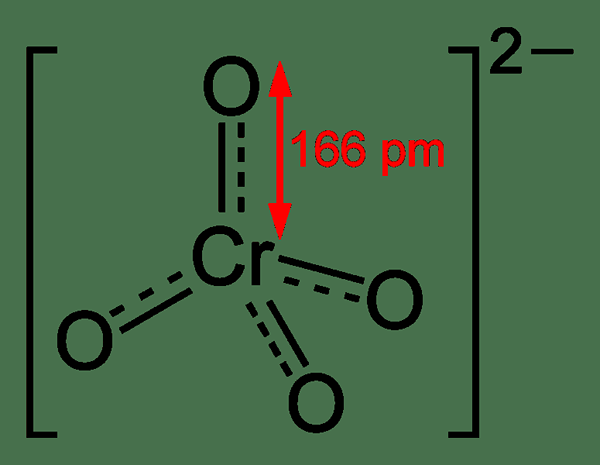
Figura 01: Estructura química del ion cromato
Al considerar las propiedades y reacciones de los cromatos, pueden reaccionar con peróxido de hidrógeno ya que el anión de peróxido reemplaza uno o más átomos de oxígeno. En una solución acuosa, generalmente hay un equilibrio entre el cromato y el dicromato. Sin embargo, podemos encontrar una gran cantidad de cromato a altos valores de pH (superiores a 6.5 ph) donde la cantidad de dicromato es muy pequeña. Esto significa que, en las soluciones alcalinas, la especie predominante es cromato.
Que es dicromato?
El dicromato es una oxianión de cromo que tiene la fórmula química CR2O72-. Por lo general, usamos este término para nombrar los compuestos que contienen este anión colectivamente como un grupo. Delantero.gramo., Dicromato de potasio, el dicromato de sodio son dicromatos. Además, los compuestos que contienen dicromato como anion muestran un color naranja brillante. La masa molar de este anión es 215.99 g/mol. Al considerar la geometría del dicromato, tiene geometría tetraédrica alrededor del átomo de cromo.

Figura 02: Apariencia de compuestos de dicromato
En una solución acuosa, normalmente hay un equilibrio entre el cromato y el dicromato. Sin embargo, podemos encontrar una gran cantidad de dicromato y una cantidad muy pequeña de cromato a valores de pH bajos (inferiores a 6.5 pH).
¿Cuál es la diferencia entre cromato y dicromato??
El cromato y el dicromato son aniones que contienen átomos de cromo y oxígeno. Por lo tanto, son oxianiones de cromo. La diferencia clave entre el cromato y el dicromato es que el cromato aparece en un color amarillo brillante, mientras que el dicromato aparece en un color naranja brillante. Además, el ion cromato tiene un átomo de cromo por anión, mientras que el ion dicromato tiene dos átomos de cromo por anión.
Además, una mayor diferencia entre el cromato y el dicromato está en su masa molar. La masa molar del anión dicromato es 215.99 g/mol, mientras que la masa molar de anión cromato es 115.99 g/mol. En una solución acuosa, normalmente hay un equilibrio entre el cromato y el dicromato. Sin embargo, podemos encontrar una gran cantidad de cromato a altos valores de pH (superiores a 6.5 ph) donde la cantidad de dicromato es muy pequeña. Pero a valores de pH bajos (inferiores a 6.5 ph), hay más iones dicromados.

Resumen -Cromato vs Dicromato
El cromato y el dicromato son aniones que contienen átomos de cromo y oxígeno. Por lo tanto, son oxianiones de cromo. La diferencia clave entre el cromato y el dicromato es que el cromato aparece en un color amarillo brillante, mientras que el dicromato aparece en un color naranja brillante. En una solución acuosa, normalmente hay un equilibrio entre el cromato y el dicromato. Sin embargo, podemos encontrar una gran cantidad de cromato a altos valores de pH (superiores a 6.5 pH), mientras que en valores de pH bajos (inferiores a 6.5 ph), hay más iones dicromados.
Referencia:
1."Dicromato."Centro Nacional de Información de Biotecnología. Base de datos de compuestos de pubChem, u.S. Biblioteca Nacional de Medicina, disponible aquí.
2."Dicromato de potasio."Wikipedia, Fundación Wikimedia, 9 de noviembre. 2019, disponible aquí.
3. Cheremisinoff, Paul N. "Tratamiento del ejemplo de la industria de fertilizantes de efluentes."Minimización de residuos y reducción de costos para las industrias de procesos, 1995, PP. 285-324., doi: 10.1016/b978-081551388-9.50010-5.
Imagen de cortesía:
1. "Chromate-2D-Dimensions" por Ben Mills-Trabajo propio (dominio público) a través de Commons Wikimedia
2. "Potasio-dicromato-muestra" de Benjah-BMM27-Trabajo propio (dominio público) a través de Commons Wikimedia


