Diferencia entre los colores producidos por los metales alcalinos y el calcio

El diferencia clave Entre los colores producidos por los metales alcalinos y el calcio es que el El calcio produce un color de llama de color rojo naranja característica que cualquiera de los metales alcalinos no puede producir.
La prueba de llama es una técnica de análisis cualitativo en la que podemos tener una idea para identificar un cierto elemento químico al observar el color de la llama que da cuando quemamos ese elemento; principalmente metales. Sin embargo, no podemos usar esta técnica analítica para identificar todos los metales que conocemos porque algunos metales no producen un color de llama y algunos metales tienen colores de llama en común.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Cuáles son los colores producidos por Alkali Metals?
3. ¿Qué son los colores producidos por el calcio?
4. Comparación lado a lado: colores producidos por Alkali Metals vs Calcium en forma tabular
6. Resumen
¿Cuáles son los colores producidos por Alkali Metals??
Los colores producidos por los metales alcalinos varían según el metal. Los metales alcalinos son los elementos químicos del Grupo 1. Los miembros de este grupo son litio, sodio, potasio, rubidio y cesio. Para estos metales del Grupo 1, la prueba de llama es la forma más fácil de identificar el metal porque dan colores, que son diferentes entre sí. Ahora consideremos el método para realizar una prueba de llama.
- Limpiar un alambre de platino sumergiéndolo en ácido HCl concentrado.
- Luego sosténgalo en una llama de Bunsen caliente.
- Deberíamos repetir los dos pasos anteriores hasta que el cable de platino no muestre color de llama.
- Luego humedezca el cable nuevamente en ácido y sumérjalo en la muestra del metal que vamos a probar.
- A continuación, sostenga el cable junto con la muestra en un quemador de Bunsen caliente. Esto muestra un color diferente que es el color de la llama del metal de muestra

Figura 01: El color de la llama del rubidio
Cuando sostenemos el metal de muestra en la llama, la energía térmica de la llama hace que los electrones del metal salten de un nivel de energía a un nivel de energía más alto. Llamamos a esto "excitación de electrones". Sin embargo, esta excitación es muy inestable. Por lo tanto, el electrón inmediatamente regresa a donde estaba, liberando energía como luz visible. Reconocemos esto como el color de la llama. Además, el color dado por átomos más grandes a menudo tiene una baja intensidad que el de los átomos pequeños. Los colores de la llama producidos por Alkali Metals son los siguientes:
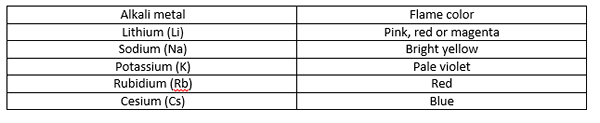
¿Cuáles son los colores producidos por el calcio??
La prueba de llama para el calcio proporciona un color característico de color rojo naranja, que cualquier otro metal no puede producir.

Figura 02: Color de la llama del calcio
Aunque el rubidio en el grupo de metal alcalino también produce un color rojo, es distinto del color del calcio principalmente debido a la diferencia en los tamaños de los dos átomos (el rubidio tiene una cubierta de electrones adicional que el átomo de calcio; por lo tanto, las excitaciones de electrones son diferentes de entre sí. Esto da como resultado diferentes colores de llama).
¿Cuál es la diferencia entre los colores producidos por los metales alcalinos y el calcio??
Los metales alcalinos producen diferentes colores de llama que facilitan identificar un metal alcalino de otro. Por ejemplo, litio - color magenta, sodio - amarillo brillante, potasio - violeta pálida, rubidio - rojo y cesio - azul. Sin embargo, el color de la llama producido por el calcio es diferente de todos estos colores; Produce un color rojo naranja, que es un color de llama característico de calcio solo (ningún otro metal da el mismo color). Esta es la diferencia entre los colores producidos por los metales alcalinos y el calcio.

Resumen: colores producidos por Alkali Metals vs Calcium
Diferentes metales producen diferentes colores de llama cuando los quemamos. El color producido por el calcio es característico para el calcio; Por lo tanto, podemos distinguirlo de los colores de la llama dados por Alkali Metals. La diferencia entre los colores producidos por los metales alcalinos y el calcio es que el calcio produce un color de llamas de color rojo naranja característico que cualquiera de los metales alcalinos no puede producir.
Referencia:
1. Helmenstine, Anne Marie. "Cómo se producen los colores de las pruebas de llamas."THEWLECO, THIENTOCO. Disponible aquí
2. Bibliotecas. "Pruebas de llama."Bibliotecas de química, Librettexts, 17 de febrero. 2018. Disponible aquí
Imagen de cortesía:
1."Die Flammenfärbung des Rubidium" de Didaktische.Medien - Trabajo propio, (CC By -SA 3.0) a través de Commons Wikimedia
2."356886434" por Tjmwatson (CC por 2.0) a través de Flickr


