Diferencia entre CUSO4 y CUSO4 5H2O

El diferencia clave entre CUSO4 y CUSO4 5H2O es que CUSO4 es amorfo, mientras que CUSO4 5H2O es cristalino.
CUSO4 es la fórmula química del sulfato de cobre (II), mientras que CUSO4 5H2O es la forma hidratada de cobre (ii) sulfato. El término hidratado indica que este compuesto tiene una o más moléculas de agua en asociación con él. Por lo tanto, CUSO4 es el nombre habitual de la forma anhidra.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es CUSO4?
3. ¿Qué es CUSO4 5H2O?
4. Comparación de lado a lado - CUSO4 vs CUSO4 5H2O en forma tabular
5. Resumen
¿Qué es CUSO4??
CUSO4 es sulfato de cobre (II) que tiene el metal de cobre en estado de oxidación +2. Es un compuesto inorgánico que no tiene moléculas de agua asociadas con él. Por lo tanto, lo llamamos la forma anhidra de sulfato de cobre. Además, este compuesto anhidro ocurre como un polvo blanco.
La producción industrial de sulfato de cobre implica tratar el metal de cobre con ácido sulfúrico en forma caliente y concentrada. Además, es posible producir este compuesto usando óxidos de cobre también. Aquí, se realiza tratando el óxido de cobre con ácido sulfúrico diluido. Además, la lixiviación lentamente del mineral de cobre de bajo grado en el aire es otro método de producción. Es posible usar bacterias para catalizar este proceso.

Figura 02: sulfato de cobre anhidro
Al considerar las propiedades químicas de este compuesto, la masa molar es 159.6 g/mol. Aparece en color blanco gris. La densidad es 3.60 g/cm3. Al considerar el punto de fusión del sulfato de cobre, es de 110 ° C, y al calentarse aún más, el compuesto se descompone.
¿Qué es CUSO4 5H2O??
CUSO4 5H2O es pentahidrato de sulfato de cobre (ii). Tiene cinco moléculas de agua asociadas con la molécula de sulfato de cobre. Aparece como un color azul brillante sólido. Además, es la forma hidratada más común de sulfato de cobre. Además, algunos nombres comunes para este compuesto son vitriolo azul, azul, vitriolo de cobre, vitriolo romano, etc.

Figura 02: Apariencia de pentahidrato de sulfato de cobre
Además, este compuesto se disuelve exotérmicamente en agua. Luego, forma un complejo Aqua que contiene una molécula CUSO4 en asociación con seis moléculas de agua, y este complejo tiene una geometría molecular octaédrica. La masa molar es 249.65 g/mol. Al considerar el punto de fusión, al calentarse por encima de 560 ° C, el compuesto se descompone. Eso significa; el compuesto se descompone antes de derretirse. Allí, este compuesto elimina dos moléculas de agua a 63 ° C y dos más a 109 ° C. Además, la molécula de agua final se libera a 200 ° C.
¿Cuál es la diferencia entre CUSO4 y CUSO4 5H2O??
CUSO4 es sulfato de cobre (II) que tiene el metal de cobre en estado de oxidación +2. CUSO4 5H2O es pentahidrato de sulfato de cobre (ii). La diferencia clave entre CUSO4 y CUSO4 5H2O es que CUSO4 es amorfo, mientras que CUSO4 5H2O es cristalino. Además, el sulfato de cobre es anhidro, mientras que el pentahidrato de sulfato de cobre es una forma hidratada.
Además, una diferencia adicional entre CUSO4 y CUSO4 5H2O es su punto de fusión; El punto de fusión de CUSO4 es de 110 ° C, y al calentamiento adicional, el compuesto se descompone, mientras que el compuesto CUSO4 5H2O se descompone antes de derretirse.
A continuación, la infografía muestra más información sobre la diferencia entre CUSO4 y CUSO4 5H2O.
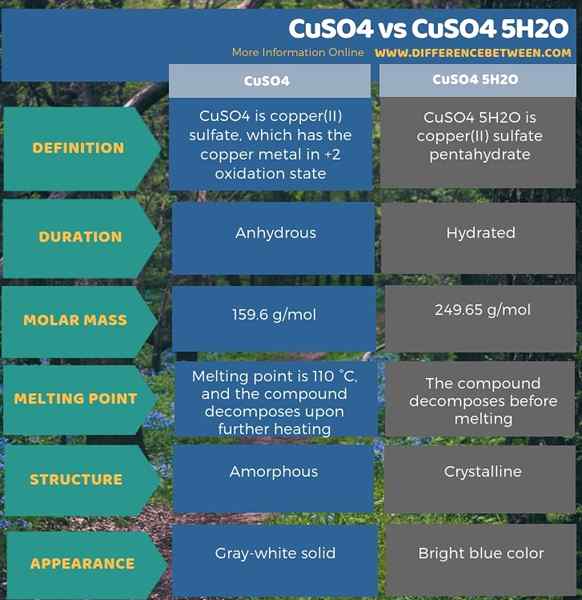
Resumen -CUSO4 vs CUSO4 5H2O
CUSO4 es sulfato de cobre (II) que tiene el metal de cobre en estado de oxidación +2. CUSO4 5H2O es pentahidrato de sulfato de cobre (ii). En resumen, la diferencia clave entre CUSO4 y CUSO4 5H2O es que CUSO4 es amorfo, mientras que CUSO4 5H2O es cristalino.
Referencia:
1. "Pentahidrato de sulfato de cobre."Centro Nacional de Información de Biotecnología. Base de datos de compuestos de pubChem, u.S. Biblioteca Nacional de Medicina, disponible aquí.
Imagen de cortesía:
1. "Sulfato de cobre" por Stephanb - Trabajo propio, (CC By -SA 3.0) a través de Commons Wikimedia
2. "Sulfato de cobre anhidro" por W. Oelen - (CC BY -SA 3.0) a través de Commons Wikimedia


