Diferencia entre la ley de tasa diferencial y la ley de tasas integradas
Diferencia clave: ley de tasas diferenciales versus ley de tasas integradas
La ley de tasas diferenciales y la ley de tasas integradas son dos formas de leyes de tasas. La diferencia clave entre la ley de tasa diferencial y la ley de tasas integradas es que La ley de velocidad diferencial da la velocidad de una reacción química en función del cambio en la concentración de uno o más reactivos durante un período de tiempo particular, mientras que la ley de velocidad integrada da la velocidad de una reacción química en función de la concentración inicial de uno o más reactivos después de un período específico de tiempo.
La velocidad de reacción es la medida del cambio de concentración de reactivos o productos durante la progresión de una reacción química. Se utilizan diferentes leyes de tasa para explicar el progreso de la reacción. Estas leyes de tasas se expresan como relaciones matemáticas entre diferentes parámetros.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la ley de tasa diferencial?
3. ¿Qué es la ley de tarifas integrada?
4. Relación entre la ley de tasas diferenciales y la ley de tasas integradas
5. Comparación de lado a lado - Ley de tasa diferencial frente a la ley de tasa integrada en forma tabular
6. Resumen
¿Qué es la ley de tasa diferencial??
La ley de velocidad diferencial se utiliza para determinar la velocidad de una reacción química en función del cambio en la concentración de uno o más reactivos durante un período de tiempo particular. La ley de velocidad diferencial indica lo que está sucediendo a nivel molecular de una reacción química. El mecanismo general de una reacción química se puede determinar utilizando leyes de velocidad diferencial (conversión de reactivos en productos).
Ecuación de ley de tasa diferencial
La ley de tasa diferencial para la reacción química a continuación se puede dar como una expresión matemática.
A → B + C
Tasa = - d [a] / dt = k [a]norte
Aquí, [a] es la concentración del reactivo "A" y "K" es la velocidad constante. "N" da el orden de reacción. La ecuación de ley de tasa diferencial puede integrarse para obtener una relación clara entre [a] y el tiempo "t". Esta integración proporciona la ley de tarifas integrada.

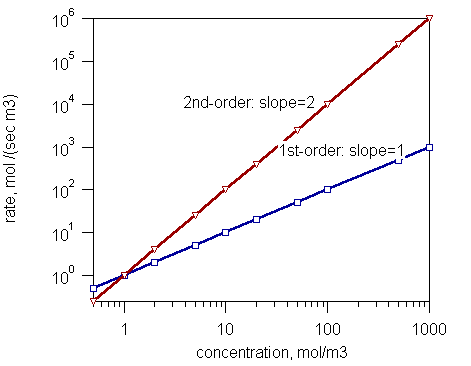
Figura 1: Un gráfico que muestra el orden de reacción
¿Qué es la ley de tarifas integrada??
La ley de velocidad integrada da la velocidad de una reacción química en función de la concentración inicial de uno o más reactivos después de un período de tiempo específico. La ley de velocidad integrada se puede utilizar para determinar la constante de velocidad de una reacción química particular, y el orden de reacción se puede obtener a través de datos experimentales.
Ecuación de ley de tasas integradas
Para la reacción química A → B + C, la ley de velocidad integrada se puede expresar como una expresión matemática como se da a continuación.
ln [a] = -kt + ln [a]0
Aquí un]0 es la concentración inicial del reactante A y [a] es la concentración del reactivo "A" después de que haya pasado el tiempo "T". Sin embargo, las leyes de tasa integradas son diferentes entre sí en función del orden de la reacción "n". La ecuación anterior se da para reacciones químicas de orden cero.
Para Reacciones de primer orden, La ecuación de la ley de tasas es,
[A] = [a] e-kt
Para Reacciones de segundo orden, La ecuación de la ley de tasas es,
1/[a] = 1/[a]0 + kt
Para determinar el velocidad constante de una reacción, Las ecuaciones anteriores se pueden usar de la siguiente manera.
Para reacciones de primer orden,
k = ln [a] - ln [a]0 / t
Para reacciones de segundo orden,
k = 1/[a] - 1/[a]0 / t
¿Cuál es la relación entre la ley de tasas diferenciales y la ley de tasas integradas??
- La ley de velocidad diferencial de una reacción química se puede integrar para obtener la ley de velocidad integrada de la misma reacción química.
¿Cuál es la diferencia entre la ley de tasa diferencial y la ley de tasas integradas??
Ley de tasas diferenciales frente a la ley de tarifas integradas | |
| La ley de velocidad diferencial se utiliza para determinar la velocidad de una reacción química en función del cambio en la concentración de uno o más reactivos durante un período de tiempo particular. | La ley de velocidad integrada da la velocidad de una reacción química en función de la concentración inicial (o la concentración en un momento particular) de uno o más reactivos después de un período de tiempo específico. |
| Solicitud | |
| La ley de velocidad diferencial se puede utilizar para indicar lo que está sucediendo a nivel molecular de una reacción química y, el mecanismo general de una reacción química se puede determinar utilizando esta ley de velocidad. | La ley de velocidad integrada se puede utilizar para determinar la constante de velocidad de una reacción química particular. |
| Uso | |
| La ley de tasa diferencial es difícil de usar en comparación con la ley de tasas integradas. | La ley integrada facilita la determinación de la clara relación entre la concentración de reactivos y el tiempo transcurrido. |
Resumen -Ley de tasas diferenciales frente a la ley de tarifas integradas
La ley de la velocidad de una reacción química da la relación entre la velocidad de reacción y las concentraciones de reactivos. La diferencia clave entre la ley de tasa diferencial y la ley de tasa integrada es que la ley de tasa diferencial da la velocidad de una reacción química en función del cambio en la concentración de uno o más reactivos durante un período de tiempo particular, mientras que la ley de tasa integrada da la tasa de Una reacción química en función de la concentración inicial de uno o más reactivos después de un período específico de tiempo.
Referencia:
1. "Leyes de tarifas - diferencial."Bibliotecas de química, Librettexts, 17 de julio de 2015, disponible aquí.
2. Bibliotecas. "12.4: Leyes de tarifas integradas."Bibliotecas de química, Librettexts, 11 de septiembre. 2017, disponible aquí.]
Imagen de cortesía:
1. "Rateloglogplot" de Fabiuccio ~ enwikibooks en English Wikibooks - Transferido desde EN.wikibooks a los comunes.(Dominio público) a través de Commons Wikimedia


