Diferencia entre electropositivo y electronegativo
El diferencia clave entre electropositivo y electronegativo es que Electropositivo se refiere a la capacidad de perder electrones, formando cationes, mientras que el electronegativo se refiere a la capacidad de ganar electrones, formando aniones.
Los términos electropositivos y electronegativos vienen con la atracción o repulsión de elementos químicos hacia los electrones. Podemos clasificar los elementos químicos de acuerdo con esta característica; O pierden o ganan electrones durante una reacción química.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es electropositivo?
3. ¿Qué es electronegativo?
4. Comparación de lado a lado: electropositivo frente a electronegativo en forma tabular
5. Resumen
¿Qué es electropositivo??
Electropositivo significa que los elementos químicos tienden a perder electrones. La pérdida de electrones forma cationes o iones cargados positivamente en reacciones químicas. Es una medida de la capacidad de un elemento para donar electrones. Los elementos tienden a perder sus electrones para obtener una configuración de electrones de gas noble.
Por lo general, todos los metales se consideran elementos químicos electropositivos porque tienen electrones fácilmente removibles en sus orbitales más externos. Entre ellos, los metales alcalinos (elementos químicos del grupo 1) son los elementos más electropositivos. Teóricamente, Francium es el elemento químico más electropositivo, aunque es de naturaleza inestable. Aunque el hidrógeno está en el grupo 1 de la tabla periódica, puede perder o ganar electrones; Por lo tanto, podemos clasificarlo en elementos electropositivos y electronegativos.
¿Qué es electronegativo??
Electronegativo se refiere a la capacidad de un elemento químico para obtener electrones. La obtención de electrones desde el exterior forma aniones; Los aniones son las especies químicas cargadas negativamente. La electronegatividad es lo opuesto a la electropositividad. El símbolo de este fenómeno es χ. El término puede referirse a la atracción de un par de electrones compartidos o una densidad de electrones hacia sí mismo. Hay dos factores principales que afectan la electronegatividad de un elemento químico: número atómico y distancia entre el núcleo y los electrones de valencia.

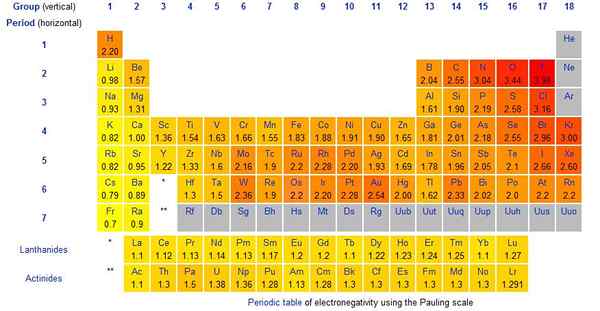
Figura 01: Valores de escala de Pauling para elementos químicos
La escala Pauling es el método que utilizamos para dar un valor a la electronegatividad de un elemento químico. La escala fue propuesta por Linus Pauling. Es una cantidad adimensional. Además, es una escala relativa que considera que la electronegatividad varía de 0.79 a 3.98. La electronegatividad del hidrógeno es 2.20. El elemento más electronegativo es el fluorino, y su valor de escala pauling es 3.98 (generalmente lo tomamos como 4). Por lo general, todos los halógenos (elementos del grupo 7) son altamente electronegativos.
¿Cuál es la diferencia entre electropositivo y electronegativo??
La diferencia clave entre electropositivo y electronegativo es que el término electropositivo se refiere a la capacidad de perder electrones, formando cationes, mientras que el electronegativo se refiere a la capacidad de ganar electrones, formando anions. Además, al considerar los elementos químicos en la parte superior de la lista, en la lista de elementos electropositivos, el elemento más electropositivo es Francium, mientras que entre los elementos electronegativos, el elemento más electronegativo es Fluorine.
La escala Pauling es la escala que usamos para dar un valor a cada elemento electropositivo y electronegativo. Sin embargo, esta escala da la electronegatividad de un elemento; Por lo tanto, podemos determinar que un valor de electronegatividad muy bajo indica que el elemento es más electropositivo.
Debajo de la infografía resume la diferencia entre electropositivo y electronegativo.

Resumen -electropositivo frente a electronegativo
Los términos electropositivos y electronegativos describen la atracción o repulsión de elementos químicos hacia los electrones. La diferencia clave entre electropositivo y electronegativo es que el término electropositivo se refiere a la capacidad de perder electrones formando cationes, mientras que el electronegativo se refiere a la capacidad de obtener electrones que forman aniones.
La escala Pauling es la escala que usamos para dar un valor a cada elemento electropositivo y electronegativo. La escala da la electronegatividad de un elemento; Por lo tanto, podemos determinar que un valor de electronegatividad muy bajo indica que el elemento es más electropositivo.
Referencia:
1."Electronegatividad."Wikipedia, Fundación Wikimedia, 13 de septiembre. 2019, disponible aquí.
2. "¿Por qué los metales llamaron elementos electropositivos ynosb3ss -quemistry."Topperlearning, disponible aquí.
Imagen de cortesía:
1. "Electronegativo" de AdBlocker - Trabajo propio, (CC BY -SA 3.0) a través de Commons Wikimedia


