Diferencia entre los radicales electropositivos y electronegativos
El diferencia clave entre los radicales electropositivos y electronegativos es que Los radicales electropositivos son compuestos radicales que tienen la capacidad de perder electrones y transportar una carga positiva, mientras que los radicales electronegativos son compuestos radicales que tienen la capacidad de obtener electrones y transportar una carga negativa.
Un radical, en química, es un átomo, una molécula o un ion que contiene un electrón de valencia no apareado. En la mayoría de los casos, este electrón no apartado hace que un compuesto químico sea altamente reactivo porque este electrón tiende a emparejar con otro electrón para obtener un nivel de energía bajo. Además, un átomo, ión o molécula que tiene una cubierta de electrones abierta que puede obtener electrones también se clasifica como radical en química. Debido a la naturaleza altamente reactiva, estos radicales a menudo tienden a sufrir reacciones de dimerización y polimerización.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué son los radicales electropositivos?
3. ¿Qué son los radicales electronegativos?
4. Comparación lado a lado: radicales electropositivos frente a electronegativos en forma tabular
5. Resumen
¿Qué son los radicales electropositivos??
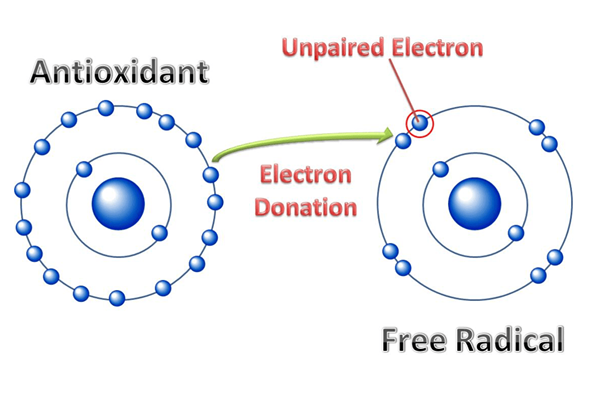
Los radicales electropositivos son átomos, iones o moléculas que pueden perder un electrón y transportar una carga eléctrica positiva. Se forma un radical electropositivo debido a la naturaleza electropositiva de una especie química, lo que significa que una especie química particular tiene la tendencia a perder electrones para formar radicales positivos. Además, algunos ejemplos de radicales electropositivos incluyen catión de calcio (CA+2), catión de sodio (na+), etc.

Figura 01: Formación de un radical
¿Qué son los radicales electronegativos??
Los radicales electronegativos son átomos, iones o moléculas que pueden ganar un electrón y transportar una carga eléctrica negativa. Se forma un radical electronegativo debido a la alta electronegatividad de una especie química, lo que significa que una especie química particular tiene la tendencia a ganar electrones y formar radicales cargados negativamente.
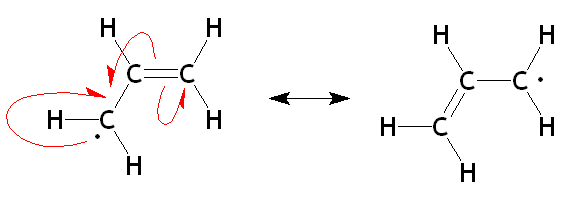
Figura 02: Resonancia en radicales
Además, algunos ejemplos de radicales electronegativos incluyen anión cloro (CL-), Anión fluoruro (F-), etc.
¿Cuál es la diferencia entre los radicales electropositivos y electronegativos??
Los radicales son especies químicas como átomos, iones o moléculas que tienen un electrón no apareado. La diferencia clave entre los radicales electropositivos y electronegativos es que los radicales electropositivos son compuestos radicales que tienen la capacidad de los electrones y transportan una carga positiva, mientras que los radicales electronegativos son compuestos radicales que tienen capacidad para obtener electrones y transportan una carga negativa. Por lo tanto, los radicales electropositivos transportan una carga positiva, mientras que los radicales electronegativos tienen una carga negativa. Algunos ejemplos de radicales electropositivos incluyen catión de calcio y catión de sodio, mientras que los ejemplos de radicales electronegativos incluyen iones de fluoruro y cloruro.
La siguiente tabla resume la diferencia entre los radicales electropositivos y electronegativos.

Resumen -Radicales electropositivos vs electronegativos
Un radical, en química, es un átomo, una molécula o un ion que contiene un electrón de valencia no apareado. La diferencia clave entre los radicales electropositivos y electronegativos es que los radicales electropositivos son compuestos radicales que tienen la capacidad de perder electrones y transportar una carga positiva, mientras que los radicales electronegativos son compuestos radicales que tienen capacidad para obtener electrones y transportar una carga negativa. La mayoría de las veces, los radicales son especies químicas altamente reactivas, lo que hace que se sometan a reacciones de dimerización y polimerización.
Referencia:
1. Más, Hemant. "Nomentar los compuestos químicos: radicales, iones, ácidos, bases, sales, etc." El factor de hecho, 5 de junio de 2020, disponible aquí.
2. "Electronegatividad." Wikipedia, Fundación Wikimedia, 24 de octubre. 2020, disponible aquí.
3. "¿Qué es la electropositiva?? Definición, tendencias, comparación con electronegatividad."Byjus, Byju's, 17 de agosto. 2020, disponible aquí.
Imagen de cortesía:
1. “Antioxidantes Radicales libres Lobo et al.,"Por Lobo, V., Patil, un., Phatak, un., & Chandra, N - Lobo, V., Patil, un., Phatak, un., & Chandra, N. (2010). Radicales libres, antioxidantes y alimentos funcionales: impacto en la salud humana. Pharmacognosy Reviews, 4 (8), 118-126. (CC BY-SA 4.0) a través de Commons Wikimedia
2. "Allyl Radical Resonance" por Orgonaute - Trabajo propio (CC BY -SA 3.0) a través de Commons Wikimedia


