Diferencia entre elemento y molécula
El diferencia clave entre el elemento y la molécula es que Los elementos son sustancias puras que consisten en un solo tipo de átomo, y no pueden descomponerse por medios químicos, mientras que las moléculas pueden contener dos o más átomos del mismo elemento o diferentes elementos.
Los átomos son las unidades pequeñas que se acumulan para formar todas las sustancias químicas existentes. Los átomos pueden unirse a otros átomos de varias maneras y formar miles de moléculas y otros compuestos. De acuerdo con sus habilidades de donación o retirada de electrones, pueden formar enlaces covalentes o enlaces iónicos. A veces hay atracciones muy débiles entre los átomos. Tanto las moléculas como los elementos están formados por átomos.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es un elemento
3. ¿Qué es una molécula?
4. Comparación lado a lado - Elemento vs molécula en forma tabular
5. Resumen
Que es un elemento?
Estamos familiarizados con la palabra "elemento", porque aprendemos sobre ellos en la tabla periódica. Hay alrededor de 118 elementos en la tabla periódica, organizados de acuerdo con su número atómico. Un elemento es una sustancia química que consta de un solo tipo de átomos, por lo tanto, son puros. El elemento más pequeño es el hidrógeno, y la plata, el oro, el platino son algunos de los elementos preciosos comúnmente conocidos. Cada elemento tiene una masa atómica, número atómico, símbolo, configuración electrónica, etc. Aunque la mayoría de los elementos están ocurriendo naturalmente, hay algunos elementos sintéticos como Californium, Americium, Einsteinium y Mendelevium.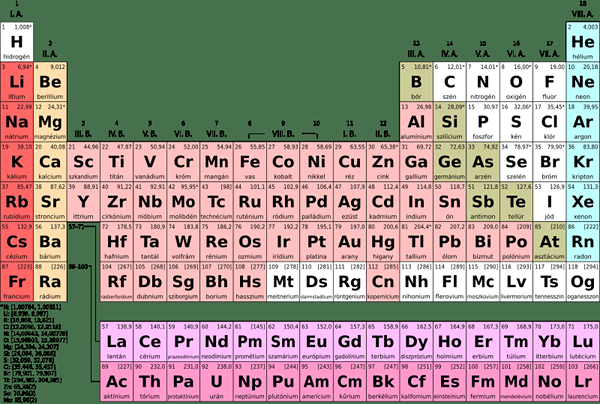
Todos los elementos se pueden clasificar ampliamente en tres categorías: metal, metaloides y no metales. Además, se clasifican en grupos y períodos basados en características más específicas. Los elementos en el mismo grupo o períodos comparten ciertas características comunes, y algunas propiedades pueden cambiar secuencialmente cuando pasa por un grupo o período. Los elementos pueden someterse a cambios químicos para formar varios compuestos; Sin embargo, los elementos no pueden descomponerse aún más por métodos químicos simples. Hay átomos del mismo elemento con un número diferente de neutrones; Estos se conocen como isótopos de un elemento.
¿Qué es una molécula??
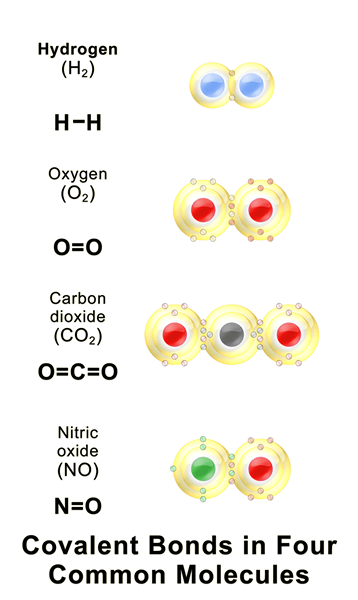
Las moléculas están formadas por unir químicamente dos o más átomos del mismo elemento (E.gramo.: O2, norte2) o elementos diferentes (h2O, NH3). Las moléculas no tienen carga, y los átomos están unidos por los enlaces covalentes. Las moléculas pueden ser muy grandes (hemoglobina) o muy pequeñas (h2), dependiendo del número de átomos que están conectados. El tipo y el número de átomos en una molécula se muestran mediante la fórmula molecular.

La relación entera más simple de los átomos presentes en una molécula viene dada por la fórmula empírica. Por ejemplo, C6H12O6 es la fórmula molecular de glucosa y ch2O es la fórmula empírica. La masa molecular es la masa calculada considerando el número total de átomos dados en la fórmula molecular. Cada molécula tiene su propia geometría. Los átomos en una molécula están dispuestos de la manera más estable con un ángulo de enlace específico y longitudes de enlace para minimizar las repulsiones y las fuerzas de forraje.
¿Cuál es la diferencia entre elemento y molécula??
Los elementos son sustancias puras que consisten en un solo tipo de átomo, y no pueden descomponerse por medios químicos, mientras que las moléculas pueden contener dos o más átomos del mismo elemento o diferentes elementos. Por lo tanto, la diferencia clave entre el elemento y la molécula es que los elementos consisten en un solo tipo de átomos, mientras que las moléculas pueden contener dos o más átomos del mismo elemento o diferentes elementos. Algunos ejemplos de elementos incluyen hidrógeno, nitrógeno, oxígeno, sodio, cobre y zinc, mientras que algunos ejemplos de moléculas incluyen dióxido de carbono, agua y ozono. Además, las propiedades de un elemento a menudo cambian por completo cuando son parte de una molécula.
La siguiente información gráfica muestra las diferencias entre el elemento y la molécula en forma tabular.
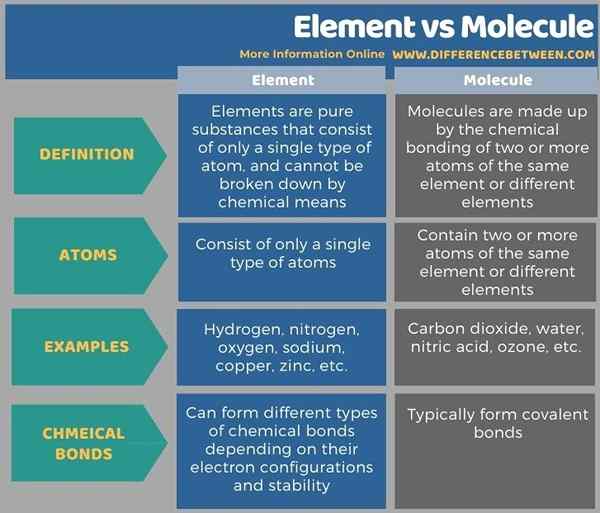
Resumen -Elemento vs molécula
La diferencia clave entre el elemento y la molécula es que los elementos consisten en un solo tipo de átomos, mientras que las moléculas pueden contener dos o más átomos del mismo elemento o elementos diferentes. Las propiedades de un elemento a menudo cambian por completo cuando son parte de una molécula.
Imagen de cortesía:
1. "Table periódica Simple Hu" de László Németh - Trabajo propio, CC0) a través de Commons Wikimedia
2. "Bonos covalentes" de Bruceblaus - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia


