Diferencia entre reacciones endotérmicas y exotérmicas
El diferencia clave entre las reacciones endotérmicas y exotérmicas es que Las reacciones endotérmicas absorben la energía del entorno circundante, mientras que las reacciones exotérmicas liberan energía al entorno circundante.
La energía es la capacidad de trabajar. En un sistema, la energía puede funcionar; Puede cambiar a otras formas como calor, sonido, luz, etc. Cuando la energía de un sistema cambia como resultado de una diferencia de temperatura entre el sistema y los alrededores, decimos que la energía se ha transferido como calor. Una reacción endotérmica es un proceso en el que se adquiere energía desde sus alrededores al sistema, mientras que una reacción exotérmica es un proceso que libera energía desde el sistema hasta el entorno.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué son las reacciones endotérmicas?
3. ¿Cuáles son las reacciones exotérmicas?
4. Comparación de lado a lado: reacciones endotérmicas vs exotérmicas en forma tabular
5. Resumen
¿Qué son las reacciones endotérmicas??
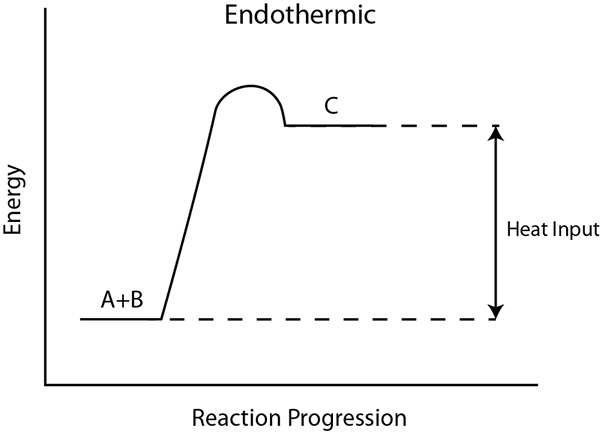
Una reacción endotérmica es un proceso en el que se adquiere energía de sus alrededores, en forma de calor. Si el entorno no suministra calor, la reacción no ocurre. Durante esta reacción, el vaso de reacción se enfría porque absorbe el calor del entorno circundante, bajando así la temperatura.
Para romper un enlace químico, necesita energía. En las reacciones endotérmicas, la energía que rompe el enlace de los reactivos es mayor que la energía de formación de enlaces totales de los productos. Por lo tanto, el cambio de entalpía es un valor positivo, y la reacción no es espontánea. Por lo tanto, para las reacciones endotérmicas, tenemos que suministrar energía desde el exterior.

Por ejemplo, al disolver el cloruro de amonio en el agua, el vaso de precipitados se enfría porque la solución absorbe energía del entorno exterior. La fotosíntesis es una reacción endotérmica que ocupa lugar en el entorno natural. Para la fotosíntesis, la luz solar suministra la energía requerida.
¿Cuáles son las reacciones exotérmicas??
Una reacción exotérmica es un proceso que libera energía a los alrededores, generalmente en forma de calor. Además, la energía también puede liberarse en otras formas, como sonido, luz, etc. Dado que la energía se libera durante la reacción, los productos contienen menos energía que los reactivos. Por lo tanto, el cambio de entalpía (∆H) se vuelve negativo.
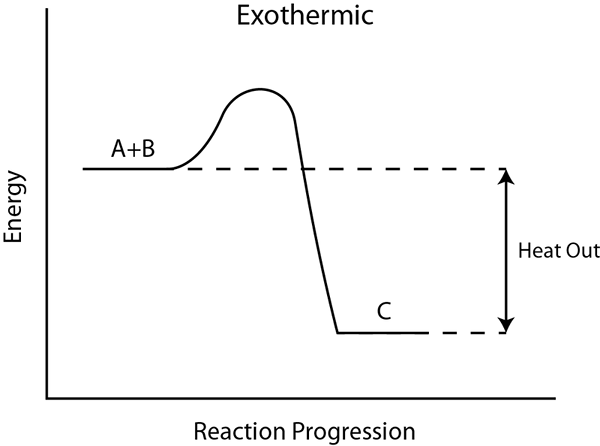
En este tipo de reacción, las liberaciones de energía durante la formación de enlaces. Si la energía de formación de enlaces totales es mayor que la energía de ruptura de enlaces durante la reacción, entonces es exotérmica. Si la energía se libera como calor, la temperatura circundante aumenta, por lo que la reacción a veces puede ser explosiva. Las reacciones exotérmicas son espontáneas. Un suministro de energía externo no es necesario para las reacciones exotérmicas, ya que producen la energía requerida a medida que avanza la reacción. Sin embargo, para comenzar la reacción, puede ser necesario un suministro de energía inicial.
Si podemos capturar esta energía lanzada, podemos usarla para mucho trabajo útil. Por ejemplo, la energía liberada de la combustión de combustibles es útil para operar un vehículo o una máquina. Además, todas las reacciones de combustión son exotérmicas.
¿Cuál es la diferencia entre las reacciones endotérmicas y exotérmicas??
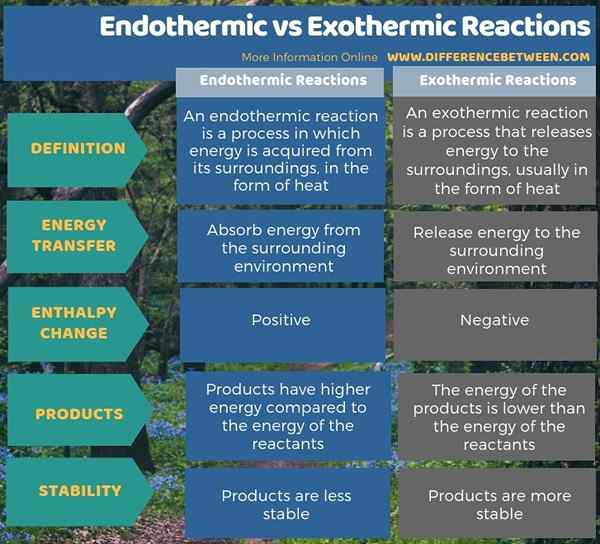
Endotérmico y exotérmico son términos relacionados con la transferencia de calor en los sistemas termodinámicos. La diferencia clave entre las reacciones endotérmicas y exotérmicas es que las reacciones endotérmicas absorben la energía del entorno circundante, mientras que las reacciones exotérmicas liberan energía al entorno circundante. Además, el cambio de entalpía en un proceso endotérmico es positivo, mientras que el cambio de entalpía en un proceso exotérmico es negativo. Al considerar el producto final, el producto de la reacción endotérmica tiene mayor energía en comparación con la energía de los reactivos, mientras que, en reacciones exotérmicas, los productos tienen energía más baja que la energía de los reactivos.
Resumen -Reacciones endotérmicas vs exotérmicas
Endotérmico y exotérmico son términos relacionados con la transferencia de calor en los sistemas termodinámicos. La diferencia clave entre las reacciones endotérmicas y exotérmicas es que las reacciones endotérmicas absorben la energía del entorno circundante, mientras que las reacciones exotérmicas liberan energía al entorno circundante.
Referencia:
Helmenstine, Anne Marie. "Ejemplos de reacción endotérmica."Thoughtco, puede. 9, 2019, disponible aquí.
Imagen de cortesía:
1. "Reacción endotérmica" por BrazoSport College - Trabajo propio (CC By -SA 3.0) a través de Commons Wikimedia
2. "Reacción exotérmica" por BrazoSport College - Trabajo propio (CC By -SA 3.0) a través de Commons Wikimedia


