Diferencia entre esterificación y saponificación
La diferencia clave entre la esterificación y la saponificación es que La esterificación forma un éster, mientras que la saponificación descompone los ésteres en sus materiales de partida.
Se forma un éster a partir de un ácido carboxílico y un alcohol. Por lo tanto, la esterificación es la formación de un éster a partir de un ácido carboxílico y un alcohol. Mientras que la saponificación forma el ácido carboxílico y el alcohol que se utilizan para producir el éster.

CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la esterificación?
3. ¿Qué es la saponificación?
4. Comparación de lado a lado: esterificación vs saponificación en forma tabular
5. Resumen
¿Qué es la esterificación??
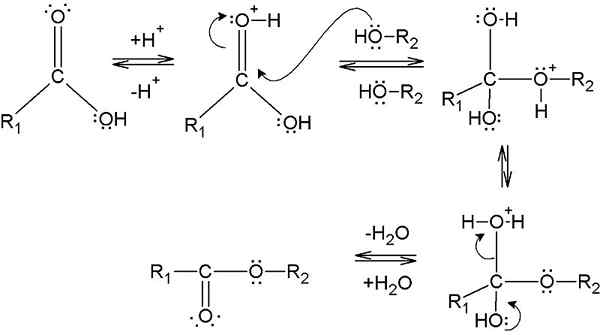
La esterificación es la formación de un éster a partir de la reacción entre un ácido carboxílico y un alcohol. Este proceso requiere un catalizador para reducir la barrera de energía de activación de la reacción. Este catalizador es típicamente un catalizador ácido. Además, la mezcla de reacción debe calentarse porque el proceso de esterificación requiere energía (para escindir el enlace C -OH del ácido carboxílico para eliminar el grupo -OH).

Figura 1: Formación de un éster mediante esterificación
El proceso de esterificación implica la eliminación del grupo hidroxilo (-OH) del ácido carboxílico y el átomo de hidrógeno del grupo hidroxilo del alcohol. Durante este proceso, cuando el grupo -OH se retira del ácido carboxílico, actúa como un electrofilo. Y cuando se elimina el protón del alcohol, actúa como un nucleófilo. Por lo tanto, este nucleófilo ataca el electrofilo formado a partir del ácido carboxílico y forma un éster. Esto da una molécula de agua como subproducto. Por lo tanto, la molécula de agua se forma a partir de la combinación del grupo -OH del ácido carboxílico y el protón del alcohol. Por lo tanto, se puede obtener un éster puro usando un agente deshidratante (para eliminar el agua de la mezcla de reacción).
¿Qué es la saponificación??
La saponificación es el desglose de un éster en un ácido carboxílico y un alcohol. Es lo opuesto a la esterificación. La saponificación ocurre en un medio acuoso en presencia de una base. Las condiciones básicas del medio hacen que el anión carboxilato sea más estable que la forma del ácido carboxílico. Por lo tanto, el ion carboxilato se separa del éster. La saponificación puede ocurrir en ausencia de energía térmica porque no tiene barrera de energía. Aquí, las moléculas de agua en el medio acuoso proporcionan h+ iones, y la base proporciona oh- iones requeridos para la formación de alcohol y ácido carboxílico respectivamente.
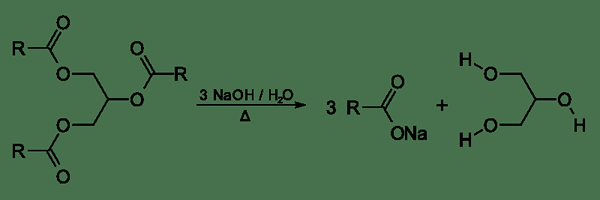
Figura 2: proceso general de saponificación
Mecanismo de reacción de saponificación:
- Ataque nucleofílico
- Reordenamiento
- Eliminación del grupo de salida
- Desprotonación
Los iones hidroxilo (oh-) actuar como nucleófilos ya que son ricos con electrones. Estos iones pueden atacar el enlace éster (-c-o-o-) del éster. Atacan el átomo de carbono de este enlace porque el átomo de carbono tiene una carga positiva parcial debido a la presencia de átomos de oxígeno unidos al átomo de carbono. Entonces el ion oh forma un enlace covalente con el átomo de carbono. Pero el átomo de carbono no puede tener cinco enlaces covalentes, ya que es un estado inestable de carbono. Por lo tanto, se produce un paso de reordenamiento después de esta formación de enlace. En el paso de reordenamiento, las moléculas se están estables mediante la eliminación del grupo (que provino del alcohol que se usaba para hacer el éster). Es el grupo de salida de la reacción de saponificación. Se produce una desprotonación del ácido carboxílico porque el ion carboxilato es la forma estable en un medio básico.
¿Cuál es la diferencia entre esterificación y saponificación??
Esterificación vs saponificación | |
| La esterificación es la formación de un éster a partir de la reacción entre un ácido carboxílico y un alcohol. | La saponificación es el desglose de un éster en un ácido carboxílico y un alcohol. |
| Requisito de energía | |
| La esterificación requiere energía en forma de calor. | La saponificación no requiere energía externa. |
| Reactivos | |
| Los reactivos de la esterificación son alcohol y ácido carboxílico. | Los reactivos de la saponificación son éster y base junto con agua. |
| Catalizador | |
| La esterificación requiere un catalizador ácido. | La saponificación requiere un catalizador base. |
Resumen -Esterificación vs Saponificación
La esterificación y la saponificación son reacciones químicas importantes en la química. La esterificación es la síntesis de éster, y la saponificación es la rotura del enlace éster. La diferencia clave entre la esterificación y la saponificación es que el proceso de esterificación implica la formación de un éster, mientras que el proceso de saponificación implica romper un éster en sus materiales de partida.
Referencia:
1. Helmenstine, Anne Marie, PH.D. “Definición y reacción de saponificación."Thinkco, octubre. 3, 2017, disponible aquí.
2. "Saponificación."Wikipedia, Fundación Wikimedia, 3 de abril. 2018, disponible aquí.
3. Esterificación: alcoholes y ácidos carboxílicos. Disponible aquí.
Imagen de cortesía:
1. "Formación de ésteres" de Laghi.L - Trabajo propio (CC By -SA 3.0) a través de Commons Wikimedia
2. "SaponificationGenera" de V8RIK en English Wikipedia (CC BY-SA 3.0) a través de Commons Wikimedia


