Diferencia entre el sulfato férrico y ferroso

El diferencia clave entre el sulfato férrico y ferroso es que El sulfato férrico tiene hierro en el estado de oxidación de +3, mientras que el sulfato ferroso tiene hierro en el estado de oxidación +2.
El sulfato férrico y ferroso son sulfatos de hierro. Son compuestos iónicos que contienen cationes (hierro en diferentes estados de oxidación) y aniones (aniones de sulfato). La fórmula química del sulfato férrico es Fe2(ENTONCES4)3 mientras que la fórmula química del sulfato ferroso es feso4.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el sulfato férrico?
3. ¿Qué es el sulfato ferroso?
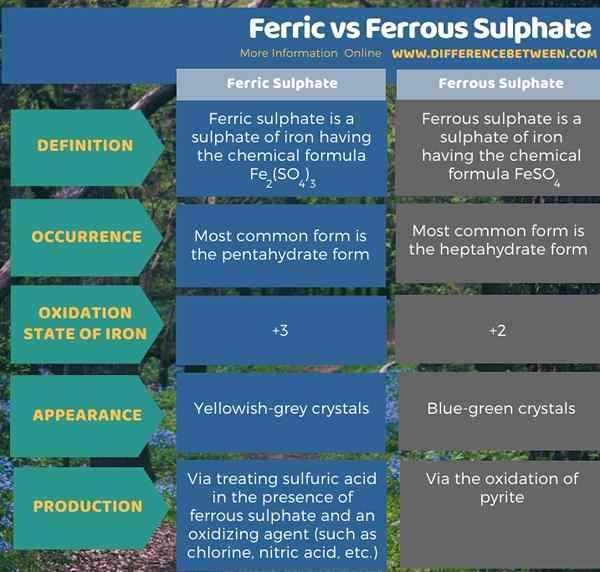
4. Comparación de lado a lado: sulfato férrico vs ferroso en forma tabular
5. Resumen
¿Qué es el sulfato férrico??
El sulfato férrico es un sulfato de hierro que tiene la fórmula química Fe2(ENTONCES4)3. El hierro en este compuesto está en el estado de oxidación de +3. El nombre químico es hierro (iii) sulfato. Es soluble en agua y generalmente aparece en cristales de color de color gris amarillento. Hay forma anhidra, así como algunas formas hidratadas. La masa molar de la forma anhidra es 399.9 g/mol. Sin embargo, la forma anhidra rara vez ocurre en la naturaleza. La forma de pentahidrato (que tiene cinco moléculas de agua asociadas con una molécula de sulfato férrico) es la forma más común.

Figura 01: Apariencia de sulfato férrico
En el proceso de producción, este compuesto se obtiene como una solución en lugar de un sólido. La producción a gran escala implica el tratamiento del ácido sulfúrico en presencia de sulfato ferroso y un agente oxidante (como cloro, ácido nítrico, etc.)
¿Qué es el sulfato ferroso??
El sulfato ferroso es un sulfato de hierro que tiene la fórmula química feso4. El hierro en este compuesto está en el estado de oxidación +2. El nombre químico del sulfato ferroso es el sulfato de hierro (ii). Hay formas anhidros y formas hidratadas. La forma más común es la forma de heptahidrato. Tiene siete moléculas de agua asociadas con una molécula de sulfato ferroso. Esta forma de heptahidrato ocurre como cristales de color verde azulado.

Figura 02: Cristales de heptahidrato de sulfato ferroso
El sulfato ferroso se prepara comercialmente por oxidación de pirita. Sin embargo, otro método que produce este compuesto en grandes cantidades como subproducto es el acabado de acero. Aquí, la lámina de acero pasa a través de un baño de decapado que contiene ácido sulfúrico.
¿Cuál es la diferencia entre sulfato férrico y ferroso??
El sulfato férrico y ferroso son sulfatos de hierro. La diferencia clave entre el sulfato férrico y ferroso es que el sulfato férrico tiene hierro en el estado de oxidación de +2, mientras que el sulfato ferroso tiene hierro en el estado de oxidación +3. El sulfato férrico es un sulfato de hierro que tiene la fórmula química Fe2(ENTONCES4)3 Mientras que el sulfato ferroso es un sulfato de hierro que tiene la fórmula química feso4. Las formas anhidro de estos compuestos son raras; Por lo tanto, podemos encontrar la forma hidratada más común de sulfato férrico como la forma pentahidratada; La forma más común de sulfato ferroso es la forma de heptahidrato.
Además, la forma hidratada más común de sulfato férrico aparece en cristales de gris amarillento, mientras que el sulfato ferroso aparece en forma de cristal azul verde. Por lo tanto, esta es una diferencia fácilmente distinguible entre el sulfato férrico y ferroso. Al considerar el proceso de producción, podemos producir sulfato férrico mediante el tratamiento del ácido sulfúrico en presencia de sulfato ferroso y un agente oxidante (como cloro, ácido nítrico, etc.). Mientras tanto, podemos producir sulfato ferroso a través de la oxidación de la pirita. Sin embargo, otro método que produce este compuesto en grandes cantidades como subproducto es el acabado de acero.
Resumen - Sulfato ferroso vs ferroso
El sulfato férrico y ferroso son sulfatos de hierro. La diferencia clave entre el sulfato férrico y ferroso es que el sulfato férrico tiene hierro en el estado de oxidación de +2, mientras que el sulfato ferroso tiene hierro en el estado de oxidación +3.
Referencia:
1."Sulfato férrico."Centro Nacional de Información de Biotecnología. Base de datos de compuestos de pubChem, u.S. Biblioteca Nacional de Medicina, disponible aquí.
2. "Sulfato de hierro (ii)."Wikipedia, Fundación Wikimedia, 18 de septiembre. 2019, disponible aquí.
3. "Sulfato de hierro (iii)."Wikipedia, Fundación Wikimedia, 23 de septiembre. 2019, disponible aquí.
4. "Compuestos."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 13 de junio de 2019, disponible aquí.
Imagen de cortesía:
1. "Síran železitý" de Ondřej mangl - Trabajo propio (dominio público) a través de Commons Wikimedia
2. "Iron (II) -sulfato-Heptahidrato-Muestra" por Benjah-BMM27-Trabajo propio (dominio público) a través de Commons Wikimedia


