Diferencia entre la primera y tercera serie de transición
El diferencia clave Entre la primera y tercera serie de transición es que El orbital D más externo de la primera serie de transición es 3D, mientras que la serie de transición orbital más externa es 4D y el orbital D más externo en la tercera serie de transición es 5D.
Un metal de transición es un elemento químico que tiene un orbital D parcialmente lleno. En la tabla periódica de elementos, hay tres series de elementos de transición; Los nombramos como la primera, segunda y tercera serie de transición. Estos son elementos químicos de tres períodos diferentes en la tabla periódica. Por lo tanto, contienen diferentes orbitales más externos.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Cuál es la primera serie de transición?
3. ¿Cuál es la segunda serie de transición?
4. ¿Cuál es la tercera serie de transición?
5. Comparación de lado a lado - Primera vs SEGURA VS TERDER SERIE DE TRANSICIÓN EN TABULAR
6. Resumen
¿Cuál es la primera serie de transición??
La primera serie de transición es la lista de elementos químicos que van desde escandio hasta cobre. También podemos describirlos como metales de transición de primera fila porque estos son metales incluidos en el primer período del bloque D, que contiene los metales de transición. Por lo tanto, al considerar la configuración de electrones de estos elementos, todos estos elementos tienen electrones 3D y 4S. Esto significa que los orbitales D más externos de estos elementos son orbitales 3D. Además, los elementos de esta serie contienen una configuración de electrones Argón completa con electrones 3D y 4S.
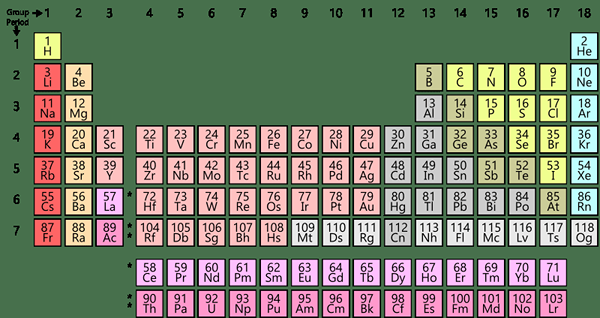
Figura 01: Tabla periódica de elementos
Elementos químicos en la primera serie de transición
La lista de los elementos químicos de esta serie es la siguiente:
- Escandio
- Titanio
- Vanadio
- Cromo
- Manganeso
- Hierro
- Cobalto
- Níquel
- Cobre
¿Cuál es la segunda serie de transición??
La segunda serie de transición es la lista de elementos químicos que van desde el itrio hasta la plata. Podemos nombrarlos como metales de transición de segunda fila también porque están en el segundo período del bloque D y son metales. Las configuraciones de electrones de estos elementos tienen orbitales 4D y 5S; Por lo tanto, los orbitales D más externos son orbitales 4D. Además, los elementos de esta serie contienen una configuración completa de electrones de Krypton con electrones 4D y 5S. Los miembros de esta lista son los siguientes:
Elementos químicos en la segunda serie de transición
- Itrio
- Circonio
- Niobio
- Molibdeno
- Tecnecio
- Rutenio
- Rodio
- Paladio
- Plata
¿Cuál es la tercera serie de transición??
La tercera serie de transición es la lista de elementos químicos que van desde el hafnio hasta el oro, más el lantano. Estos se encuentran en el tercer período del bloque D, y también contiene el primer miembro de la serie de lantanidas (lantano) porque los elementos de la tercera serie de transición y el lantano tienen orbitales de electrones 5D y 6S en su configuración de electrones. Además, los elementos de esta serie contienen una configuración completa de electrones de Xenon con electrones 5D y 6S.

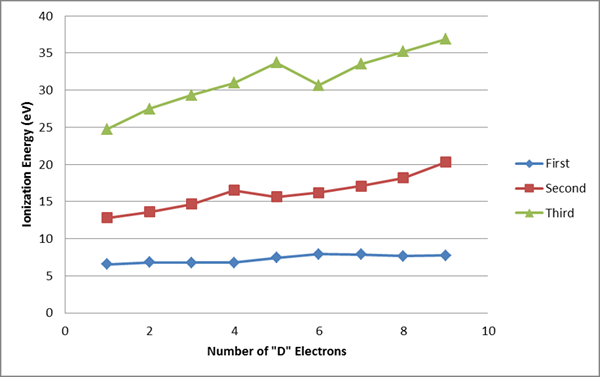
Figura 02: energías ionizantes de los elementos de transición primero, segundo y tercero
Elementos químicos en la tercera serie de transición
- Lantano
- Hafnio
- Tántalo
- Tungsteno
- Renio
- Osmio
- Indio
- Platino
- Oro
¿Cuál es la diferencia entre la primera y tercera serie de transición??
En la tabla periódica de elementos, hay tres series de elementos de transición que nombramos como primera, segunda y tercera serie de transición. La diferencia clave entre la primera y tercera serie de transición es que el orbital D más externo de los elementos de la primera serie de transición es 3D, mientras que el orbital D más externo de la segunda serie de transición es 4D y el orbital D de la tercera serie de transición es 5D es 5D.
Además, la primera serie de transición es la lista de elementos químicos que van desde escandio hasta cobre. La segunda serie de transición es la lista de elementos químicos que van desde el itrio hasta la plata, mientras que la tercera serie de transición es la lista de elementos químicos que van desde el hafnium hasta el oro, más el lantano. Entre estas tres series, la segunda y tercera serie de transición tienen propiedades estrechamente relacionadas, que difieren considerablemente de las propiedades de la primera serie de transición.
Además, los elementos de la primera serie de transición contienen una configuración completa de Argon Electron con electrones 3D y 4S. Sin embargo, la segunda serie de transición contiene una configuración completa de electrones de Krypton con electrones 4D y 5S. Mientras tanto, los elementos de la tercera serie de transición contienen una configuración completa de Xenon Electron con electrones 5D y 6S. Entonces, esta también es una diferencia significativa entre la primera y tercera serie de transición.
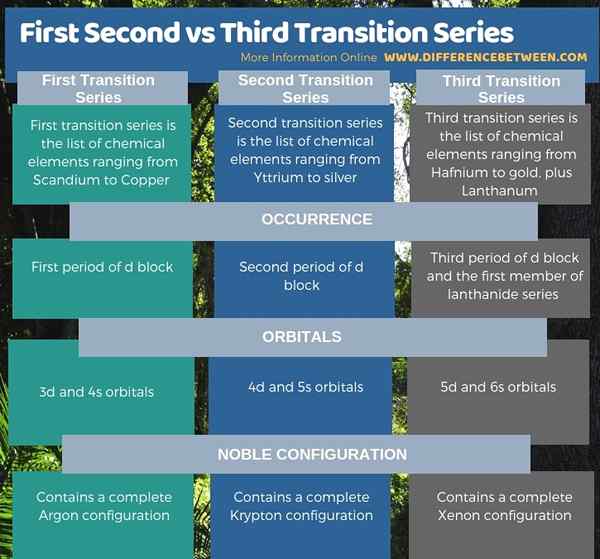
Resumen -Primera vs Second vs Third Transition Series
En la tabla periódica de elementos, hay tres series de elementos de transición; Los nombramos como la primera, segunda y tercera serie de transición. La diferencia clave entre la primera y tercera serie de transición es que el orbital D más externo de los elementos de la primera serie de transición es 3D, mientras que el orbital D más externo de la segunda serie de transición es 4D y el orbital D de la tercera serie de transición es 5D es 5D.
Referencia:
1. "23.1: Propiedades generales de los metales de transición."Bibliotecas de química, Librettexts, 18 de septiembre. 2019, disponible aquí.
2. "Tercera serie de transición (o) series 5D."Simplemente ciencia, disponible aquí.
Imagen de cortesía:
1. "Energías de ionización de metales de transición" por Oncandor - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia
2. "Simple Periódico Table Chart -en" de Offnfopt - Trabajo propio (dominio público) a través de Commons Wikimedia


