Diferencia entre los radicales libres y las especies reactivas de oxígeno
El diferencia clave entre los radicales libres y las especies reactivas de oxígeno es que Los radicales libres pueden o no contener átomos de oxígeno, mientras que las especies reactivas de oxígeno esencialmente contienen átomos de oxígeno.
Por lo general, usamos los términos radicales libres y las especies reactivas de oxígeno indistintamente porque las especies reactivas de oxígeno son siempre compuestos de radicales libres. Sin embargo, no todos los radicales libres son especies reactivas de oxígeno; Pueden o no contener átomos de oxígeno, pero son muy reactivos debido a la presencia de un electrón no apareado. Por lo tanto, ambas formas tienden a reaccionar con fuentes adecuadas para obtener un electrón para acoplar con su electrón no apartado para que la configuración de electrones se vuelva estable.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué son los radicales libres?
3. ¿Qué son las especies reactivas de oxígeno?
4. Comparación de lado a lado: oxígeno atómico frente a especies de oxígeno molecular en forma tabular
5. Resumen
¿Qué son los radicales libres??
Los radicales libres son átomos reactivos o grupo de átomos que contienen uno o más electrones no apareados. Son altamente reactivos debido a la presencia de un electrón no apareado. Además, los radicales libres son muy inestables, y tienden a estabilizarse mediante la obtención de electrones del exterior para llenar orbitales vacíos. Reaccionan con otros compuestos químicos para capturar el electrón necesario. Los radicales libres son intermedios importantes en los procesos naturales. Podemos denotar radicales libres por un punto superíndice a la derecha. Por ejemplo, H., CL., HO., H3C.
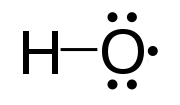
Figura 01: radical hidroxilo
Los radicales libres de larga vida se encuentran en tres categorías: radicales estables, radicales persistentes y di-radicales.
- Radicales estables: el principal ejemplo de un radical estable es el oxígeno molecular O2. Los radicales orgánicos que contienen el sistema π conjugado pueden vivir mucho.
- Radicales persistentes: son de larga vida debido al hacinamiento estérico alrededor del centro radical y los hacen físicamente difíciles de reaccionar con otra molécula.
- Di-Radicals: algunas moléculas tienen dos centros radicales; Los nombramos como di-radicales. Oxígeno molecular naturalmente (oxígeno atmosférico) existe como un diradical.
¿Qué son las especies reactivas de oxígeno?
Las especies reactivas de oxígeno son radicales que son altamente reactivos y contienen electrones no apareados. La denotación para este término es ROS. Estas especies químicas esencialmente contienen átomos de oxígeno que contienen un electrón no apareado. Algunos ejemplos comunes incluyen peróxido, superóxido, radical hidroxilo, oxígeno alfa, etc.

Figura 02: Formación de ROS endógenamente
Diferentes reacciones químicas forman estas especies reactivas de oxígeno; Por ejemplo, la reducción del oxígeno molecular forma superóxido y esta especie reactiva de oxígeno actúa como un precursor para muchas otras formaciones radicales. Los peróxidos son otro tipo de ROS importante que se forma a partir de la dismutación del superóxido.
Hay vías endógenas y exógenas para producir ROS. Por ejemplo, las especies reactivas de oxígeno se forman en diversas reacciones biológicas dentro de las células y los orgánulos como los peroxisomas. La producción exógena de ROS se refiere a la formación de especies reactivas de oxígeno debido a la influencia de agentes externos como contaminantes, metales pesados, humo, drogas, etc.
¿Cuál es la diferencia entre los radicales libres y las especies reactivas de oxígeno??
Por lo general, usamos los términos radicales libres y las especies reactivas de oxígeno indistintamente porque las especies reactivas de oxígeno son siempre compuestos de radicales libres. Sin embargo, no todos los radicales libres son especies reactivas de oxígeno. La diferencia clave entre los radicales libres y las especies reactivas de oxígeno es que los radicales libres pueden contener o no átomos de oxígeno, mientras que las especies reactivas de oxígeno contienen esencialmente átomos de oxígeno.
A continuación se muestra un resumen de la diferencia entre los radicales libres y las especies reactivas de oxígeno.

Resumen -Radicales libres vs especies reactivas de oxígeno
Los radicales libres son átomos reactivos o grupo de átomos que contienen uno o más electrones no apareados, mientras que las especies reactivas de oxígeno son radicales que son altamente reactivos y contienen electrones no apareados. La diferencia clave entre los radicales libres y las especies reactivas de oxígeno es que los radicales libres pueden contener o no átomos de oxígeno, mientras que las especies reactivas de oxígeno contienen esencialmente átomos de oxígeno.
Referencia:
1."Especies de oxígeno reactivas."Wikipedia, Fundación Wikimedia, 4 de noviembre. 2019, disponible aquí.
2. "¿Qué son los radicales libres??"Fitoquímicos, disponibles aquí.
3. "Radical (Química)."Wikipedia, Fundación Wikimedia, 27 de noviembre. 2019, disponible aquí.
Imagen de cortesía:
1. "Radical hidroxilo" de Smokeyjoe - Trabajo propio (CC By -SA 4.0) a través de Commons Wikimedia
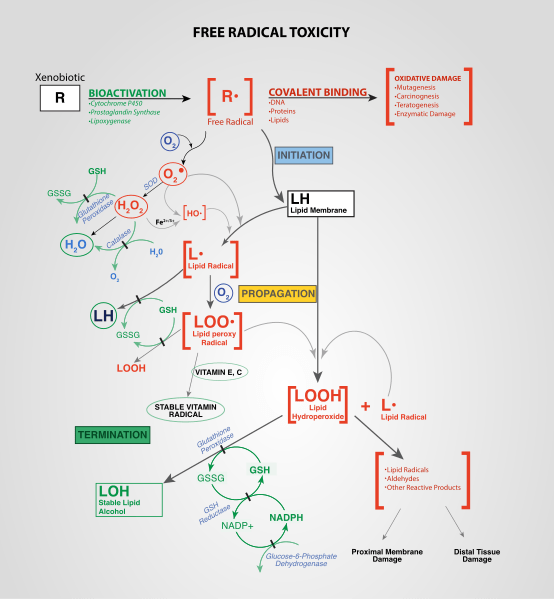
2. "Toxicidad radical libre" de Dan COJOCARI - Own Worker (CC By -SA 4.0) a través de Commons Wikimedia


