Diferencia entre el punto de congelación y la depresión del punto de congelación

El diferencia clave entre el punto de congelación y la depresión del punto de congelación es que El punto de congelación es la temperatura a la que un líquido se convierte en un sólido, mientras que la depresión del punto de congelación es la disminución del punto de congelación de un solvente debido a la adición de un soluto al solvente.
El punto de congelación es un valor de temperatura en el que un cambio de fase de la materia tiene lugar de fase líquida a sólida. La mayoría de las veces, es similar al punto de fusión de un material en el que un sólido se convierte en su estado líquido.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el punto de congelación?
3. ¿Qué es la depresión del punto de congelación?
4. Comparación lado a lado: punto de congelación frente a la depresión del punto de congelación en forma tabular
6. Resumen
¿Qué es el punto de congelación??
El punto de congelación es la temperatura a la que un líquido se vuelve sólido. En el punto de congelación, la transición líquida a sólida de la fase de la materia ocurre en el punto de fusión, la fase sólida se convierte en su fase líquida. Teóricamente, el punto de congelación es igual al punto de fusión. Pero prácticamente, podemos superar líquidos más allá del punto de congelación.

Podemos usar los términos congelamiento y solidificación indistintamente, pero algunos autores tienden a diferenciarse entre estos dos términos porque la congelación ocurre debido a los cambios en la temperatura, mientras que la solidificación puede ocurrir debido a cambios en la presión también.
Conocer el punto de congelación de los materiales es muy importante en diferentes aplicaciones, incluida la preservación de los alimentos, donde podemos inhibir la descomposición de los alimentos y el crecimiento de microorganismos, congelación de organismos o tejidos vivos durante la preservación de los tejidos, etc.
¿Qué es la depresión del punto de congelación??
La depresión del punto de congelación es la disminución del punto de congelación de un solvente debido a la adición de un soluto al solvente. Esta es una propiedad coligatoria, lo que significa que la depresión del punto de congelación depende solo de la cantidad de solutos, no de la naturaleza del soluto. Después del punto de congelación, se ha producido depresión de la sustancia, el punto de congelación del solvente disminuye a un valor más bajo que el del solvente puro. La depresión del punto de congelación es la razón por la cual el agua de mar permanece en estado líquido incluso a 0 ° C (el punto de congelación de agua pura).
Sin embargo, el soluto agregado debe ser un soluto no volátil; Si no, el soluto no afecta el punto de congelación del solvente porque se volatiliza fácilmente. Este concepto también se puede utilizar para explicar los cambios en el punto de congelación de las mezclas sólidas. Los compuestos sólidos finamente en polvo tienen un punto de congelación más bajo que los compuestos sólidos puros cuando están presentes las impurezas (mezcla sólida-sólida).
El punto de congelación es la temperatura a la que la presión de vapor de un disolvente y la presión de vapor de la forma sólida de ese solvente es igual. Si se agrega un soluto no volátil a este disolvente, la presión de vapor del solvente puro disminuye. Entonces la forma sólida del solvente puede permanecer en equilibrio con el solvente incluso a temperaturas más bajas que el punto de congelación normal.
¿Cuál es la diferencia entre el punto de congelación y la depresión del punto de congelación??
El punto de congelación es un valor de temperatura en el que se produce un cambio de fase de la materia. La diferencia clave entre el punto de congelación y la depresión del punto de congelación es que el punto de congelación es la conversión de la fase líquida en fase sólida debido al cambio de temperatura, mientras que la depresión del punto de congelación es la disminución del punto de congelación de un solvente debido a la adición de un soluto en el solvente.
La siguiente infografía resume las diferencias entre el punto de congelación y la depresión del punto de congelación en forma tabular.

Resumen -Punto de congelación vs depresión del punto de congelación
El punto de congelación es un valor de temperatura, mientras que la liberación de la depresión del punto es un resultado. La diferencia clave entre el punto de congelación y la depresión del punto de congelación es que el punto de congelación es la temperatura a la que un líquido se vuelve sólido, mientras que la depresión del punto de congelación es la disminución del punto de congelación de un solvente debido a la adición de un soluto al solvente.
Referencia:
1. Helmenstine, Anne Marie. "¿Cuál es el punto de congelación del agua??"Thinkco, agosto. 28, 2020, disponible aquí.
Imagen de cortesía:
1. "Light Gelling Off Icículos" de Daler Boi - Trabajo propio (CC By -SA 4.0) a través de Commons Wikimedia
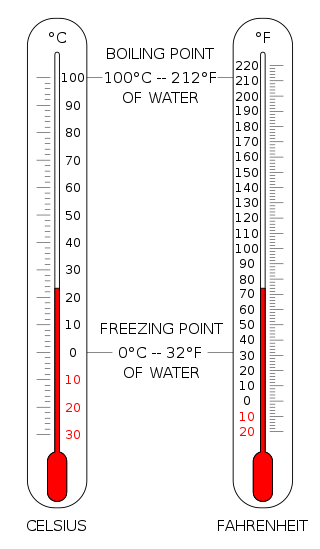
2. "Termómetro cf" de Gringer - N /A (dominio público) a través de Commons Wikimedia


