Diferencia entre fusión y vaporización
El diferencia clave Entre la fusión y la vaporización es que La fusión es la conversión de un sólido en un líquido, mientras que la vaporización es la conversión de un líquido en su vapor.
El término fusión tiene diferentes definiciones en diferentes campos, pero en química física, lo usamos para describir el proceso de fusión. Eso es; La fusión es la conversión de una fase sólida en su fase líquida. Por otro lado, la conversión de un líquido en su sólido se conoce como congelación o solidificación. Si la fase líquida de una sustancia se convierte en la fase gaseosa, entonces la llamamos vaporización. Además, las energías requeridas para cada conversión se conocen como "calor de fusión" y "calor de vaporización".
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es la fusión
3. ¿Qué es la vaporización?
4. Comparación lado a lado: fusión vs vaporización en forma tabular
5. Resumen
Que es la fusión?
La fusión es el proceso de fusión donde una fase sólida se convierte en su fase líquida. Por lo tanto, este término se refiere a una transición de fase. Ocurre en el punto de fusión de la sustancia. La energía requerida para este proceso se llama "calor de fusión". Durante la fusión, la entropía del sistema aumenta porque las partículas que estaban en lugares fijos en el sólido tienden a tener la oportunidad de moverse en la fase líquida (esto aumenta la aleatoriedad, aumentando la entropía).
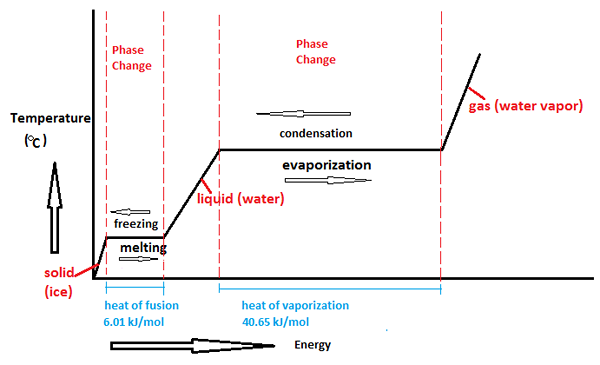
Figura 01: Cambio de fase en el agua
El calor de la fusión o la entalpía de la fusión es el cambio de entalpía. Proporcionar energía térmica a una sustancia para cambiar su fase de fase sólida a fase líquida a una presión constante da como resultado un cambio en la entalpía. La entalpía de la solidificación es el fenómeno opuesto, y tiene el mismo valor para la cantidad requerida de energía. Básicamente,
Calor de fusión = energía térmica / masa
¿Qué es la vaporización??
La vaporización es el proceso de conversión de una fase líquida en su fase de vapor. La entropía del sistema aumenta aún más porque las partículas en la fase líquida obtienen la capacidad de moverse libremente en la fase de vapor. El calor de vaporización o la entalpía de la vaporización es el cambio de entalpía cuando un líquido se convierte en su vapor y esto es una función de presión.

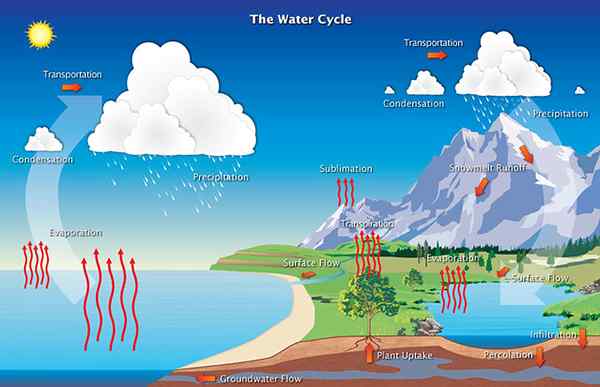
Figura 02: El vapor de agua se condensa para formar nubes durante el ciclo del agua
La vaporización puede ocurrir de dos maneras principales:
Evaporación
La evaporación ocurre en la superficie del líquido. Ocurre a temperaturas por debajo del punto de ebullición del líquido a la misma presión. Además, ocurre solo cuando la presión de vapor parcial es menor que la presión de vapor de equilibrio.
Hirviendo
Hervir es la formación de vapor como burbujas dentro del líquido. A diferencia de la vaporización, la ebullición forma vapor debajo de la superficie del líquido. Ocurre cuando la presión de vapor de equilibrio es igual o mayor que la presión ambiental.
¿Cuál es la diferencia entre fusión y vaporización??
La fusión es otro término para el proceso de fusión. La vaporización es el proceso de formación de vapor a partir de un líquido, que puede suceder de una de las dos maneras: evaporación y ebullición. La diferencia clave entre la fusión y la vaporización es que la fusión es la conversión de un sólido en un líquido, mientras que la vaporización es la conversión de un líquido en su vapor. Al considerar el cambio de entalpía, llamamos al cambio en la entalpía durante el proceso de fusión como el calor de la fusión, mientras que el cambio en la entalpía durante la vaporización es el calor de la vaporización.

Resumen -Fusión vs vaporización
La fusión y la vaporización son dos conceptos químicos importantes que describen los cambios de dos fases. La diferencia clave entre la fusión y la vaporización es que la fusión es la conversión de un sólido en un líquido, mientras que la vaporización es la conversión de un líquido en su vapor.
Referencia:
1. Helmenstine, Anne Marie, “Definición de fusión (física y química)."Thinkco, Mar. 9, 2019, disponible aquí.
2. "Entalpía de la fusión."Wikipedia, Fundación Wikimedia, 5 APR. 2019, disponible aquí.
Imagen de cortesía:
1. "Diagrama de cambio de fase de agua" por Cawang - Trabajo propio (CC BY -SA 3.0) a través de Commons Wikimedia
2. "El ciclo del agua" por Airs (CC por 2.0) a través de Flickr


