Diferencia entre isómeros geométricos y isómeros estructurales

Isómeros geométricos vs isómeros estructurales
Los isómeros son compuestos diferentes con la misma fórmula molecular. Hay varios tipos de isómeros. Los isómeros se pueden dividir principalmente en dos grupos como isómeros y estéreo constitucionales. Los isómeros constitucionales son isómeros donde la conectividad de los átomos difiere en las moléculas. En los estereisómeros, los átomos están conectados en la misma secuencia, a diferencia de los isómeros constitucionales. Los estereoisómeros difieren solo en la disposición de sus átomos en el espacio. Los estereoisómeros pueden ser de dos tipos, enantiómeros y diastereómeros. Los diastereómeros son estereoisómeros, cuyas moléculas no son imágenes espejo entre sí. Los enantiómeros son estereoisómeros, cuyas moléculas son imágenes de espejo no posibles entre sí. Los enantiómeros ocurren solo con moléculas quirales. Una molécula quiral se define como una que no es idéntica con su imagen de espejo. Por lo tanto, la molécula quiral y su imagen de espejo son enantiómeros entre sí. Por ejemplo, la molécula de 2-butanol es quiral, y sus imágenes de espejo son enantiómeros.
Isómeros geométricos
Los isómeros geométricos son un tipo de estereoisómeros. Este tipo de isómeros resulta, cuando las moléculas tienen una rotación restringida, básicamente, debido a un doble enlace. Cuando hay un solo enlace de carbono de carbono, la rotación es posible. Por lo tanto, sin embargo, dibujamos los átomos, su disposición será el mismo. Pero cuando hay un doble enlace de carbono -carbono, podemos dibujar dos arreglos de átomos en una molécula. Los isómeros resultantes se conocen como cis, isómeros trans o isómeros E-Z. En el isómero cis, los mismos tipos de átomos están en el mismo lado de la molécula. Pero en Trans Isomer, los mismos tipos de átomos están en el lado opuesto de la molécula. Por ejemplo, las estructuras cis y trans para 1,2-dicloroetano son las siguientes.
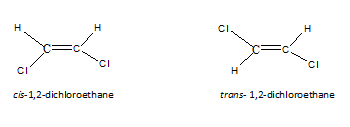
Para que una molécula tenga isómeros geométricos, no solo es suficiente tener un doble enlace solo. Los dos átomos o grupos unidos a un extremo del doble enlace deben ser diferentes. Por ejemplo, seguir la molécula no tiene isómeros geométricos, ambos átomos en el extremo izquierdo son hidrógenos. Debido a eso, si lo dibujamos en cis o trans, ambas moléculas son las mismas.
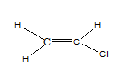
Pero no importa si los cuatro grupos o átomos adjuntos son diferentes. En esa ocasión, podemos nombrarlos como E o Z.
Isómeros estructurales
Estos también se conocen como isómeros constitucionales. Los isómeros constitucionales son isómeros, donde la conectividad de los átomos difiere en las moléculas. El butano es el alcano más simple para mostrar el isomerismo constitucional. Butane tiene dos isómeros constitucionales, Butano mismo e Isobuteno.
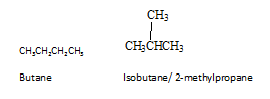
Dado que sus conectividades son diferentes, dos moléculas tienen diferentes propiedades físicas y químicas. Los isómeros estructurales se pueden formar mediante hidrocarburos donde tienen un mínimo de cuatro átomos de carbono. Hay tres tipos de isómeros estructurales como isómeros de grupo esquelético, posicional y funcional. En el isomerismo esquelético, como se da en el ejemplo anterior, el esquelético se reorganiza para dar diferentes isómeros. En los isómeros de posición, un grupo funcional u otro grupo cambia de posición. En los isómeros de grupo funcional, aunque tienen la misma fórmula, las moléculas difieren a tener diferentes grupos funcionales.
| Cuál es la diferencia entre Isómeros geométricos e isómeros estructurales? • Los isómeros geométricos son estereoisómeros. Por lo tanto, las conectividades también son las mismas en comparación con los isómeros estructurales, donde los isómeros difieren debido a las conectividades de los átomos. En los isómeros geométricos, difieren debido a la disposición tridimensional en el espacio. • A menudo para una molécula hay dos isómeros geométricos como cis, trans o e, z, pero para una molécula puede haber una gran cantidad de isómeros estructurales. • El isomerismo geométrico se muestra básicamente por molécula con dobles enlaces carbono-carbono. El isomerismo estructural se muestra mediante alcanos, alquenos, alquinos y compuestos aromáticos, también. |


