Diferencia entre la capacidad de calor y el calor específico
El diferencia clave Entre la capacidad de calor y el calor específico es que La capacidad de calor depende de la cantidad de sustancia, mientras que la capacidad de calor específica es independiente de la misma.
Cuando calentamos una sustancia, su temperatura aumenta, y cuando la enfriamos, su temperatura disminuye. Esta diferencia de temperatura es proporcional a la cantidad de calor suministrado. La capacidad de calor y el calor específico son dos constantes de proporcionalidad que se relacionan con el cambio de temperatura y la cantidad de calor.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la capacidad de calor?
3. ¿Qué es el calor específico?
4. Comparación de lado a lado: capacidad de calor frente al calor específico en forma tabular
5. Resumen
¿Qué es la capacidad de calor??
En la termodinámica, la energía total de un sistema es la energía interna. La energía interna especifica la energía cinética y potencial total de las moléculas en el sistema. Podemos cambiar la energía interna de un sistema, ya sea trabajando en el sistema o calentándolo. La energía interna de una sustancia aumenta cuando aumentamos su temperatura. La cantidad de aumento depende de las condiciones en las que se realiza el calentamiento. Aquí necesitamos calor para aumentar la temperatura.
La capacidad de calor (c) de una sustancia es "la cantidad de calor necesaria para elevar la temperatura de una sustancia en un grado Celsius (o un Kelvin)."La capacidad de calor difiere de sustancia a sustancia. La cantidad de sustancia es directamente proporcional a la capacidad de calor. Eso significa que al duplicar la masa de una sustancia, la capacidad de calor se duplica. El calor necesitamos aumentar la temperatura de t1 a t2 de una sustancia se puede calcular utilizando la siguiente ecuación.
q = c x ∆t
Q = calor requerido
∆t = t1-T2

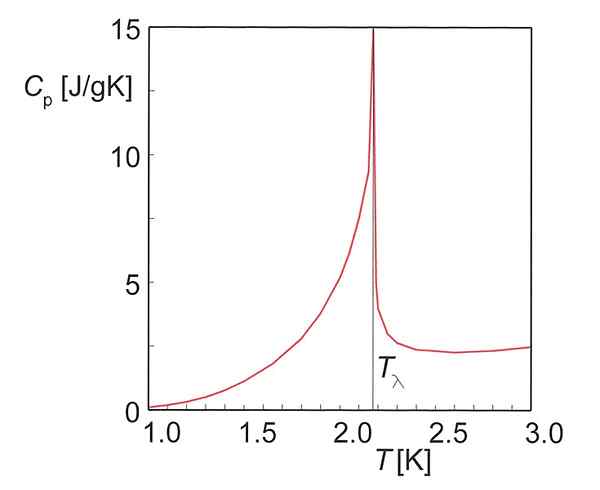
Figura 01: Capacidad de calor del helio
La unidad de capacidad térmica es jºC-1 o JK-1. Dos tipos de capacidades de calor se definen en la termodinámica; Capacidad de calor a presión constante y capacidad de calor a volumen constante.
¿Qué es el calor específico??
La capacidad de calor depende de la cantidad de sustancia. Calor específico o capacidad térmica específica es la capacidad de calor que es independiente de la cantidad de sustancias. Podemos definirlo como "la cantidad de calor requerida para elevar la temperatura de un gramo de una sustancia en un grado Celsius (o un Kelvin) a una presión constante."
La unidad de calor específico es JG-1oC-1. El calor específico del agua es muy alto, con un valor de 4.186 JG-1oC-1. Esto significa que para aumentar la temperatura de 1 g de agua en 1 ° C, necesitamos 4.186 J de energía térmica. Este alto valor explica el papel del agua en la regulación térmica. Para encontrar el calor necesario para aumentar la temperatura de una cierta masa de una sustancia de T1 a T2, se puede usar la siguiente ecuación.
q = m x s x ∆t
Q = calor requerido
m = masa de la sustancia
∆t = t1-T2
Sin embargo, la ecuación anterior no se aplica si la reacción implica un cambio de fase; Por ejemplo, cuando el agua va a una fase gaseosa (en el punto de ebullición), o cuando el agua se congela para formar hielo (en el punto de fusión). Esto se debe a que el calor agregado o eliminado durante el cambio de fase no cambia la temperatura.
¿Cuál es la diferencia entre la capacidad del calor y el calor específico??
La diferencia clave entre la capacidad de calor y el calor específico es que la capacidad de calor depende de la cantidad de sustancia, mientras que la capacidad de calor específica es independiente de la misma. Además, al considerar la teoría, la capacidad de calor de la cantidad de calor necesaria para cambiar la temperatura de una sustancia en 1 ° C o 1K, mientras que el calor específico es el calor necesario para cambiar 1 g de la temperatura de las sustancias en 1 ° C o 1K.

Resumen -Capacidad de calor versus calor específico
La capacidad del calor y el calor específico son términos importantes en termodinámica. La diferencia clave entre la capacidad de calor y el calor específico es que la capacidad de calor depende de la cantidad de sustancia, mientras que la capacidad de calor específica es independiente de la misma.
Referencia:
1. Helmenstine, Anne Marie. "Capacidad térmica específica en química."Thinkco, Mar. 21, 2019, disponible aquí.
Imagen de cortesía:
1. "Capacidad de calor de 4He 01" por Adwaele en English Wikipedia (CC By-SA 3.0) a través de Commons Wikimedia


