Diferencia entre hiperconjugación y resonancia
Diferencia de clave: Hyperconjugation vs Resonance
La hiperconjugación y la resonancia pueden estabilizar moléculas o iones poliatómicos de dos maneras diferentes. Los requisitos para estos dos procesos son diferentes. Si una molécula puede tener más de una estructura de resonancia, esa molécula posee la estabilización de resonancia. Pero, la hiperconjugación ocurre en presencia de un enlace σ con un orbital P vacío o parcialmente lleno o un π-orbital. Este es el diferencia clave Hiperconjugación y resonancia
¿Qué es la hiperconjugación??
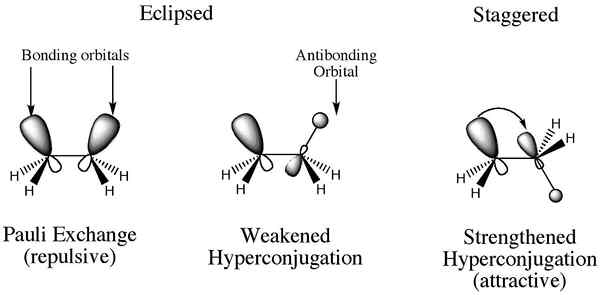
La interacción de los electrones en un enlace σ (generalmente enlaces C-H o C-C) con un P-Orbital o parcialmente relleno adyacente o un π-orbital en un orbital molecular extendido al aumentar la estabilidad del sistema. Esta interacción de estabilización se llama 'hiperconjugación. Según la teoría de los enlaces de valencia, esta interacción se describe como 'doble enlace sin resonancia de enlace'.

Hyperconjugación Schreiner
¿Qué es la resonancia??
La resonancia es el método para describir electrones delocalizados en una molécula o ion poliatómico cuando puede tener más de una estructura de Lewis para expresar el patrón de unión. Se pueden usar varias estructuras contribuyentes para representar estos electrones delocalizados en una molécula o un ion, y esas estructuras se llaman Estructuras de resonancia. Todas las estructuras contribuyentes se pueden ilustrar utilizando una estructura de Lewis con un número contable de enlaces covalentes distribuyendo el par de electrones entre dos átomos en el enlace. Dado que se pueden usar varias estructuras de Lewis para representar la estructura molecular. La estructura molecular real es un intermedio de todas esas posibles estructuras de Lewis. Se llama un resonancia híbrida. Todas las estructuras contribuyentes tienen los núcleos en la misma posición, pero la distribución de electrones puede ser diferente.
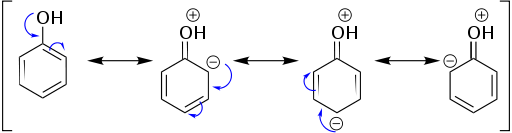
Resonancia de fenol
¿Cuál es la diferencia entre hiperconjugación y resonancia??
Características de hiperconjugación y resonancia
Hiperconjugación
- La hiperconjugación afecta la longitud del enlace, y da como resultado el acortamiento de los enlaces sigma (enlaces σ).
| Molécula | Longitud de enlace C-C | Razón |
| 1,3-butadieneno | 1.46 A | Conjugación normal entre dos partes de alquenilo. |
| Metilacetileno | 1.46 A | Hyperconjugación entre las partes alquilo y alquinilo |
| Metano | 1.54 A | Es un hidrocarburo saturado sin hiperconjugación |
- Las moléculas con hiperconjugación tienen valores más altos para el calor de formación en comparación con la suma de sus energías de enlace. Pero, el calor de hidrogenación por doble enlace es menor que el de Etileno.
- La estabilidad de las carbocaciones varía según el número de enlaces C-H unidos al átomo de carbono cargado positivamente. La estabilización de la hiperconjugación es mayor cuando se adjuntan muchos enlaces C-H.
(CH3)3C+ > (CH3)2Pez+ > (CH3) Ch2+ > CH3+
- La resistencia a la hiperconjugación relativa depende del tipo de isótopos del hidrógeno. El hidrógeno tiene una mayor resistencia en comparación con el deuterio (d) y el tritio (t). El tritio tiene la menor capacidad de mostrar hiperconjugación entre ellos. La energía requerida para romper el enlace C-T> Bond C-D> C-H Bond, y esto facilita que H HyperConjugation.
Resonancia
- Se pueden usar varias estructuras de Lewis para representar la estructura, pero la estructura real es un intermedio de estas estructuras contribuyentes, y está representada por un híbrido de resonancia.
- Las estructuras de resonancia no son isómeros. Estas estructuras de resonancia difieren solo en la posición de los electrones, pero no en la posición de los núcleos.
- Cada estructura de Lewis tiene un número igual de valencia y electrones no apareados, y esto lleva a tener la misma carga en cada estructura.
- La estructura real posee una energía potencial total más baja en comparación con el valor estimado de las estructuras contribuyentes. Por lo tanto, las moléculas/iones que tienen un híbrido de resonancia proporcionan una estabilización adicional a la molécula/ion respectiva.


