Diferencia entre la unión de hidrógeno intermolecular e intramolecular
Diferencia clave: intermolecular Vs enlace de hidrógeno intramolecular
El enlace de hidrógeno es una forma de fuerza de atracción entre ciertas moléculas polares. Es un tipo de unión débil que los enlaces iónicos o covalentes, pero son fuertes fuerzas de atracción en comparación con las fuerzas dipolo-dipolo y las fuerzas de van der Waal. Se forma un enlace de hidrógeno si la molécula polar tiene un átomo fuertemente electronegativo que tiene un par solitario de electrones (que puede actuar como donante de electrones) unido a un átomo de hidrógeno (un aceptador de electrones). Dado que el átomo fuertemente electronegativo puede atraer la par de electrones de enlace hacia sí mismo que el de un átomo de hidrógeno, el átomo de hidrógeno obtiene una carga positiva parcial, lo que resulta en una fuerte separación de carga. Por lo tanto, los enlaces químicos de formación de enlaces de hidrógeno comunes son enlaces O-H, enlaces N-H y enlaces F-H. Hay dos formas de enlaces de hidrógeno que se pueden formar; enlace de hidrógeno intermolecular que ocurre entre las moléculas polares y el enlace de hidrógeno intramolecular que ocurre en la misma molécula única. El diferencia clave entre un enlace de hidrógeno intermolecular e intramolecular es que El enlace de hidrógeno intermolecular ocurre entre dos moléculas, mientras que el enlace de hidrógeno intramolecular ocurre en una sola molécula.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el enlace de hidrógeno intermolecular?
3. ¿Qué es el enlace de hidrógeno intramolecular?
4. Comparación lado a lado: enlace de hidrógeno intramolecular intermolecular en forma tabular
5. Resumen
¿Qué es el enlace de hidrógeno intermolecular??
Los enlaces de hidrógeno intermoleculares se producen entre moléculas separadas en una sustancia. Por lo tanto, el donante de electrones y el aceptador de electrones deben estar presentes en dos moléculas separadas. Si hay donantes y aceptores de electrones adecuados, cualquier molécula puede formar enlaces de hidrógeno.

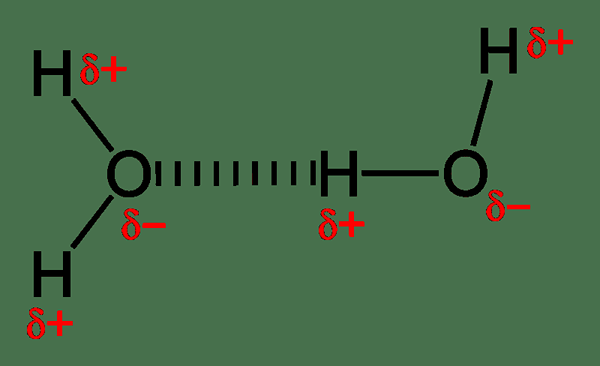
Figura 01: enlace de hidrógeno intermolecular en moléculas de agua
Un ejemplo común para las moléculas que pueden formar enlaces de hidrógeno intermoleculares son las moléculas de agua (H2O).Los enlaces de hidrógeno entre las moléculas de agua causan la formación de una estructura rígida cuando el agua líquida se convierte en hielo sólido.
¿Qué es el enlace de hidrógeno intramolecular??
Los enlaces de hidrógeno intramoleculares son aquellos que ocurren dentro de una sola molécula.Este tipo de enlace de hidrógeno surge cuando dos grupos funcionales que son capaces de formar enlaces de hidrógeno entre sí están presentes en la misma molécula única. Esto significa que tanto el donante de electrones como el aceptador de electrones deben estar presentes en la misma molécula.
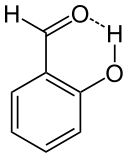
Figura 02: enlace de hidrógeno intramolecular en salicilaldehído
Además, estos dos grupos funcionales deben colocarse lo suficientemente cerca para este enlace de hidrógeno. El ejemplo más común de una molécula que muestra este tipo de enlace de hidrógeno es el salicilaldehído (c7H6O2).
¿Cuál es la diferencia entre el enlace de hidrógeno intermolecular e intramolecular??
Enlace de hidrógeno intramolecular intermolecular | |
| Los enlaces de hidrógeno intermoleculares se producen entre moléculas separadas en una sustancia. | Los enlaces de hidrógeno intramoleculares son los que ocurren dentro de una sola molécula. |
| Componentes | |
| Se forman enlaces de hidrógeno intermoleculares entre dos moléculas. | Se forman enlaces de hidrógeno intramoleculares entre las moléculas separadas. |
Resumen -Intermolecular Vs enlace de hidrógeno intramolecular
El enlace de hidrógeno es una forma de interacción dipolo-dipolo. Pero es un tipo de enlace débil. Hay dos formas de enlace de hidrógeno como enlaces de hidrógeno intermoleculares e intramoleculares. La diferencia entre el enlace de hidrógeno intermolecular e intramolecular es que el enlace de hidrógeno intermolecular ocurre entre dos moléculas, mientras que el enlace de hidrógeno intramolecular se produce en una sola molécula.
Referencia:
1."Enlaces de hidrógeno."Bibliotecas de química, Librettexts, 21 de julio de 2016. Disponible aquí
2."Enlace de hidrógeno."Wikipedia, Fundación Wikimedia, 14 mar. 2018. Disponible aquí
Imagen de cortesía:
1.'Hidrógeno Bonding-in-Water-2D' (dominio público) a través de Commons Wikimedia
2.'Salicylaldehyd Wasserstoffbrücke'by Neurotiker ⇌ - Trabajo propio, (dominio público) a través de Commons Wikimedia


