Diferencia entre el método de electrones de iones y el método de número de oxidación
El diferencia clave entre el método de electrones de iones y el método de número de oxidación es que, En el método de electrones de iones, la reacción se equilibra dependiendo de la carga de iones, mientras que, en el método de número de oxidación, la reacción se equilibra dependiendo del cambio en los números de oxidación de oxidantes y reductantes.
Tanto el método de electrones de iones como el método de número de oxidación son importantes para equilibrar las ecuaciones químicas. Se proporciona una ecuación química equilibrada para una reacción química particular y nos ayuda a determinar cuánto del reactante reaccionó para dar una cantidad particular del producto, o la cantidad de reactivos necesarios para obtener una cantidad deseada del producto.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el método de electrones de iones?
3. ¿Qué es el método de número de oxidación?
4. Comparación de lado a lado -Método de electrones de iones frente al método de número de oxidación en forma tabular
5. Resumen
¿Qué es el método de electrones de iones??
El método de electrones de iones es una técnica analítica que podemos usar para determinar la relación estequiométrica entre reactivos y productos, utilizando medias reacciones iónicas. Dada la ecuación química para una reacción química particular, podemos determinar las dos medias reacciones de la reacción química y equilibrar el número de electrones e iones en cada reacción mitad para obtener ecuaciones completamente equilibradas.

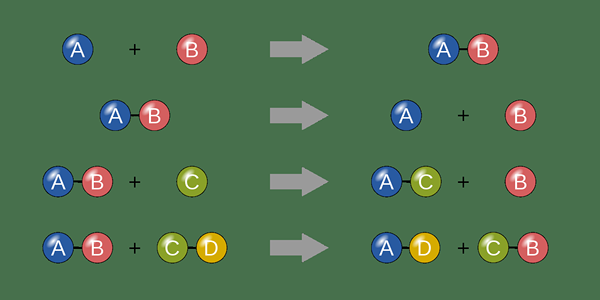
Figura 01: Reacciones químicas
Consideremos un ejemplo para comprender este método.
La reacción entre el ion permanganato y el ion ferroso es la siguiente:
Mno4- + Ceñudo2+ ⟶ MN2+ + Ceñudo3+ + 4h2O
Las dos medias reacciones son la conversión del ion permanganato en iones de manganeso (II) e ion ferroso en iones férricos. Las formas iónicas de estas dos medias reacciones son las siguientes:
Mno4- ⟶ Mn2+
Ceñudo2+ ⟶ Fe3+
A partir de entonces, tenemos que equilibrar el número de átomos de oxígeno en cada media reacción. En la media reacción donde el ferroso se convierte en iones férricos, no hay átomos de oxígeno. Por lo tanto, tenemos que equilibrar el oxígeno en la otra media reacción.
Mno4- ⟶ Mn2+ + 4o2-
Estos cuatro átomos de oxígeno provienen de la molécula de agua (no oxígeno molecular porque no hay producción de gas en esta reacción). Entonces la media reacción correcta es:
Mno4- ⟶ Mn2+ + 4h2O
En la ecuación anterior, no hay átomos de hidrógeno en el lado izquierdo, pero hay ocho átomos de hidrógeno en el lado derecho, por lo que tenemos que agregar ocho átomos de hidrógeno (en forma de iones de hidrógeno) al lado izquierdo.
Mno4- + 8h+ ⟶ Mn2+ + 4h2O
En la ecuación anterior, la carga iónica del lado izquierdo no es igual al lado derecho. Por lo tanto, podemos agregar electrones a uno de los dos lados para equilibrar la carga iónica. La carga en el lado izquierdo es +7 y en el lado derecho es +2. Aquí tenemos que agregar cinco electrones al lado izquierdo. Entonces la media reacción es,
Mno4- + 8h+ + 5e- ⟶ Mn2+ + 4h2O
Al equilibrar la medias reacción de la conversión ferrosa en iones férricos, la carga iónica se convierte de +2 a +3; Aquí necesitamos agregar un electrón al lado derecho de la siguiente manera para equilibrar la carga iónica.
Ceñudo2+ ⟶ Fe3+ + mi-
A partir de entonces, podemos agregar dos ecuaciones juntas equilibrando el número de electrones. Tenemos que multiplicar la media reacción con la conversión de ferroso en férrico por 5 para obtener cinco electrones y luego agregando esta ecuación de media reacción modificada a la medias reacción con la conversión de permanganato en iones de manganeso (ii), los cinco, los cinco Los electrones en cada lado cancelan. La siguiente reacción es el resultado de esta adición.
Mno4- + 8h+ + 5fe2+ + 5e- ⟶ Mn2+ + 4h2O + 5fe3+ + 5e-
Mno4- + 8h+ + 5fe2+ ⟶ Mn2+ + 4h2O + 5fe3+
¿Qué es el método de número de oxidación??
El método de número de oxidación es una técnica analítica que podemos usar para determinar la relación estequiométrica entre reactivos y productos, utilizando el cambio en la oxidación de elementos químicos cuando la reacción pasa de los reactivos a los productos. En una reacción redox, hay dos medias reacciones: reacción de oxidación y reacción de reducción. Para el mismo ejemplo que anteriormente, la reacción entre los iones permanganato y ferroso, la reacción de oxidación es la conversión de ferroso en iones férricos, mientras que la reacción de reducción es la conversión de iones de permanganato en iones de manganeso (ii).
Oxidación: Fe2+ ⟶ Fe3+
Reducción: MNO4- ⟶ Mn2+
Al equilibrar este tipo de reacción, primero debemos determinar el cambio en los estados de oxidación de los elementos químicos. En la reacción de oxidación, +2 de ion ferroso se convierte en +3 iones férricos. En la reacción de reducción, +7 de manganeso se convierte en +2. Por lo tanto, podemos equilibrar los estados de oxidación de estos multiplicando la medias reacción con el grado de incremento/disminución del estado de oxidación en la otra media reacción. En el ejemplo anterior, el cambio en el estado de oxidación para la reacción de oxidación es 1 y el cambio en el estado de oxidación para la reacción de reducción es 5. Luego, tenemos que multiplicar la reacción de oxidación con 5 y la reacción de reducción con 1.
5fe2+ ⟶ 5fe3+
Mno4- ⟶ Mn2+
A partir de entonces, podemos agregar estas dos medias reacciones para obtener la reacción completa y luego podemos equilibrar los otros elementos (átomos de oxígeno) usando moléculas de agua e iones de hidrógeno para equilibrar la carga iónica en ambos lados.
Mno4- + 8h+ + 5fe2+ ⟶ MN2+ + 4h2O + 5fe3+
¿Cuál es la diferencia entre el método de electrones de iones y el método de número de oxidación??
El método de electrones de iones y el método de número de oxidación son importantes para equilibrar las ecuaciones químicas. La diferencia clave entre el método de electrones de iones y el método de número de oxidación es que en el método de electrones de iones, la reacción se equilibra dependiendo de la carga de iones, mientras que, en el método de número de oxidación, la reacción se equilibra dependiendo del cambio en los números de oxidación de oxidantes y reductantes.
A continuación, la infografía resume la diferencia entre el método de electrones de iones y el método de número de oxidación.

Resumen -Método de electrones de iones versus método de número de oxidación
La diferencia clave entre el método de electrones de iones y el método de número de oxidación es que en el método de electrones de iones, la reacción se equilibra dependiendo de la carga de iones, mientras que, en el método de número de oxidación, la reacción se equilibra dependiendo del cambio en los números de oxidación de oxidantes y reductantes.
Referencia:
1. "Ecuaciones de equilibrio ." organizar, 17 de abril. 2017, disponible aquí.
Imagen de cortesía:
1. "Reacciones químicas" de Daniele Pugliesi - Trabajo propio (CC By -SA 3.0) a través de Commons Wikimedia


