Diferencia entre el sistema aislado y el sistema cerrado
El diferencia clave entre el sistema aislado y el sistema cerrado es que Los sistemas aislados no pueden intercambiar materia y energía con los alrededores, pero, aunque los sistemas cerrados tampoco pueden intercambiar materia con los alrededores, puede intercambiar la energía.
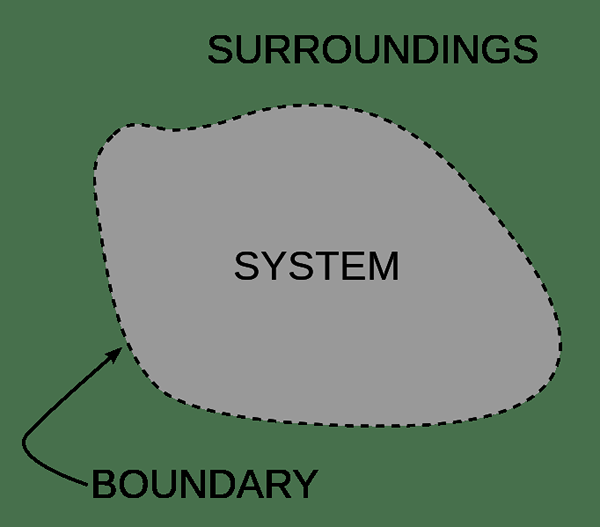
Para la facilidad de estudiar la química, dividimos el universo en dos partes. La parte que vamos a estudiar es el "sistema", y el resto es el "entorno". Por ejemplo, un sistema puede ser un organismo, un recipiente de reacción o incluso una sola célula. Hay un límite entre un sistema y los alrededores. El límite define el alcance del sistema. A veces, la materia y el intercambio de energía a través de estos límites. Además, podemos clasificar un sistema en dos categorías; son el sistema abierto y el sistema cerrado. Un sistema aislado es una forma de un sistema cerrado.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el sistema aislado?
3. ¿Qué es el sistema cerrado?
4. Comparación de lado a lado: sistema aislado frente al sistema cerrado en forma tabular
5. Resumen
¿Qué es el sistema aislado??
Un sistema aislado es una forma de un sistema cerrado. Pero, difiere de un sistema cerrado porque no tiene contacto mecánico ni térmico con sus alrededores. Eso significa; Los sistemas aislados no pueden intercambiar materia y energía con los alrededores. Además, estos sistemas alcanzan el equilibrio termodinámico con el tiempo, equilibrando la presión, la temperatura u otros parámetros.
Prácticamente, un sistema aislado no existe porque todas las cosas interactúan entre sí de ciertas maneras. Sin embargo, podemos considerar todo el universo como un sistema aislado, considerando que no hay transferencia de la materia y la energía fuera del universo. Teóricamente, esto es útil al construir modelos. Por ejemplo, las leyes termodinámicas de primera y segunda describen un sistema aislado.
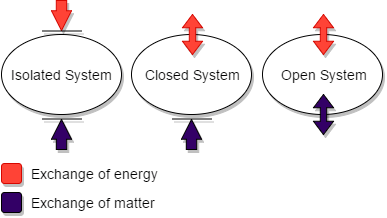
Figura 01: Comparación del sistema aislado con sistemas abiertos y cerrados
El Primera ley de la termodinámica establece que la "energía interna de un sistema aislado es constante." El Segunda ley de la termodinámica dice que "la entropía de un sistema aislado aumenta en el curso de un proceso espontáneo."Sin embargo, esta ley solo es cierta para los sistemas aislados. La entropía aumentará con el tiempo en un sistema aislado y alcanzará el valor máximo en el equilibrio. En resumen, la energía general de estos sistemas nunca puede aumentar. Por lo tanto, la entropía nunca puede disminuir.
¿Qué es el sistema cerrado??
En un sistema cerrado, la materia no puede pasar a través del límite. Por lo tanto, la materia dentro de un sistema cerrado es siempre el mismo. Sin embargo, en este tipo de sistema, los intercambios de energía con los alrededores. Por ejemplo, cuando ocurre una reacción, el sistema puede expandirse, o puede transferir la energía al entorno si está a una temperatura más baja.

Figura 02: un sistema y su entorno separados por un límite
Ej: Si cubrimos la parte superior de una taza de té cálida con tapa, entonces se convierte en un sistema cerrado. Allí, el vapor no puede escapar del sistema. Además, las moléculas de gas en el entorno no pueden ingresar al sistema. Por lo tanto, no hay intercambio de materia. Sin embargo, el calor del té intercambia con los alrededores. Podemos sentir el calor si tocamos la tapa de la taza. Por lo tanto, la energía sale como energía térmica. Allí, el sistema alcanza un equilibrio con los alrededores cuando la temperatura dentro y fuera del sistema se vuelve igual.
¿Cuál es la diferencia entre el sistema aislado y el sistema cerrado??
Un límite separa un sistema y sus alrededores. Podemos nombrar un sistema como un sistema abierto o cerrado dependiendo del intercambio de materia y energía a través de este límite. Un sistema aislado también es una forma de un sistema cerrado. La diferencia clave entre el sistema aislado y el sistema cerrado es que los sistemas aislados no pueden cambiar tanto la materia como la energía con los alrededores, pero, aunque los sistemas cerrados no pueden intercambiar materia con los alrededores, puede intercambiar la energía.
Como otra diferencia importante entre el sistema aislado y el sistema cerrado, podemos decir que la entropía de un sistema aislado nunca puede disminuir, mientras que la entropía de un sistema cerrado puede disminuir. Además, los sistemas aislados son teóricos; Eso significa que estos sistemas no existen en la realidad. Sin embargo, existen sistemas cerrados en la realidad.
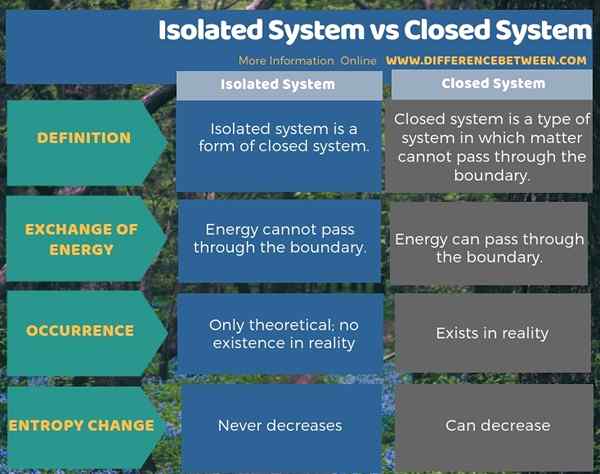
Resumen: sistema aislado frente al sistema cerrado
Los sistemas son de dos tipos; son el sistema abierto y el sistema cerrado. Los sistemas aislados también son un tipo de sistema cerrado. Sin embargo, hay pocas diferencias entre ellos. La diferencia clave entre el sistema aislado y el sistema cerrado es que los sistemas aislados no pueden cambiar tanto la materia como la energía con los alrededores, pero, aunque los sistemas cerrados tampoco pueden intercambiar materia con los alrededores, puede intercambiar la energía.
Referencia:
1. Helmenstine, Anne Marie, PH.D. “Definición del sistema cerrado (ciencia)."Thinkco, junio. 22, 2018. Disponible aquí
2. Helmenstine, Anne Marie, PH.D. "Definición del sistema aislada."Thinkco, Jul. 12, 2017. Disponible aquí
Imagen de cortesía:
1."Sistemas de diagrama" de ALKH.Alwa - Trabajo propio, (CC By -SA 4.0) a través de Commons Wikimedia
2."Límite del sistema" de Wavesmikey, (dominio público) a través de Commons Wikimedia


