Diferencia entre enlaces químicos localizados y delocalizados
El diferencia clave entre los enlaces químicos localizados y delocalizados que el enlace químico localizado es un enlace específico o un par de electrones solitario en un átomo específico, mientras que el enlace químico delocalizado es un enlace específico que no está asociado con un solo átomo o un enlace covalente.
Un enlace químico es una conexión entre dos átomos. Esta conexión ocurre debido a la superposición de los orbitales moleculares. Hay dos formas principales de enlaces como enlaces químicos localizados y delocalizados. Los enlaces químicos localizados son las superposiciones orbitales moleculares normales, como los enlaces sigma y los enlaces PI. Sin embargo, los enlaces químicos delocalizados son diferentes. Estos enlaces se forman cuando varios enlaces localizados se mezclan entre sí. Más detalles están a continuación.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Cuáles son los enlaces químicos localizados?
3. ¿Qué son los enlaces químicos delocalizados?
4. Comparación lado a lado: enlaces químicos localizados vs delocalizados en forma tabular
5. Resumen
¿Cuáles son los enlaces químicos localizados??
Los enlaces químicos localizados son enlaces Sigma y PI normales o pares de electrones solitarios que existen en un solo átomo. Estos enlaces se concentran en una región limitada de una molécula. Estas regiones tienen una distribución de electrones concentrados. En otras palabras, la densidad de electrones de esta región es muy alta.

Figura 01: un enlace Sigma: un enlace químico localizado
Un enlace localizado se forma cuando dos orbitales moleculares de dos átomos separados se superponen entre sí. Los enlaces sigma pueden formarse debido a la superposición de dos orbitales S, dos orbitales P o superposición de S-P.
¿Qué son los enlaces químicos delocalizados??
Los enlaces químicos delocalizados son los enlaces químicos que no se asocian con un solo átomo sino con varios átomos u otros enlaces químicos. Llamamos a los electrones en estos enlaces como 'electrones delocalizados'. La deslocalización ocurre en el sistema PI conjugado. Un sistema PI conjugado tiene dobles enlaces y enlaces únicos en un patrón alterno.
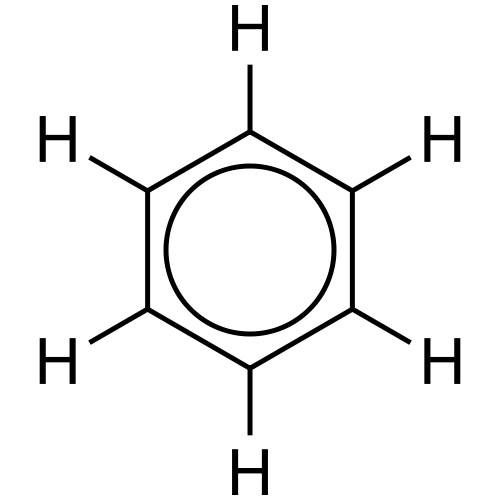
Figura 02: Deslocalización de electrones
Por ejemplo, el anillo de benceno tiene tres enlaces individuales y tres enlaces dobles en un patrón alterno. Cada átomo de carbono en este anillo tiene un orbital P que no se superpone frontal. Por lo tanto, estos orbitales P pueden tener superposición lateral. Este tipo de superposición es la delocalización. Podemos indicar esto como dos círculos en la parte superior del anillo de benceno y la parte inferior del anillo. Estos electrones son libres de moverse a lo largo de la molécula porque no tienen una unión permanente a un solo átomo o un enlace covalente.
¿Cuál es la diferencia entre los enlaces químicos localizados y delocalizados??
Los enlaces químicos localizados son enlaces Sigma y PI normales o pares de electrones solitarios que existe en un solo átomo. Estos enlaces se forman debido a la superposición frontal entre los orbitales S, los orbitales P o los orbitales S y P. Además, estos electrones se limitan a una región particular entre dos átomos separados. Los enlaces químicos delocalizados son los enlaces químicos que no se asocian con un solo átomo sino con varios átomos u otros enlaces químicos. Estos enlaces tienen electrones extendidos por la molécula que son libres de moverse. Estos enlaces se forman debido a la superposición lateral de los orbitales P. Esta es la principal diferencia entre los enlaces químicos localizados y delocalizados.
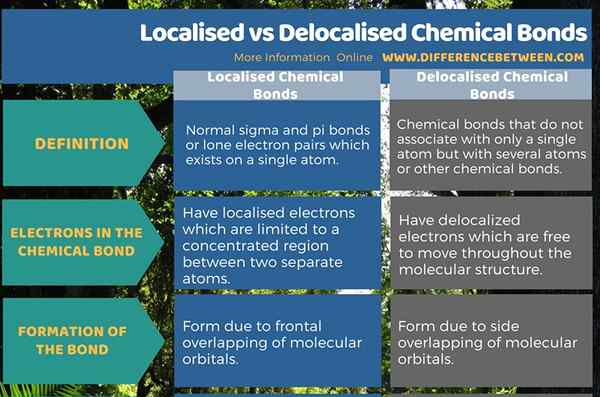
Resumen: enlaces químicos localizados vs delocalizados
Un enlace químico es una conexión entre dos átomos. Hay dos formas de enlaces químicos como enlaces químicos localizados y delocalizados. La diferencia entre los enlaces químicos localizados y delocalizados es que un enlace químico localizado es un enlace específico o un par solitario de electrones en un átomo específico, mientras que un enlace químico delocalizado es un enlace específico que no está asociado con un solo átomo o un enlace covalente.
Referencia:
1. Bibliotecas. "Deslocalización de electrones."Bibliotecas de química, Librettexts, 20 DEC. 2016. Disponible aquí
2. "Orbitales moleculares localizados."Wikipedia, Fundación Wikimedia, 19 de junio de 2018. Disponible aquí
Imagen de cortesía:
1.'Sigma Bond'by SVG: Zoofari; Raster: Anselmo H. C. Horn (CC By-SA 3.0) a través de Commons Wikimedia
2.'Benceno-6H-Delocalizado' por un trabajo propio de élite, (CC By-SA 3.0) a través de Commons Wikimedia


