Diferencia entre electrones localizados y delocalizados
El diferencia clave entre los electrones localizados y delocalizados es que Los electrones localizados se encuentran entre los átomos, mientras que los electrones delocalizados se encuentran por encima y por debajo de los átomos.
En química general, los electrones localizados y los electrones delocalizados son términos que describen estructuras químicas de los compuestos químicos. Los electrones localizados son los electrones de unión en las moléculas, mientras que los electrones delocalizados son electrones no de combinación que ocurren como nubes de electrones por encima y por debajo de la molécula.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué son los electrones localizados?
3. ¿Qué son los electrones delocalizados?
4. Comparación lado a lado: electrones delocalizados localizados vs en forma tabular
5. Resumen
¿Qué son los electrones localizados??
Los electrones localizados son los electrones de unión en compuestos químicos. Estos electrones se encuentran entre átomos donde se pueden encontrar enlaces sigma. Los enlaces sigma son los enlaces formados por la superposición axial de los orbitales atómicos medio llenos de átomos.
Por lo tanto, los electrones localizados ocurren en compuestos covalentes que tienen enlaces químicos covalentes. Estos electrones localizados pertenecen a dos átomos particulares, en contraste con los electrones delocalizados, que son comunes a todos los átomos en la molécula. Los electrones localizados se comparten entre átomos que forman enlaces covalentes, enlaces de coordinación, etc.
¿Qué son los electrones delocalizados??
Los electrones delocalizados son los electrones que no son de filo en los compuestos químicos. Este término se refiere a electrones que no están asociados con un solo átomo o un enlace covalente. Sin embargo, el término electrón delocalizado tiene diferentes significados en diferentes campos. Por ejemplo, en la química orgánica, los electrones delocalizados están en las estructuras de resonancia de los sistemas conjugados en compuestos aromáticos. En física en estado sólido, los electrones delocalizados son los electrones libres que facilitan la conducción eléctrica. Además, la física cuántica usa el término electrones delocalizados para referirse a electrones orbitales moleculares que se han extendido sobre varios átomos.

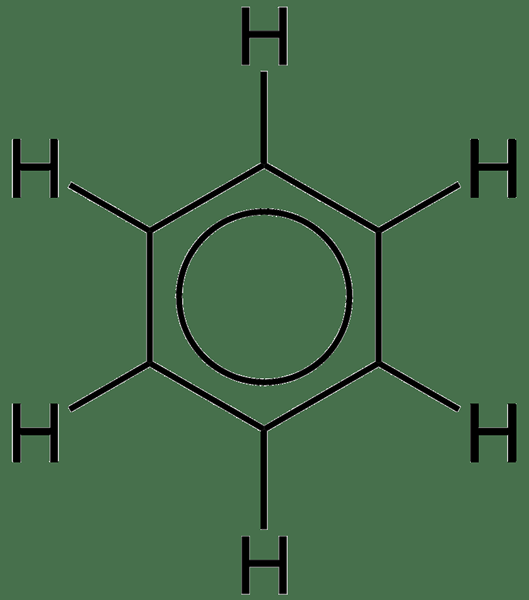
Figura 01: Benceno, (la delocalización de los electrones está indicada por el círculo)
El anillo de benceno es el ejemplo más simple de un sistema aromático que tiene electrones delocalizados. Hay seis electrones PI en la molécula de benceno; a menudo indicamos estos usando gráficamente un círculo. Este círculo significa que los electrones PI están asociados con todos los átomos en la molécula. Esta delocalización hace que el anillo de benceno tenga enlaces químicos con longitudes de enlace similares.
¿Cuál es la diferencia entre los electrones localizados y delocalizados??
Utilizamos los términos electrones localizados y delocalizados bajo la rama de la química general, con respecto a la estructura química de los compuestos. Un átomo localizado es un electrón que pertenece a un átomo particular, mientras que un electrón delocalizado es un electrón no asociado con un solo átomo o un solo enlace covalente. La diferencia clave entre los electrones localizados y delocalizados es que los electrones localizados se encuentran entre los átomos, mientras que los electrones delocalizados están ubicados por encima y por debajo de los átomos. En otras palabras, los electrones localizados se limitan a una región particular entre dos átomos, mientras que los electrones delocalizados se extienden sobre varios átomos.
Además, otra diferencia significativa entre los electrones localizados y delocalizados es que los electrones localizados están asociados con átomos particulares en un compuesto, mientras que los electrones delocalizados están asociados con todos los átomos en la molécula. Además, los electrones localizados se indican gráficamente mediante líneas rectas, mientras que los electrones delocalizados se indican gráficamente por círculos.
La siguiente tabla resume las diferencias entre los electrones localizados y delocalizados.

Resumen: electrón localizado y delocalizado
Los términos electrones localizados y delocalizados se discuten bajo la química general. La diferencia clave entre los electrones localizados y delocalizados es que los electrones localizados se encuentran entre los átomos, mientras que los electrones delocalizados están ubicados por encima y por debajo de los átomos. Además, los electrones delocalizados están asociados con átomos particulares en un compuesto, mientras que los electrones delocalizados están asociados con todos los átomos en la molécula.
Referencia:
1. "Pares y enlaces solitarios localizados y delocalizados." Pasos de química, 22 de agosto. 2020, disponible aquí.
2. "Electrón delocalizado."Wikipedia, Fundación Wikimedia, 13 de julio de 2020, disponible aquí.
Imagen de cortesía:
1. "Benz4" por SelfMade by Cacycle, Leyo - Trabajo propio (CC By -Sa 3.0) a través de Commons Wikimedia


