Diferencia entre cloruro de magnesio y sulfato de magnesio

El diferencia clave entre el cloruro de magnesio y el sulfato de magnesio es que La molécula de cloruro de magnesio tiene un catión de magnesio asociado con dos aniones de cloruro, mientras que la molécula de sulfato de magnesio tiene un catión de magnesio asociado con un anión sulfato.
El magnesio es un metal de tierra alcalino que puede formar un catión estable divalente. Este catión puede formar muchos compuestos iónicos como el cloruro de magnesio y el sulfato de magnesio. Ambos son compuestos sólidos a temperatura ambiente que pueden existir en diferentes formas hidratadas. Este artículo analiza más detalles sobre estos dos compuestos y otras diferencias entre ellos.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el cloruro de magnesio?
3. ¿Qué es el sulfato de magnesio?
4. Comparación de lado a lado: cloruro de magnesio frente a sulfato de magnesio en forma tabular
5. Resumen
¿Qué es el cloruro de magnesio??
El cloruro de magnesio es un compuesto inorgánico que tiene la fórmula química MGCL2. Puede existir en varias formas de hidrato. Estos compuestos son haluros iónicos y son altamente solubles en agua. Podemos obtener las formas hidratadas del agua de mar a través de diferentes extracciones. La masa molar de la forma anhidra es 95.211 g/mol. Es un sólido cristalino blanco a blanco a incoloro.

Figura 01: Cristales de cloruro de magnesio
El punto de fusión de esto es 714 ° C, y el punto de ebullición es de 1412 ° C. La cristalización de este compuesto se asemeja a la cristalización del cloruro de cadmio. Tiene centros de mg octaédricos. Los hidratos más comunes incluyen cloruro de magnesio asociado con 2, 4, 6, 8 y 12 moléculas de agua.
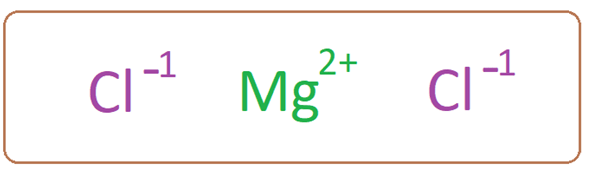
El cloruro de magnesio tiene un catión de magnesio asociado con dos aniones de cloruro
Podemos producir este compuesto a través del proceso Dow en el que el hidróxido de magnesio se trata con ácido HCl para obtener cloruro de magnesio y agua.
Mg (oh)2 + HCL → MGCL2 + H2O
Las aplicaciones de este compuesto incluyen la producción de metal de magnesio a través de la electrólisis, control de polvo, estabilización del suelo, como soporte de catalizador para el catalizador Ziegler-Natta, etc.
¿Qué es el sulfato de magnesio??
El sulfato de magnesio es un compuesto inorgánico que tiene la fórmula química MGSO4. Es una sal de magnesio y también puede existir en varias formas hidratadas. La masa molar de la forma anhidra es 120.36 g/mol. Aparece como un sólido cristalino blanco a temperatura ambiente. Este complejo es inodoro. No tiene punto de fusión. En cambio, se descompone a 1124 ° C.

Figura 02: sulfato de magnesio anhidro
A diferencia del sulfato de magnesio, este compuesto no es tanta agua soluble. Las formas hidratadas incluyen sulfato de magnesio asociado con moléculas de agua 1, 4, 5, 6 y 7.
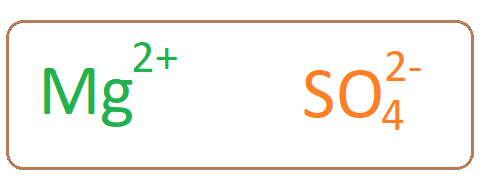
La molécula de sulfato de magnesio tiene un catión de magnesio asociado con un anión sulfato
Las aplicaciones de este compuesto están en el campo de la medicina como mineral para la producción farmacéutica de magnesio, la pasta de este compuesto es útil para tratar las inflamaciones de la piel, etc. Además, es útil en la agricultura aumentar los niveles de magnesio y azufre en el suelo.
¿Cuál es la diferencia entre cloruro de magnesio y sulfato de magnesio??
Teniendo en cuenta la estructura molecular de ambos, la molécula de cloruro de magnesio tiene un catión de magnesio asociado con dos aniones de cloruro, mientras que la molécula de sulfato de magnesio tiene un catión de magnesio asociado con un anión sulfato. Esta es la diferencia clave entre el cloruro de magnesio y el sulfato de magnesio.
Además, el cloruro de magnesio es un compuesto inorgánico que tiene la fórmula química MGCL2. La masa molar de la forma anhidra es 95.211 g/mol. Además, los hidratos más comunes incluyen cloruro de magnesio asociado con 2, 4, 6, 8 y 12 moléculas de agua. El sulfato de magnesio es un compuesto inorgánico que tiene la fórmula química MGSO4. La masa molar de la forma anhidra es 120.36 g/mol. Además, las formas hidratadas comunes incluyen sulfato de magnesio asociado con moléculas de agua 1, 4, 5, 6 y 7.
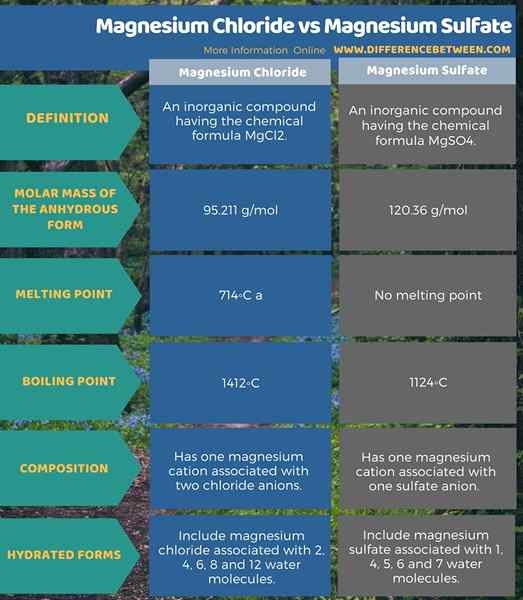
Resumen -cloruro de magnesio vs sulfato de magnesio
El magnesio es un elemento químico del Grupo 2 que puede formar cationes estables y divalentes que son capaces de formar compuestos iónicos. El cloruro de magnesio es un haluro iónico, y el sulfato de magnesio es una sal de magnesio. La diferencia entre el cloruro de magnesio y el sulfato de magnesio es que la molécula de cloruro de magnesio tiene un catión de magnesio asociado con dos aniones de cloruro, mientras que la molécula de sulfato de magnesio tiene un catión de magnesio asociado con un anionario de sulfato.
Referencia:
1. "Cloruro de magnesio."Wikipedia, Fundación Wikimedia, 19 de junio de 2018.Disponible aquí
2. "Sulfato de magnesio."Wikipedia, Fundación Wikimedia, 19 de junio de 2018. Disponible aquí
Imagen de cortesía:
1.'Cloruro de magnesio' (dominio público) a través de Commons Wikimedia
2.'Sulfato de magnesio anhidro' (dominio público) a través de Commons Wikimedia


