Diferencia entre la ruta libre media y la presión
Diferencia clave: ruta libre media versus presión
La ruta libre media es la distancia promedio recorrida por una molécula en movimiento mientras choca con otras moléculas. Por lo tanto, se mide por unidades de medición de longitud. La ruta libre media se determina utilizando la velocidad promedio de una molécula, y la frecuencia de colisión desde que determinar la ruta libre media usando las distancias es difícil. La presión es un término científico que a menudo se usa. Es la fuerza perpendicular aplicada en un área de superficie de la unidad. La diferencia clave entre la ruta libre y la presión media es que El camino libre medio es medido como una distancia en metros, mientras que la presión se mide por la unidad de SI Pascals (PA).
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es un camino libre?
3. Que es la presión
4. Comparación de lado a lado: ruta libre media frente a presión en forma tabular
6. Resumen
¿Qué es un camino libre??
La ruta libre media es la distancia promedio recorrida por una partícula móvil (un átomo, molécula o ion) entre colisiones (impactos sucesivos). Estas colisiones modifican la dirección o energía de las partículas en movimiento. Este término se llama ruta libre media porque se calcula como un valor promedio. La ruta libre media se puede estimar utilizando la teoría cinética. La teoría cinética establece que las moléculas de gas están en movimiento aleatorio constante con colisiones frecuentes entre sí. La ruta libre media se denota por el símbolo "λ". Consideremos un ejemplo para comprender qué es la ruta libre.

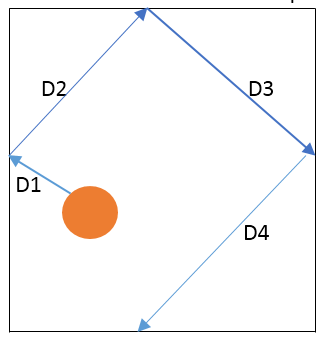
Figura 1: movimiento de una molécula de gas con colisiones entre la molécula de gas y la pared del contenedor.
Cálculo medio de ruta libre
La ruta libre media de la molécula de gas en la imagen de arriba se da como se muestra a continuación.
λ = (D1 + D2 + D3 + D4) /4
Sin embargo, este tipo de cálculo no es posible porque las distancias entre cada colisión no se pueden determinar fácilmente. Por lo tanto, la ruta libre media se calcula de la siguiente manera.
λ = c / z
Aquí, c es la velocidad promedio de una molécula de gas y z es la frecuencia de colisión. La frecuencia de colisión es la velocidad a la que dos moléculas chocan entre sí. Por lo tanto, es igual a 1/t (t es el tiempo promedio entre colisiones). Entonces la ecuación anterior se puede reorganizar de la siguiente manera.
λ = c / (1 / t)
λ = c t
Que es la presión?
La presión es un término científico utilizado para nombrar la fuerza aplicada perpendicular a un área de superficie de la unidad. Cuando se considera un fluido, la presión es la tensión en un punto dentro de un fluido. La unidad SI de medir la presión es Pascal (PA). La presión se denota por el símbolo "P". Sin embargo, hay algunas unidades comunes utilizadas para medir la presión. Ej: N/M2 (Newton por metro cuadrado), PSI (la fuerza de libra por pulgada cuadrada), cajero automático (atmósfera), 1/760 de cajero automático se nombra como un torr.
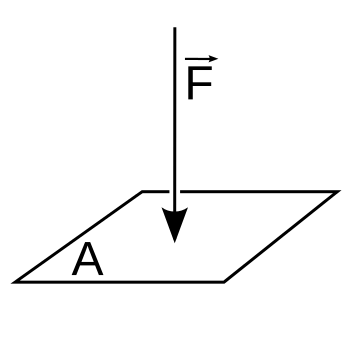
Figura 2: La presión es la fuerza perpendicular aplicada en una superficie dividida por el área de superficie en la que se ejerce la fuerza.
Ecuación para el cálculo de la presión
La presión se puede calcular utilizando la siguiente ecuación:
P = - (f/a)
Donde p es la presión, F es la magnitud de la fuerza se aplica en un área de un. Hay varios tipos de presión.
- Presión fluida - la fuerza de compresión en un punto dentro de un fluido.
- Presión de explosión - La presión resultó por el encendido de gases explosivos.
- Presión negativa - Hay ciertas condiciones en las que la presión se vuelve negativa. Ej: Cuando las fuerzas intermoleculares entre las moléculas de fluido exceden las fuerzas repulsivas (que se crea debido al movimiento térmico).
- Presión de un gas ideal - La presión de un gas ideal se calcula usando p = nrt/v (en el que p es la presión, n es la cantidad de sustancia, r es la constante de gas universal, v es el volumen y t es la temperatura del gas).
- Presión de vapor - La presión del vapor que está en contacto con su fase líquida en un sistema termodinámico cerrado.
¿Cuál es la diferencia entre la ruta libre y la presión??
Ruta libre media frente a presión | |
| La ruta libre media es la distancia promedio recorrida por una partícula móvil (un átomo, molécula o ion) entre colisiones (impactos sucesivos). | La presión es un término científico utilizado para nombrar la fuerza aplicada perpendicular a un área de superficie de la unidad. |
| Unidad de medida | |
| La ruta libre media se mide como una distancia en metros (a menudo se usa como micrómetros - μm). | La presión se mide por la unidad SI Pascals (PA). |
| Teoría | |
| El camino libre medio es la distancia recorrida por una partícula en movimiento. | La presión es la fuerza aplicada en un área unitaria (perpendicularmente). |
Resumen: ruta libre media versus presión
La ruta libre media es el promedio de distancias recorridas por una molécula entre colisiones durante el movimiento. La presión es la fuerza aplicada en una superficie de la unidad en una dirección perpendicular. La diferencia clave entre la ruta libre y la presión media es que la ruta libre media se mide como una distancia en metros, mientras que la presión se mide por la unidad SI Pascals (PA).
Referencia:
1. "Camino libre medio."Bibliotecas de química, Librettexts, 21 de julio de 2016, disponible aquí.
2. "Camino libre medio."Wikipedia, Fundación Wikimedia, 28 de febrero. 2018, disponible aquí.
3. "Camino libre medio."Media ruta libre, colisiones moleculares, disponibles aquí.
Imagen de cortesía:
1."Área de fuerza a presión" del Klaus-Dieter Keller-Trabajo propio (CC BY-SA 3.0) a través de Commons Wikimedia


