Diferencia entre metano y propano
Metano vs propano
El metano y el propano son los primeros y terceros miembros de la familia Alkane. Sus fórmulas moleculares son CH4 y C3H8 respectivamente. El diferencia clave entre metano y propano es su estructura química; El metano contiene solo un átomo de carbono y cuatro átomos de hidrógeno, mientras que el propano contiene tres átomos de carbono con ocho átomos de hidrógeno. Sus propiedades químicas y físicas varían debido a esta diferencia.
Que es metano?
Metano, también conocido como carbano, gas natural, gas pantanino, tetrahidruro de carbono, o carburo de hidrógeno, es el miembro más pequeño de la familia Alkane. Su fórmula química es CH4 (Cuatro átomos de hidrógeno se unen a un átomo de carbono). Es un componente importante del gas natural. El metano es un gas incoloro, inodoro e insípido. Se puede encender fácilmente ya que su vapor es más ligero que el aire.
El metano se puede encontrar naturalmente debajo del suelo y debajo del fondo del mar. El metano atmosférico se considera un gas de efecto invernadero. El metano se descompone en CH3- con agua en la atmósfera.
Que es el propano?
El propano es el tercer miembro de la familia Alkane. Su fórmula molecular es c3H6, y la masa molecular es igual a 44.10 g · mol−1. Existe como un gas a temperatura y presión estándar, pero puede comprimir en un líquido transportable. El propano no existe naturalmente, pero se obtiene del proceso de refinación de petróleo y como un subproducto del procesamiento de gas natural.
El propano es una sustancia gaseosa incolora, inodoro, no tóxica y inflamable y se agrega un olor comercial para la identificación de fugas.
¿Cuál es la diferencia entre metano y propano??
Características de metano y propano
Estructura molecular:
Metano: La fórmula molecular del metano es CH4, y es un ejemplo de una molécula tetraédrica con cuatro enlaces C-H equivalentes (enlaces sigma). Su estructura se da a continuación.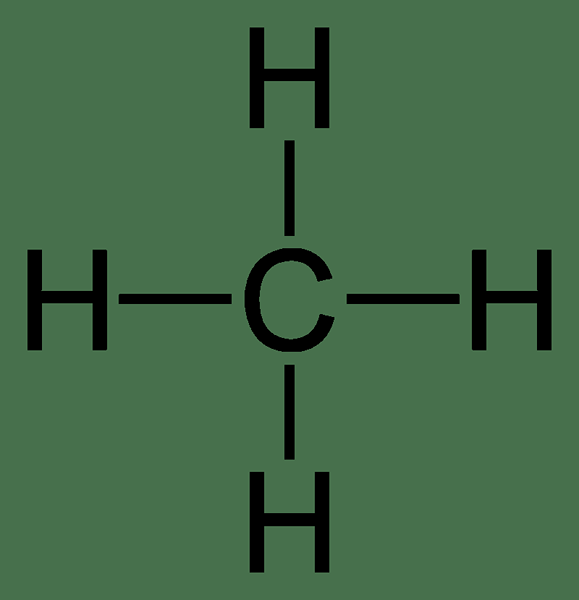
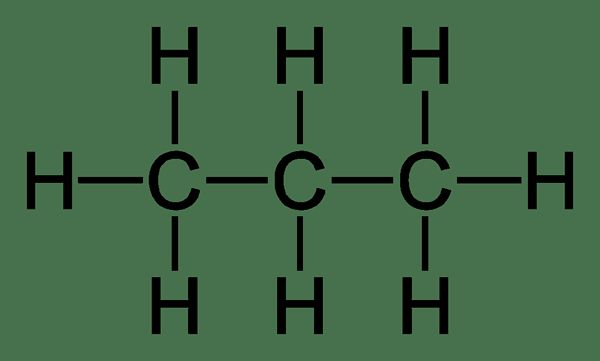
Propano: La fórmula molecular del etano es c3H8, y su estructura se da a continuación.
Propiedades químicas:
Combustión:
Metano: El metano arde con una llama no luminosa de color azul pálido que produce dióxido de carbono y agua en presencia de exceso de aire u oxígeno. Es una reacción altamente exotérmica; Por lo tanto, es un excelente combustible.
Pez4(g) +2o2 → CO2 + 2h2O +890 kJ/mol
Se quema parcialmente en gas de monóxido de carbono (CO) en presencia de aire u oxígeno insuficiente.
2ch4(g) +3o2 → 2CO +2H2O +Energía
Propano: El propano también se quema de manera similar a los otros alcanos. Se quema por completo en presencia de exceso de oxígeno que produce agua y dióxido de carbono.
C3H8 + 5O2 → 3Co2 + 4h2O +2220 kJ/mol
En ausencia de oxígeno suficiente para el proceso de combustión, se quema incompletamente en monóxido de carbono y/o carbono de hollín.
2 C3H8 + 9O2 → 4Co2 + 2CO +8H2O +calor
O
C3H8 + 9O2 → 3C + 4h2O +calor
La combustión de propano es mucho más limpia que la combustión de la gasolina, pero no tan limpia como la del gas natural.
Reacciones:
Metano: El metano muestra reacciones de sustitución con halógenos. En estas reacciones, uno o más átomos de hidrógeno se reemplazan por un número igual de átomos de halógeno y se llama "halogenación."Reacciona con cloro (CL) y bromo (BR) en presencia de la luz solar.
Cuando se pasa una mezcla de metano y vapor a través de un níquel calentado (1000 K) soportado en la superficie de alúmina, puede producir hidrógeno.
Propano: El propano también muestra reacciones de halogenación en condiciones especiales que producen diferentes productos en varias proporciones.
Pez3-Pez2-Pez3 + CL2 → Pez3-Pez2-Pez2CL (45%) + CH3-Chcl-ch3 (55%)
Pez3-Pez2-Pez3 + BR2 → Pez3-Pez2-Pez2Br (3%) + CH3-CHBR-CH3 (97%)
Usos de metano y propano
Metano: El metano se usa en muchos procesos químicos industriales (como combustible, gas natural, gas natural licuado) y se transporta como un fluido refrigerado.
Propano: El propano generalmente se usa como combustible en motores, hornos, estufas portátiles, antorchas de gas oxi, calentadores de agua, secadores de lavandería y calefacción en casas. Es uno de los gases de petróleo licuados como butano, propileno y butileno.
Definiciones:
Reacción exotérmica: una reacción exotérmica es una reacción química que libera energía por luz o calor.
Reacciones de sustitución: la reacción de sustitución es una reacción química que implica el desplazamiento de un grupo funcional en un compuesto químico y lo reemplazó con otro grupo funcional.
Referencias: “Reacción del propano con oxígeno!"THECOLT84" Reacciones de los alquenos "Imagen de la Universidad Estatal de Michigan cortesía:" Propano "de Holger87 - Trabajo propio (CC By -SA 3.0) a través de Commons Wikimedia "metano" (dominio público) a través de Commons Wikimedia

