Diferencia entre el ácido nítrico y el ácido nitroso
El diferencia clave entre el ácido nítrico y el ácido nitroso es que La molécula de ácido nítrico contiene tres átomos de oxígeno unidos a un átomo de nitrógeno central, mientras que la molécula de ácido nitroso contiene dos átomos de oxígeno unidos a un átomo de nitrógeno central.
Los ácidos nítricos y nitrosos son ácidos inorgánicos de nitrógeno. Ambos ácidos contienen átomos de nitrógeno, oxígeno e hidrógeno.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el ácido nítrico?
3. ¿Qué es el ácido nitroso?
4. Comparación de lado a lado: ácido nítrico versus ácido nitroso en forma tabular
5. Resumen
¿Qué es el ácido nítrico??
El ácido nítrico tiene la fórmula química HNO3. Es un ácido muy corrosivo y peligroso. Además, puede tener una naturaleza química diluida o concentrada. De cualquier manera, tiene moléculas de ácido nítrico disuelto en agua. La reacción entre el dióxido de nitrógeno y el agua forma ácido nítrico. Hay dos tipos de ácido nítrico: ácido nítrico fumante y ácido nítrico concentrado.
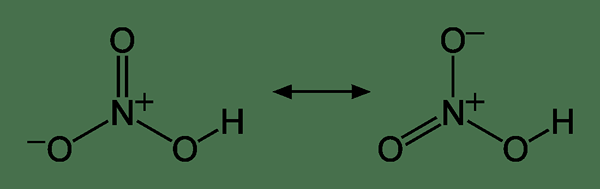
Figura 01: Estructuras de resonancia de la molécula de ácido nítrico
El ácido nítrico de humo es un grado comercial de ácido nítrico que tiene una concentración muy alta y una alta densidad. Contiene 90-99% HNO3. Podemos preparar este líquido agregando dióxido de nitrógeno excesivo al ácido nítrico. Forma un líquido fuming incoloro, amarillento o parduzco que es altamente corrosivo. Por lo tanto, esta solución ácida tiene moléculas gaseosas en combinación con el agua; No hay agua en él. El humo de este ácido se eleva de la superficie del ácido; Esto lleva a su nombre, "Fuming". La fórmula química de este compuesto es HNO3-xNO2.
El ácido nítrico concentrado es simplemente una solución que contiene más ácido nítrico en menos agua. Eso significa que la forma concentrada de este ácido contiene una menor cantidad de agua en comparación con la cantidad de solutos en él. En escala comercial, el 68% o más se considera como ácido nítrico concentrado. Además, la densidad de esta solución es 1.35 g/cm3. Esta gran concentración no produce humos, pero la concentración muy alta de este ácido puede dar humos de color blanco. Podemos producir este líquido reaccionando con dióxido de nitrógeno con agua.
¿Qué es el ácido nitroso??
El ácido nitroso es un ácido inorgánico que tiene la fórmula química HNO2. Es un ácido débil y un ácido monoprótico. Este ácido ocurre en el estado de la solución, en la fase gaseosa y en forma de sal de nitrilo. Este ácido es útil para hacer sales de diazonio que son reactivos en las reacciones de acoplamiento de azo.

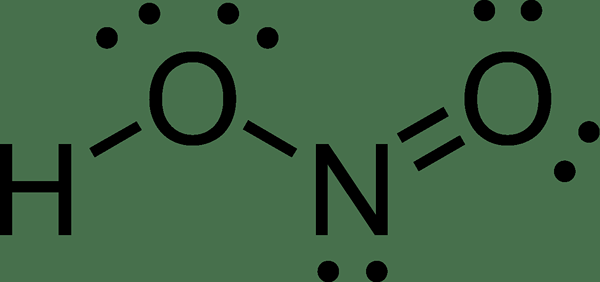
Figura 02: Estructura del ácido nitroso
Las soluciones de ácido nitroso aparecen en color azul pálido. La base conjugada de este ácido es el ion nitrilo. En su fase gaseosa, el ácido nitroso está en la geometría plana, y puede adoptar tanto las formas cis como las trans. El isómero trans predomina a temperatura ambiente, y es estable que el isómero cis.
El ácido nitroso se puede preparar mediante la acidificación de soluciones acuosas de nitrito de sodio con un ácido mineral. Podemos llevar a cabo el proceso de acidificación a temperaturas del hielo, y el HNO2 se consume en condiciones in situ. Las moléculas de ácido nitroso libre son inestables y tienden a descomponerse rápidamente. Además, podemos producir ácido nitroso a través de la disolución del trióxido de dinitrógeno en agua.
¿Cuál es la diferencia entre el ácido nítrico y el ácido nitroso??
El ácido nítrico y el ácido nitroso son ácidos inorgánicos que contienen átomos de nitrógeno. La diferencia clave entre el ácido nítrico y el ácido nitroso es que la molécula de ácido nítrico contiene tres átomos de oxígeno unidos a un átomo de nitrógeno central, mientras que la molécula de ácido nitroso contiene dos átomos de oxígeno unidos a un átomo de nitrógeno central.
Además, una diferencia fácilmente identificable entre el ácido nítrico y el ácido nitroso es que el ácido nítrico es un líquido incoloro, de color amarillo pálido o rojo, mientras que el ácido nitroso es una solución de color azul pálido. Además de eso, el ácido nítrico es un ácido fuerte que el ácido nitroso.
La infografía a continuación tabula las diferencias entre el ácido nítrico y el ácido nitroso.
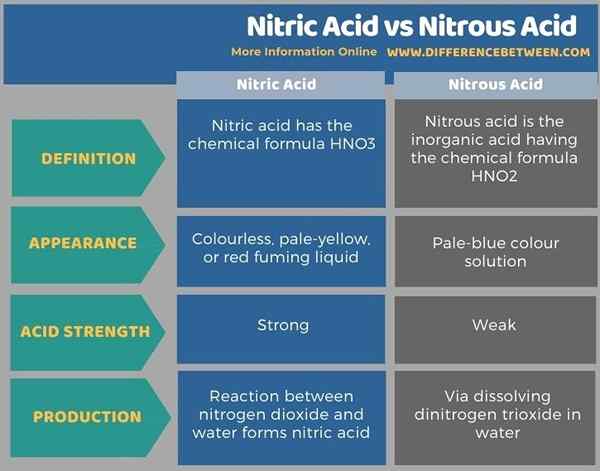
Resumen -ácido nítrico versus ácido nitroso
El ácido nítrico y el ácido nitroso son ácidos inorgánicos que contienen átomos de nitrógeno. La diferencia clave entre el ácido nítrico y el ácido nitroso es que la molécula de ácido nítrico contiene tres átomos de oxígeno unidos a un átomo de nitrógeno central, mientras que la molécula de ácido nitroso contiene dos átomos de oxígeno unidos a un átomo de nitrógeno central.
Referencia:
1. Ácido nitroso. (norte.d.). Con ciencias. Consultado el 13 de octubre de 2020, disponible aquí.
Imagen de cortesía:
1. "Ben Mills-Wikimedia a través de Commons Wikimedia
2. "ACSV de ácido nitroso" de Calvero - Trabajo propio (dominio público) a través de Commons Wikimedia


