Diferencia entre oxidación y reducción
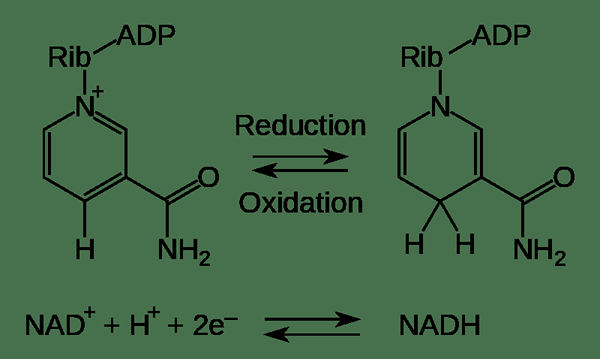
El diferencia clave entre la oxidación y la reducción es que La oxidación se refiere a la pérdida de electrones, mientras que la reducción se refiere a la ganancia de electrones.
Las reacciones químicas entre diferentes compuestos se denominan reacciones redox si los estados de oxidación de los reactivos son diferentes de los de los productos. Redox es corto para la reducción de oxidación, que es lo que ocurre en cualquier reacción química. Si bien las oxidaciones se refieren a la pérdida de electrones, las reducciones son donde se produce la recuperación de los electrones. Estas reacciones pueden ser simples o complejas, dependiendo del proceso y los átomos involucrados.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la oxidación?
3. ¿Qué es la reducción?
4. Comparación de lado a lado: oxidación frente a reducción en forma tabular
5. Resumen
¿Qué es la oxidación??
La oxidación puede describirse como un aumento en el número de oxidación. Por lo tanto, la oxidación se puede definir como la pérdida de electrones de un átomo, molécula o un ion. Esta pérdida de electrones hace que aumente el estado de oxidación de las especies químicas. Dado que una reacción de oxidación libera electrones, debe haber una especie que acepte electrones. Por lo tanto, la reacción de oxidación es una medias reacción de una reacción importante. La oxidación de una especie química se da como el cambio de su oxidación establece. El estado de oxidación es un número con un símbolo positivo (+) o negativo (-), lo que indica la pérdida o ganancia de electrones por un átomo particular, una molécula o un ion.

Figura 01: Un ejemplo de las dos medias reacciones: oxidación y reducción
En el pasado, el término oxidación recibió la definición "la adición de oxígeno a un compuesto."Esto fue porque el oxígeno era el único agente oxidante conocido en ese momento. Sin embargo, esta definición ya no es precisa ya que hay muchas más reacciones de oxidación que ocurren en ausencia de oxígeno. Por ejemplo, la reacción entre el magnesio (mg) y el ácido clorhídrico (HCl) no implica oxígeno, pero es una reacción redox que incluye la oxidación de Mg en Mg2+.
¿Qué es la reducción??
La reducción puede describirse como una disminución en el número de oxidación. Por lo tanto, podemos definir la reducción como la ganancia de electrones de un átomo, una molécula o un ion. Esta ganancia de electrones hace que el estado de oxidación de las especies químicas disminuya. Dado que una reacción de reducción obtiene electrones, debe haber una especie donadora de electrones. Por lo tanto, la reacción de reducción es una medias reacción de una reacción importante. La reducción de una especie química se da como el cambio de su oxidación establece.
En el pasado, el término reducción recibió la definición "la eliminación de oxígeno de un compuesto."Esto fue porque el oxígeno era el único agente oxidante conocido en ese momento. Sin embargo, esta definición ya no es precisa ya que hay muchas más reacciones de oxidación que ocurren en ausencia de oxígeno.
¿Cuál es la diferencia entre oxidación y reducción??
Reducción y oxidación son procesos químicos involucrados en cada reacción química. Estas son dos reacciones opuestas. La diferencia clave entre oxidación y reducción es que la oxidación se refiere a la pérdida de electrones, mientras que la reducción se refiere a la ganancia de electrones. Si bien la oxidación aumenta el valor del signo positivo (+), la reducción aumenta el valor del signo negativo (-).
Resumen -Oxidación vs Reducción
Reducción y oxidación son procesos químicos involucrados en cada reacción química. La diferencia clave entre oxidación y reducción es que la oxidación se refiere a la pérdida de electrones, mientras que la reducción se refiere a la ganancia de electrones.
Referencia:
1. Helmenstine, Anne Marie. “Definición y ejemplo de oxidación en química."Thinkco, febrero. 12, 2020, disponible aquí.
2. Helmenstine, Anne Marie. “Definición de reducción en química."Thinkco, febrero. 11, 2020, disponible aquí.
Imagen de cortesía:
1. "Reducción de oxidación NAD" por Fvasconcellos 19:44, 9 de diciembre de 2007 (UTC). W: Imagen: reducción de oxidación de NAD.PNG de Tim Vickers. - Versión vectorial de W: Imagen: reducción de oxidación NAD.PNG de Tim Vickers (dominio público) a través de Commons Wikimedia