Diferencia entre oxo y formyl
El diferencia clave entre oxo y formyl es que el El término OXO se refiere a un átomo de oxígeno unido a una molécula, mientras que el término formil se refiere a un grupo -cho unido a una molécula.
Oxo y formyl son grupos funcionales en compuestos orgánicos. Por lo tanto, estos son restos de moléculas orgánicas. Estos grupos funcionales generalmente están unidos a los átomos de carbono. Las propiedades químicas y físicas de los compuestos orgánicos están determinadas por estos grupos funcionales.
CONTENIDO
1. Descripción general y diferencia de claves
2. Que es oxo
3. Que es formyl
4. Comparación de lado a lado: oxo vs formyl en forma tabular
5. Resumen
Que es oxo?
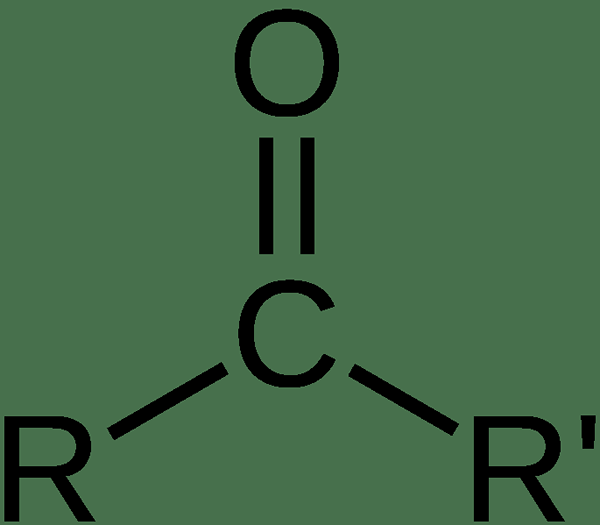
El término oxo se refiere a un grupo funcional que contiene un solo átomo de oxígeno. En general, los grupos OXO se pueden observar en compuestos de carbonilo donde un átomo de oxígeno se une a un átomo de carbono a través de un doble enlace. Este es un grupo funcional, y podemos abreviarlo como "= O".

Figura 1: La estructura de un compuesto carbonilo que tiene un grupo funcional OXO
Hay diferentes clases de compuestos oxo (compuestos de carbonilo) como aldehídos, cetonas, ácidos carboxílicos y amidios. En estos compuestos, el oxígeno es más electronegativo que el átomo de carbono al que está unido; Por lo tanto, el grupo OXO hace que estos compuestos muestren resonancia. La capacidad de formar estructuras de resonancia puede afectar la reactividad de la molécula. El enlace C = O en el grupo OXO es un enlace polar, y la alta electronegatividad del átomo de oxígeno hace que atraiga los electrones de enlace hacia sí mismo, lo que hace que el átomo de carbono sea ligeramente cargado positivamente. Por lo tanto, los átomos de carbono unidos al grupo oxo se convierten.
Que es formyl?
Formyl es un grupo funcional que tiene la fórmula química -cho. Este grupo funcional contiene un centro de carbonilo. Cuando se adjunta un grupo R a este grupo funcional, lo nombramos como un aldehído. El grupo R puede ser alifático o aromático; Por lo general, es un grupo alquilo. Por ejemplo, el compuesto más simple que contiene un grupo formil es el formaldehído. Es un compuesto de aldehído compuesto de grupo formilo unido a un átomo de hidrógeno. La fórmula química del formaldehído es HCOH.
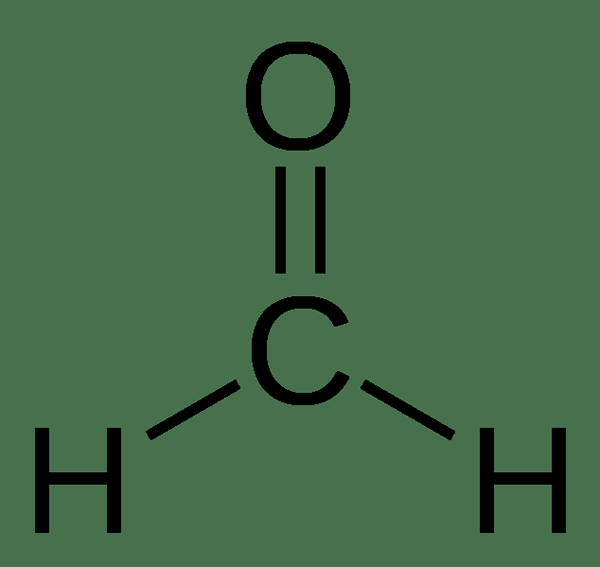
Figura 02: el formaldehído contiene un grupo formilo unido con un átomo de hidrógeno
Un grupo de formilo siempre ocurre en el término de una molécula. No puede ocurrir en el medio de una molécula (porque un extremo del grupo formilo contiene un átomo de hidrógeno que no puede formar otro enlace que no sea su enlace único con el átomo de carbono carbonilo).
Por lo general, el grupo de formilo es altamente reactivo. Por lo tanto, tiende a participar en muchas reacciones. mi.gramo. Reacciones de condensación. Tras la reducción del grupo formilo, forma un alcohol primario. Del mismo modo, tras la oxidación, se oxida fácilmente formar ácidos carboxílicos.
¿Cuál es la diferencia entre oxo y formyl??
La diferencia clave entre oxo y formilo es que el término oxo se refiere a un átomo de oxígeno unido a una molécula, mientras que el término formyl se refiere a un grupo -cho unido a una molécula. Además, un grupo OXO siempre ocurre en la parte media de la molécula, mientras que un grupo de formilo siempre ocurre en el término de la molécula.
La siguiente tabla resume la diferencia entre oxo y formyl.
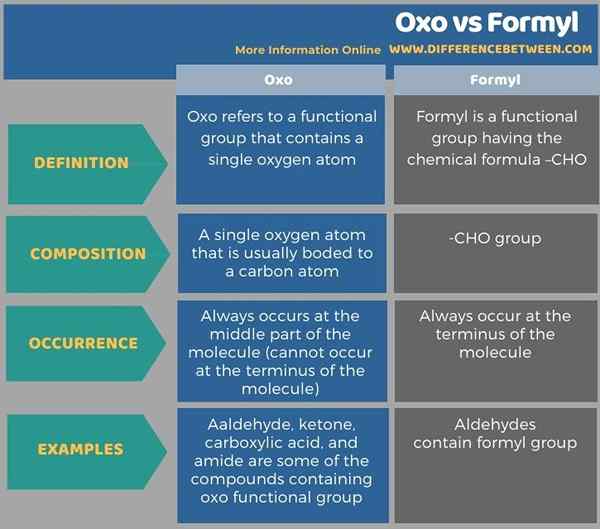
Resumen -Oxo vs Formyl
Oxo y formilo son grupos funcionales en moléculas orgánicas. La diferencia clave entre oxo y formilo es que el término oxo se refiere a un átomo de oxígeno unido a una molécula, mientras que el término formyl se refiere a un grupo -cho unido a una molécula.
Referencia:
1. "Foros químicos: nomenclatura orgánica (¿por qué tratar a un grupo como un teclado, no aldehído?) ". Foro químico, 2020, disponible aquí.
Imagen de cortesía:
1. "Ketone General" de Nothingserious - Trabajo propio (dominio público) a través de Commons Wikimedia
2. "Formaldehído -2d" por Wason - Trabajo propio (dominio público) a través de Commons Wikimedia


