Diferencia entre oxigenación y oxidación
El diferencia clave entre la oxigenación y la oxidación es que el La oxigenación esencialmente implica oxígeno molecular, mientras que la oxidación no implica necesariamente oxígeno.
Aunque ambos términos oxigenación y oxidación suenan similares, son dos términos distintos. Esto se debe a que el proceso de oxigenación requiere la presencia de oxígeno, pero el proceso de oxidación puede ocurrir en ausencia completa de oxígeno.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la oxigenación?
3. ¿Qué es la oxidación?
4. Comparación de lado a lado: oxigenación frente a oxidación en forma tabular
5. Resumen
¿Qué es la oxigenación??
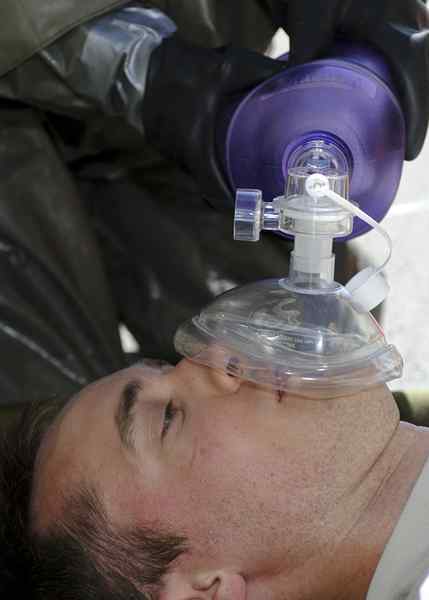
La oxigenación es la adición de oxígeno molecular a cualquier sistema. Por ejemplo, el proceso de tratar a un paciente con oxígeno también se refiere a la oxigenación. En química, utilizamos este término principalmente para indicar la adición de oxígeno molecular a una especie química como los metales de transición en la formación de compuestos de coordinación.

Figura 01: dar oxígeno a un paciente puede referirse a la oxigenación
En estos complejos de coordinación, el oxígeno molecular actúa como un ligando que se une con un metal de transición. La mayoría de las veces, estos complejos se forman reversiblemente. Eso significa; Podemos eliminar el oxígeno molecular del complejo si cambiamos las condiciones de reacción.
¿Qué es la oxidación??
La oxidación es el proceso de aumentar el número de oxidación de especies químicas. Sin embargo, hay tres definiciones distintas para este término; La adición de oxígeno, eliminación de hidrógeno o pérdida de electrones significa oxidación. Pero, todas estas definiciones tienen excepciones en diferentes ocasiones. Por lo tanto, usamos la definición anterior como definición general para todas las ocasiones.
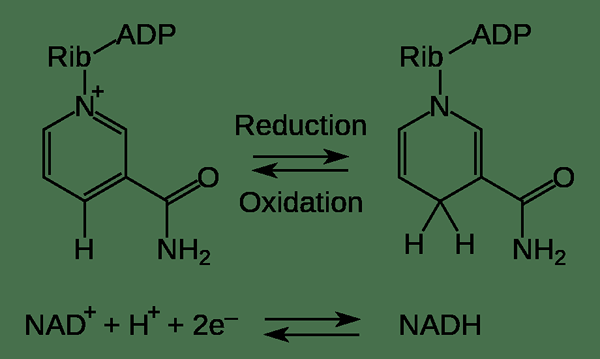
Figura 02: una reacción redox
La oxidación es un tipo de reacción redox. Una reacción redox esencialmente tiene dos reacciones paralelas; Reacciones de oxidación y reacciones de reducción. Estas reacciones siempre implican la transferencia de electrones entre dos especies químicas. Además, las especies químicas que sufre oxidación siempre liberarán electrones, mientras que las especies químicas que sufren reducción siempre obtendrán esos electrones. Por lo tanto, liberar electrones hace más protones que no tienen electrones para neutralizar su carga. Por lo tanto, la eliminación de electrones aumentará el número de oxidación de las especies químicas.
¿Cuál es la diferencia entre oxigenación y oxidación??
La oxigenación es la adición de oxígeno molecular a cualquier sistema, mientras que la oxidación es el proceso de aumentar el número de oxidación de una especie química. Por lo tanto, la diferencia clave entre la oxigenación y la oxidación es que la oxigenación esencialmente implica oxígeno molecular, mientras que la oxidación no involucra necesariamente oxígeno. Además, usamos el término oxigenación para referirnos a la adición de oxígeno molecular a una especie química como el metal de transición o el tratamiento de un paciente con oxígeno, mientras que el término oxidación se refiere al aumento del número de oxidación de una especie química.
La siguiente infografía tabula la diferencia entre la oxigenación y la oxidación como un lado para comparar lateralmente.

Resumen -Oxigenación vs Oxidación
Ambos términos oxigenación y oxidación pueden referirse a la adición de oxígeno, pero no siempre. Además, el término oxidación a veces se refiere a los procesos que ocurren en la ausencia completa de oxígeno. Por lo tanto, la diferencia clave entre la oxigenación y la oxidación es que la oxigenación esencialmente implica oxígeno molecular, mientras que la oxidación no involucra necesariamente oxígeno.
Referencia:
1. Nabili, Siamak N. "¿Qué es la policitemia vera?? Síntomas, esperanza de vida, tratamiento y causas."Medicinenet. Disponible aquí
2. "Redox."Wikipedia, Fundación Wikimedia, 6 de octubre. 2018. Disponible aquí
Imagen de cortesía:
1."2000916137" por Airman St Class Anania TekuriorElimed (CC0) a través de la Base de la Fuerza Aérea Ellsworth
2."Reducción de la oxidación de NAD" por Fvasconcellos (dominio público) a través de Commons Wikimedia


