Diferencia entre el modelo de partículas de la materia y la teoría molecular cinética
Diferencia clave - Modelo de partículas de la materia vs teoría molecular cinética
El modelo de partículas de la materia es un modelo que se utiliza para explicar la disposición de átomos, moléculas o iones que están presentes en cualquier material. La teoría molecular cinética es una teoría utilizada para explicar las propiedades físicas de un gas. La diferencia clave entre el modelo de partícula de la materia y la teoría molecular cinética es que El modelo de partículas de la materia describe las propiedades de las fases sólidas, líquidas y de gas de la materia, mientras que la teoría molecular cinética describe las propiedades de los gases.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el modelo de la materia?
3. ¿Qué es la teoría molecular cinética?
4. Comparación lado a lado - Modelo de partículas de la materia vs teoría molecular cinética en forma tabular
5. Resumen
¿Qué es el modelo de la materia??
El modelo de partículas de la materia es un modelo que explica la disposición de partículas (átomos, moléculas o iones) en una cierta fase de la materia. Hay tres fases principales que cualquier materia puede existir en: fase sólida, fase líquida y fase gaseosa. El modelo de partículas expresa los siguientes conceptos:
- Toda la materia está construida a partir de pequeñas partículas.
- Estas pequeñas partículas siempre están en movimiento.
- Hay espacios vacíos entre estas partículas.
- Cuando la materia se calienta, aumenta el movimiento de las partículas.
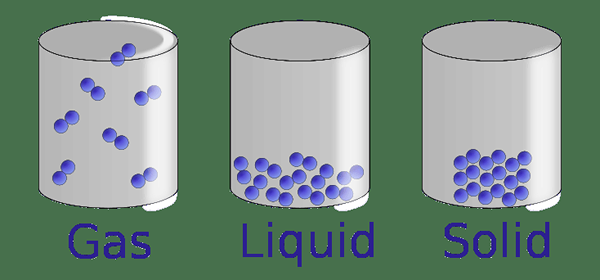
Figura 1: Las tres fases de la materia
Fase sólida
La fase sólida es la fase de la materia en la que las partículas (átomos, moléculas o iones de los que está hecho el sólido) se mantiene estrechamente. Por lo tanto, las partículas están muy estrechamente llenas. Hay espacios vacíos muy pequeños entre las partículas. Hay interacciones intermoleculares muy fuertes entre partículas. Estas características le dan a los sólidos una forma particular. Dado que las partículas están bien llenas, las partículas muestran un movimiento casi insignificante (las vibraciones se pueden observar la mayoría de las veces; por lo tanto, las partículas permanecen en ciertas posiciones). A medida que el sólido obtiene una forma fija, también tiene un volumen fijo. La densidad de un sólido es muy alta en comparación con los líquidos y los gases.
Fase líquida
La fase líquida es una fase de materia en la que las partículas se empacan de cerca, pero no es un empaque apretado como en los sólidos. Los espacios vacíos entre las partículas son grandes en comparación con los sólidos, pero son pequeños en comparación con los gases. Las partículas pueden moverse libremente. El líquido no tiene forma definida; obtiene la forma del recipiente en el que está presente el líquido. La densidad de un líquido es menor que la de un sólido y más alto que la de un gas. Sin embargo, un líquido tiene un volumen fijo ya que las partículas se empacan de cerca.
Fase gaseosa
La fase gaseosa es una fase de materia en la que las partículas están en movimiento continuo en direcciones aleatorias. Por lo tanto, hay grandes espacios entre las partículas de gas. Estas partículas llenan un recipiente cerrado en el que está presente el gas. Entonces el gas obtiene el volumen del contenedor. La densidad de un gas es muy menor en comparación con la de los sólidos y los líquidos.
¿Qué es la teoría molecular cinética??
La teoría molecular cinética es una teoría que describe las propiedades físicas de los gases a su nivel molecular. Los conceptos de la teoría molecular cinética son los siguientes.
- Los gases contienen partículas que están en constante movimiento aleatorio.
- Estas partículas chocan entre sí constantemente. Las colisiones son completamente elásticas.
- El volumen de una molécula de gas es insignificante en comparación con el volumen del contenedor en el que está presente el gas. Pero estas partículas tienen una masa considerable.
- No hay fuerzas intermoleculares entre las moléculas de gas.
- La energía cinética promedio del gas es proporcional a la temperatura absoluta del gas.

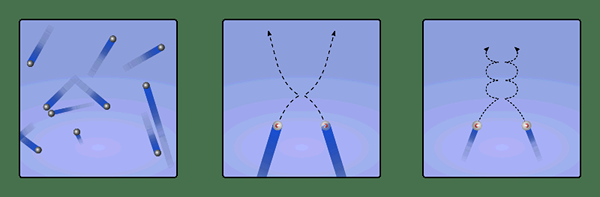
Figura 2: colisiones puras entre partículas de gas
La relación entre la energía cinética y la velocidad de las moléculas de gas se puede dar como se muestra a continuación.
Ke = ½.MV2
Donde KE es la energía cinética, M es la masa de una partícula de gas y V es la velocidad promedio de las moléculas de gas. Pero medir estos parámetros es difícil; Por lo tanto, la ecuación se modifica a continuación.
Ke = 3/2.kBT
Donde ke es la energía cinética, kB es la constante del Boltzmann (1.381 × 10-23 metro2 kg s-2 K-1), y t es la temperatura absoluta del gas (en las unidades Kelvin). Esta ecuación indica que la energía cinética del gas es directamente proporcional a la temperatura absoluta del gas.
¿Cuál es la diferencia entre el modelo de partícula de la materia y la teoría molecular cinética??
Modelo de partículas de la materia vs teoría molecular cinética | |
| El modelo de partículas de la materia es un modelo que explica la disposición de partículas (átomos, moléculas o iones) en una cierta fase de la materia. | La teoría molecular cinética es una teoría que indica las propiedades físicas de los gases a su nivel molecular. |
| Componentes | |
| El modelo de partículas de la materia describe las propiedades de las fases sólidas, líquidas y de gas de la materia. | La teoría molecular cinética describe las propiedades de los gases. |
| Contenido | |
| El modelo de partículas de la materia explica la disposición de partículas en un sólido, líquido o gas. | La teoría molecular cinética explica la relación entre la energía cinética y otras propiedades de un gas. |
Resumen - Modelo de partículas de la materia vs teoría molecular cinética
El modelo de partículas y la teoría molecular cinética explican diferentes propiedades físicas de la materia. El modelo de partículas es el modelo que explica la disposición de partículas (átomos, moléculas o iones) en una cierta fase de la materia. La teoría molecular cinética describe la relación entre la energía cinética y otras propiedades de un gas. La diferencia clave entre el modelo de partículas de la materia y la teoría molecular cinética es que el modelo de partícula de la materia describe las propiedades de las fases sólidas, líquidas y de gas de la materia, mientras que la teoría molecular cinética describe las propiedades de los gases.
Referencia:
1. "Modelo de partículas de sólidos, líquidos y gases."Chemstuff, 8 de junio de 2012, disponible aquí.
2. Panadero, rhys. "¿Cuál es el modelo de partículas: una guía para sólidos, líquidos y gases?."Owlcation, Owlcation, 14 de junio de 2016, disponible aquí.
3. Bibliotecas. "Teoría molecular cinética de los gases."Bibliotecas de química, Librettexts, 2 de octubre. 2016, disponible aquí.
Imagen de cortesía:
1. "Estados de la materia" de Yelod - Wikimedia Commons * Yelod - Wikipedia (en) * ילוד - ighibilidad.0) a través de Commons Wikimedia
2. "Teoría cinética de los gases (2)" de Olivier Cleynen y usuario: Sharayanan - Trabajo propio basado en el archivo: Teoría cinética de los gases.SVG (CC BY-SA 3.0) a través de Commons Wikimedia


