Diferencia entre rutenio y rodio

El diferencia clave Entre Ruthenium y Rhodium es que Ruthenium contiene siete electrones en la cubierta de electrones D más externa, mientras que Rhodium contiene ocho electrones en la cubierta de electrones D más externa.
Tanto el rutenio como el rodio son elementos químicos en el período 5 de la tabla periódica. Pero tienen diferentes números atómicos; Por lo tanto, estos elementos químicos tienen diferentes propiedades químicas y físicas como se describe a continuación.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es Ruthenium?
3. ¿Qué es Rhodium?
4. Comparación de lado a lado - Ruthenium vs Rhodium en forma tabular
5. Resumen
¿Qué es Ruthenium??
El rutenio es un elemento químico que tiene el número atómico 44. El símbolo químico para el rutenio es Ru, y es un metal de transición raro. Podemos encontrar rutenio en el grupo 8 y el período 5 de la tabla periódica de elementos. Por lo tanto, es un elemento de bloque D, y la configuración electrónica de este elemento es [KR] 4D75s1. A temperatura ambiente y presión, este elemento químico ocurre en estado sólido y tiene un punto de fusión muy alto (alrededor de 2300 centígrados) y un punto de ebullición muy alto (aproximadamente 4400 Celsius). Los estados de oxidación más comunes y estables de Rutenio son +3 y +4. Puede formar un óxido ligeramente ácido.

El rutenio ocurre naturalmente en su estado primordial. Esta sustancia sólida aparece como un metal blanco polivalente duro. La estructura cristalina del rutenio sólido es una estructura hexagonal llena. Además, el rutenio contiene electrones no apareados, lo que lo hace paramagnético. Además de eso, el rutenio tiene solo un electrón en la cubierta de electrones más externa, mientras que todos los demás elementos del grupo 8 contienen dos electrones. Esta es una característica única de Ruthenium.
¿Qué es Rhodium??
Rhodium es un elemento químico que tiene el número atómico 45. El símbolo químico de este elemento es rh. Es un metal de transición raro que se encuentra en el grupo 9 y el período 5 de la tabla periódica de elementos. Rhodium aparece como un metal blanco plateado. Es un metal duro que es resistente a la corrosión y químicamente inerte. Por lo tanto, podemos clasificarlo como un metal noble. Solo hay un isótopo de Rhodium natural (RH-103). Podemos encontrar este metal naturalmente como un metal libre debido a su naturaleza inerte. A veces ocurre como una aleación con metales similares, y rara vez ocurre como un compuesto químico en minerales. mi.gramo. bowieite. El estado de oxidación más común del rodio es +3. Puede formar óxidos anfotéricos.
Al considerar la ocurrencia natural de Rhodium, es primordial, y en su estado sólido, Rhodium tiene una estructura de cristal cúbico centrada en la cara. Este metal es paramagnético porque tiene electrones no apareados. El punto de fusión y el punto de ebullición son muy altos (alrededor de 1900 y 3600 Celsius, respectivamente).
Rhodium es un metal duro que tiene una alta reflectancia. Normalmente, no forma óxidos incluso al calentar. Puede absorber oxígeno solo en el punto de alquiler del metal. Tras la solidificación, este oxígeno absorbido se libera por completo. La mayoría de los ácidos no pueden atacar el metal de rodio. mi.gramo. insoluble en ácido nítrico.
¿Cuál es la diferencia entre Ruthenium y Rhodium??
El rutenio es un elemento químico que tiene el número atómico 44, mientras que Rodium es un elemento químico que tiene el número atómico 45. Ambos son elementos de período 5. La diferencia clave entre el rutenio y el rodio es que el rutenio contiene siete electrones en la cubierta de electrones D más externa, mientras que Rhodium contiene ocho electrones en la cubierta de electrones D más externa.
A continuación, la tabla presenta una comparación detallada de ambos elementos para discernir la diferencia entre Ruthenium y Rhodium.
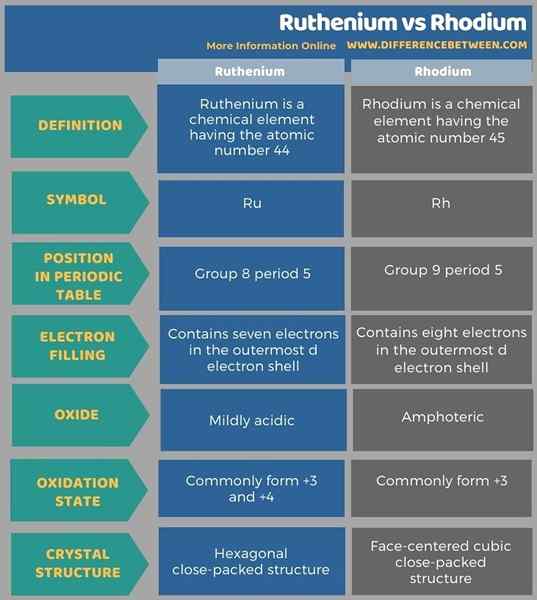
Resumen -Ruthenium vs Rhodium
Tanto el rutenio como el rodio están en el mismo período en la tabla periódica de elementos, pero están en diferentes grupos porque tienen diferentes números atómicos. La diferencia clave entre el rutenio y el rodio es que el rutenio contiene siete electrones en la cubierta de electrones D más externa, mientras que Rhodium contiene ocho electrones en la cubierta de electrones D más externa.
Referencia:
1. Pedersen, traci. "Hechos sobre Rhodium." Vida, Compra, 13 mar. 2018, disponible aquí.
Imagen de cortesía:
1. "Ruthenium A Half Bar" de Alchemist-HP (charla) (www.PSE-Mendelejew.de) - trabajo propio, fal) a través de Commons Wikimedia
2. "Rhodium Powder presionado derretido" por Alchemist-HP (charla) www.PSE-Mendelejew.Trabajo dederivativo: Purpy Pupple (Talk) - Trabajo propio (CC By -SA 3.0 de) a través de Commons Wikimedia


