Diferencia entre Rydberg y la fórmula de Balmer

El diferencia clave Entre Rydberg y la fórmula de Balmer es que La fórmula de Rydberg da la longitud de onda en términos del número atómico del átomo, mientras que la fórmula de Balmer da la longitud de onda en términos de dos enteros: M y N.
Las fórmulas de Rydberg y Balmer son importantes para determinar la longitud de onda de los fotones emitidos por las excitaciones de electrones. Estas fórmulas se desarrollaron para el espectro atómico de hidrógeno. Por lo tanto, estas fórmulas se usan con el modelo BOHR.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la fórmula de Rydberg?
3. ¿Qué es la fórmula de Balmer?
4. Comparación de lado a lado: fórmula de Rydberg vs Balmer en forma tabular
6. Resumen
¿Qué es la fórmula de Rydberg??
La fórmula de Rydberg es una expresión matemática que predice la longitud de onda de la luz emitida por excitaciones de electrones en átomos. En otras palabras, esta fórmula encuentra la longitud de onda de los fotones que se emiten cuando un electrón regresa al estado fundamental desde su estado excitado. La fórmula de Rydberg fue desarrollada por el físico Johannes Rydberg, quien intentó obtener una relación matemática entre los números de onda de las líneas espectrales adyacentes del espectro de la línea de hidrógeno. La fórmula es la siguiente:
1/λ = RZ2(1/n12-1/n22)
Donde, λ longitud de onda del fotón emitido, r es la constante de Rydberg, z es el número atómico del átomo que se está considerando, y n1 y N2 son enteros. Siempre n1 < n2. Más tarde, se descubrió que estos dos enteros están relacionados con el número cuántico principal, que está involucrado en la emisión de fotones.
Sin embargo, esta fórmula es aplicable con el átomo de hidrógeno y algunos otros átomos pequeños. Pero, cuando se trata de átomos grandes y complicados, la fórmula de Rydberg ofrece resultados incorrectos debido al efecto de detección que surge debido a la presencia de múltiples electrones (los electrones internos se detectan de electrones externos).
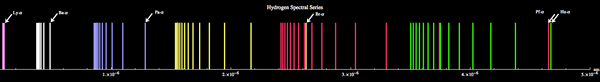
Figura 01: espectro de hidrógeno
Además, asignando diferentes valores a n1 y N2 enteros, podemos obtener las longitudes de onda correspondientes a las diferentes series de línea como la serie Lyman, la serie Balmer, la serie Paschen, etc. Al resolver problemas con respecto a la fórmula de Rydberg, tenemos que usar los valores de los números cuánticos principales para n1 y N2. Desde n1 < n2, norte1 es el número cuántico del nivel de energía al que se mueve el electrón mientras que n2 es el número cuántico del nivel de energía desde el cual se libera el electrón excitado.
¿Qué es la fórmula de Balmer??
La fórmula de Balmer es una expresión matemática que se puede usar para determinar las longitudes de onda de las cuatro líneas visibles del espectro de la línea de hidrógeno. Esta fórmula fue desarrollada por el físico Johann Jacob Balmer en 1885. Desarrolló esta fórmula usando dos enteros: M y N. La fórmula es la siguiente:
λ = constante (m2/metro2-norte2)
Sin embargo, esta fórmula es completamente empírica. Eso significa; No es una fórmula derivada de una teoría particular. Además, la fórmula de Balmer era cierta, pero en el momento de su desarrollo, había menos datos experimentales para demostrar que es una fórmula verdadera. Más tarde, otro físico llamado Rydberg modificó esta fórmula, afirmando que la fórmula de Balmer tiene una amplia aplicabilidad, introduciendo el concepto de número de onda en lugar de longitud de onda.
¿Cuál es la diferencia entre Rydberg y la fórmula de Balmer??
La fórmula de Rydberg y Balmer son fórmulas importantes en la química. En realidad, la fórmula de Rydberg es un derivado de la fórmula de Balmer. Además, la diferencia clave entre Rydberg y la fórmula de Balmer es que la fórmula de Rydberg da la longitud de onda en términos del número atómico del átomo, pero la fórmula de Balmer da la longitud de onda en términos de dos enteros: M y N.
A continuación, la infografía resume la diferencia entre Rydberg y la fórmula de Balmer.

Resumen -Fórmula de Rydberg vs Balmer
La fórmula de Rydberg y Balmer son fórmulas importantes en la química. La fórmula de Rydberg es un derivado de la fórmula Balmer. La diferencia clave entre la fórmula de Rydberg y Balmer es que la fórmula de Rydberg da la longitud de onda en términos del número atómico del átomo, pero la fórmula de Balmer da la longitud de onda en términos de dos enteros, M y N.
Referencia:
1. Helmenstine, Todd. "¿Cuál es la fórmula de Rydberg y cómo funciona??"Thinkco, agosto. 28, 2019, disponible aquí.
Imagen de cortesía:
1. "HydroGenspectrum" de Caitlin Jo Ramsey - Trabajo propio (CC BY -SA 3.0) a través de Commons Wikimedia


