Diferencia entre el puente de sal y el enlace de hidrógeno
El diferencia clave entre el puente de sal y el enlace de hidrógeno es que El puente de sal es un tubo con un electrolito que conecta dos medias células en una célula electroquímica, mientras que el enlace de hidrógeno es una fuerza de atracción entre dos átomos de dos moléculas diferentes.
El puente de sal es muy útil para mantener la conectividad entre dos medias células de una célula electroquímica. Es visible a simple vista. Sin embargo, el enlace de hidrógeno es un enlace químico que mantiene la conectividad entre dos moléculas, que puede formar enlaces de hidrógeno.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es un puente de sal?
3. ¿Qué es un enlace de hidrógeno?
4. Comparación de lado a lado - Puente de sal frente a enlace de hidrógeno en forma tabular
5. Resumen
¿Qué es un puente de sal??
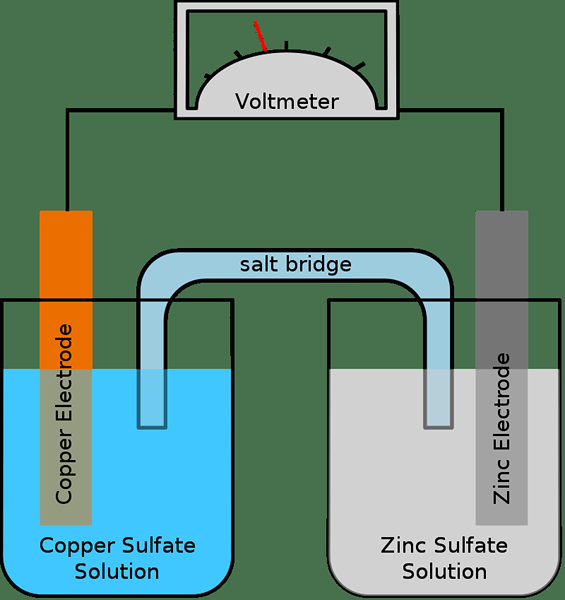
El puente de sal es un tubo que contiene un electrolito (típicamente en forma de gel), proporcionando contacto eléctrico entre dos soluciones. Por lo tanto, este tubo es importante para conectar las reacciones de oxidación y reducción de la célula galvánica. El propósito de usar un puente de sal es facilitar la reacción electroquímica que alcanza el equilibrio rápidamente. Si no hay puente de sal, entonces una media célula acumulará cargas positivas, y la otra mitad celular acumula cargas negativas. En consecuencia, la generación de electricidad se detiene.
Hay dos tipos principales de puentes de sal: puente de tubo de vidrio y puente de papel de filtro. El puente de sal del tubo de vidrio es un tubo U hecho de vidrio y contiene el electrolito. En el puente de sal de papel de filtro, hay un papel de filtro empapado con el electrolito.
¿Qué es el enlace de hidrógeno??
Un enlace de hidrógeno es un tipo de fuerza de atracción entre dos átomos de dos moléculas diferentes. Es una fuerza de atracción débil. Pero, en comparación con otros tipos de fuerzas intramoleculares, como las interacciones polar-polares, las interacciones no polar-nopolar como las fuerzas de Vander Waal, el enlace de hidrógeno es más fuerte.
Por lo general, los enlaces de hidrógeno se forman entre las moléculas covalentes polares. Estas moléculas contienen enlaces covalentes polar, que se forman como resultado de la diferencia en los valores de electronegatividad de los átomos que están en el enlace covalente. Si esta diferencia es alta, el átomo altamente electronegativo tiende a atraer los electrones de unión hacia sí mismo. Por lo tanto, esto crea un momento dipolo en el que este átomo altamente electronegativo obtiene una carga negativa parcial, mientras que el otro átomo obtiene una carga positiva parcial. Entonces el enlace se convierte en un enlace covalente polar. Cuando esta molécula se encuentra con otra molécula que tiene un momento dipolar como este, las cargas negativas y positivas tienden a atraerse entre sí. Y, esta fuerza de atracción se llama unión de hidrógeno.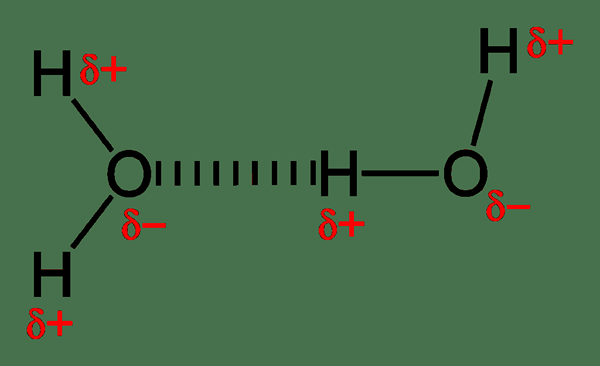
Además, los enlaces de hidrógeno se forman entre átomos altamente electronegativos y átomos menos electronegativos. Además, existen cuando tenemos O, N y F en una molécula y positivo H en la otra molécula. Es porque F, N y O son los átomos más electronegativos que son capaces de formar enlaces de hidrógeno.
¿Cuál es la diferencia entre el puente de sal y el enlace de hidrógeno??
El puente de sal y el enlace de hidrógeno son importantes para principios de conectividad entre los objetos deseados. Por ejemplo, un puente de sal conecta dos medias células de una célula electroquímica, mientras que el enlace de hidrógeno conecta dos moléculas. La diferencia clave entre el puente de sal y el enlace de hidrógeno es que un puente de sal es un tubo con un electrolito que conecta dos medias células en una célula electroquímica. Pero, un enlace de hidrógeno es una fuerza de atracción entre dos átomos de dos moléculas diferentes.
Debajo de la infografía resume la diferencia entre el puente de sal y el enlace de hidrógeno.

Resumen -Puente de sal vs enlace de hidrógeno
El puente de sal y el enlace de hidrógeno son importantes para mantener la conectividad entre los objetos deseados. Por ejemplo, el puente de sal conecta dos medias células de una célula electroquímica, mientras que el enlace de hidrógeno conecta dos moléculas. La diferencia clave entre el puente de sal y el enlace de hidrógeno es que un puente de sal es un tubo que consiste en un electrolito, y conecta dos medias células en una célula electroquímica, mientras que el enlace de hidrógeno es una fuerza de atracción entre dos átomos de dos moléculas diferentes.
Referencia:
1. Helmenstine, Anne Marie. "Definición de puente de sal."Thinkco, Jul. 3, 2019, disponible aquí.
Imagen de cortesía:
1. "Galvanic Cell" de Gringer - Archivo: Galvanische Zelle.PNG, de Tinux (CC BY-SA 3.0) a través de Commons Wikimedia
2. "Bonding-en-Water-2D" (dominio público) a través de Commons Wikimedia


