Diferencia entre fosfato de sodio monobásico y dibásico

Sodio fosfato monobásico vs dibásico | Fosfato de sodio DIBASIC VS Fosfato de sodio monobásico | Monosodium fosfato vs fosfato disódico | Monosodium vs Fosfato de disodio
Un átomo de fósforo está unido con cuatro oxígenos, para formar un anión poliatómico -3. Debido a los enlaces individuales y el doble enlace, entre P y O, el fósforo tiene un estado de oxidación de +5 aquí en. Tiene una geometría tetraédrica. La siguiente es la estructura del anión fosfato.
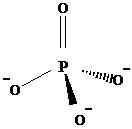
correos43-
El anión fosfato puede combinarse con diferentes cationes, para formar numerosos compuestos iónicos. El fosfato de sodio es una sal como esa donde tres iones de sodio están unidos electrostadísticamente con un anión fosfato. Trisodium fosfato es un cristal de color blanco, que se disuelve altamente en agua. Cuando soluble en agua, produce una solución alcalina. Sodio fosfato monobásico y fosfato de sodio Los dibásicos son otros dos compuestos de sodio y fosfato. Para un ácido, definimos el término monobásico como "un ácido, que posee solo un protón que puede donarse a una base durante una reacción de base ácida."Del mismo modo, el dibásico para un ácido significa tener dos protones, que se pueden donar a una base. Pero cuando considere estos dos términos con respecto a una sal, el significado es completamente diferente. Una sal monobásica se refiere a una sal, que tiene solo un átomo de un metal univalente. Y sal de dibásico significa tener dos iones metálicos univalentes. En este caso, el ion metal univalente es el catión de sodio. Dado que estas son sales, se disuelven fácilmente en agua y producen soluciones alcalinas. Estos compuestos están disponibles comercialmente en formas hidratadas y anhidros. El fosfato de sodio monobásico y dibásico juntos son muy importantes en los sistemas biológicos como un tampón. Además, médicamente, estos dos se usan como laxante salina, para tratar el estreñimiento.
Fosfato de sodio monobásico
Fosfato de sodio monobásico o fosfato monosódico tiene la fórmula molecular de NAH2correos4. La masa molar del compuesto es de 120 g de moles-1. El anión en esta molécula no es el anión fosfato trivalente, sino el H2correos4- anión. Este anión ha derivado del ion fosfato donde dos hidrógenos están unidos con dos oxígenos negativos. Alternativamente, por otro lado, se ha derivado de la eliminación de un protón del ácido fosfórico (H3correos4). El anión fosfato y H2correos4- Los aniones están en equilibrio, en medios acuosos. El monobásico de fosfato de sodio está disponible como cristales incoloros o polvo blanco. Se disuelve fácilmente en agua, pero no se disuelve en solventes orgánicos como el alcohol. El pka de esto es entre 6.8-7.20. Este compuesto se puede hacer cuando el ácido fosfórico reacciona con una sal de sodio como el haluro de sodio.
Dibásico de fosfato de sodio
Este compuesto también se conoce como fosfato disódico y tiene la fórmula molecular de NA2HPO4. La masa molar del compuesto es de 142 g moles-1. Cuando dos cationes de sodio reemplazan los átomos de hidrógeno en el ácido fosfórico, se obtiene el dibásico por fosfato de sodio. Entonces, en el laboratorio podemos hacer este compuesto reaccionando dos equivalentes de hidróxido de sodio con un equivalente de ácido fosfórico. El compuesto es un sólido cristalino blanco, y se disuelve fácilmente en agua. El pH de esta solución acuosa es un valor básico, que está entre 8 y 11. Esta sal se usa para fines de cocción y como laxante.
| Cuál es la diferencia entre Sodio fosfato monobásico y sodio fosfato dibásico? • El monobásico de fosfato de sodio tiene la fórmula química de NAH2correos4, y el dibásico de fosfato de sodio tiene la fórmula química de NA2HPO4. • El peso molecular del fosfato de sodio dibásico es mayor que el del monobásico de fosfato de sodio. • Cuando el dibásico de fosfato de sodio se disuelve en el agua, la basicidad es mayor en el medio que cuando el monobásico de fosfato de sodio se disuelve en agua. |


