Diferencia entre cloruro estánico y estannoso
El diferencia clave Entre el cloruro estánico y estannoso es que El cloruro estánico tiene el estado de oxidación +4 de estaño, mientras que el cloruro estannoso tiene el estado de oxidación +2 de estaño.
Los nombres estánicos y estannosos se refieren a la lata del elemento químico que tiene dos estados de oxidación diferentes. El cloruro estánico es cloruro de estaño (IV), mientras que el cloruro estannoso es cloruro de estaño (ii).
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el cloruro estánico?
3. ¿Qué es el cloruro estannoso?
4. Comparación lado a lado: cloruro estannico vs estannoso en forma tabular
5. Resumen
¿Qué es el cloruro estánico??
El cloruro estánico es cloruro de estaño (IV). También se conoce como tetracloruro de estaño, que es un compuesto inorgánico que tiene la fórmula química SNCL4. Este compuesto es un líquido higroscópico incoloro que sufre humo al contacto con el aire. Tiene un olor acre. Este compuesto es importante como precursor para la producción de otros compuestos que contienen estaño. Fue descubierto por el científico Andreas Libavius.

Figura 01: Compuesto de cloruro estánico
Podemos preparar cloruro estánico a través de la reacción entre el gas de cloro y el metal de estaño a 115 grados Celsius. Además, este compuesto se solidifica a aproximadamente menos 33 grados Celsius. Esta solidificación proporciona cristales monoclínicos, y esta estructura es isoestructural con SNBR4. Hay varias hidratos conocidos de cloruro estánico, como la forma de pentahidrato. La estructura hidratada tiene moléculas de agua adicionales que unen las moléculas de cloruro estanánico a través de enlaces de hidrógeno.
Al considerar los usos del cloruro estánico, la aplicación principal de este compuesto es como un precursor de los compuestos de organotina que son útiles como catalizadores y estabilizadores de polímeros. Podemos usar este compuesto en el proceso sol-gel para preparar el recubrimiento SNO2, los nanocristales de SNO2, etc.
¿Qué es el cloruro estannoso??
El cloruro estannoso es cloruro de estaño (ii). Aparece como un sólido cristalino blanco que tiene la fórmula química SNCL2. La forma principal de este compuesto es la forma de dihidrato, pero las soluciones acuosas de cloruro estannoso tienden a sufrir hidrólisis cuando la solución está caliente. Además, SNCL2 se usa ampliamente como agente reductor, y también es importante en los baños electrolíticos para el plato de estaño. Este sólido blanco es inodoro, lo cual es una diferencia con el cloruro estánico.
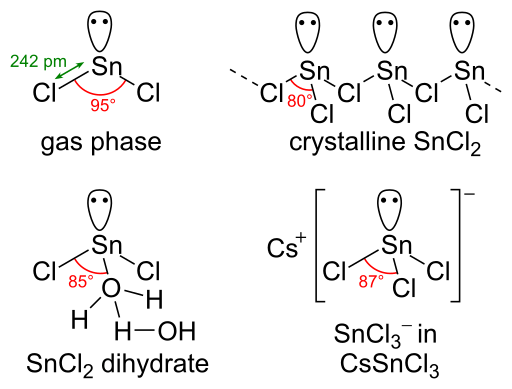
La molécula SNCL2 tiene un par solitario de electrones; Por lo tanto, esta molécula tiene una geometría doblada en su fase gaseosa. Cuando se considera el estado sólido del cloruro estannoso, forma una estructura de cadena que está vinculada a través de puentes de cloruro.

Figura 02: Estructuras de cloruro estannoso en diferentes fases
Podemos preparar cloruro estannoso a través de la acción del gas de cloruro de halógeno seco sobre metal de estaño. Podemos producir la forma de dihidrato mediante una reacción similar usando el ácido HCl. A partir de entonces, el agua presente en la solución debe eliminarse cuidadosamente mediante evaporación para obtener los cristales de cloruro de estannos dihidratos. Esta forma de dihidrato puede sufrir deshidratación a la forma anhidra usando anhídrido acético.
Hay muchos usos diferentes del cloruro estannoso que incluyen el revestimiento de acero de estaño, como un mordiente en teñido teñido porque proporciona colores brillantes con algunos tintes, como agente protegiente contra la erosión del esmalte en la pasta de dientes, como catalizador en la producción de material de plástico PLA , como agente reductor, etc.
¿Cuál es la diferencia entre el cloruro estánico y estannoso??
Los nombres estánicos y estannosos se refieren a la lata del elemento químico que tiene dos estados de oxidación diferentes. La diferencia clave entre el cloruro estánico y estannoso es que el cloruro estánico tiene el estado de oxidación +4 de estaño, mientras que el cloruro estannoso tiene el estado de oxidación +2 de estaño. Al considerar la preparación de estos dos compuestos, se puede hacer cloruro estánico a través de la reacción entre el gas de cloro y el metal de estaño a 115 grados Celsius. El cloruro estannoso se puede hacer mediante la acción del gas de cloruro de halógeno seco sobre metal de estaño.
A continuación, las infografías enumeras más diferencias entre el cloruro estannico y estannoso.
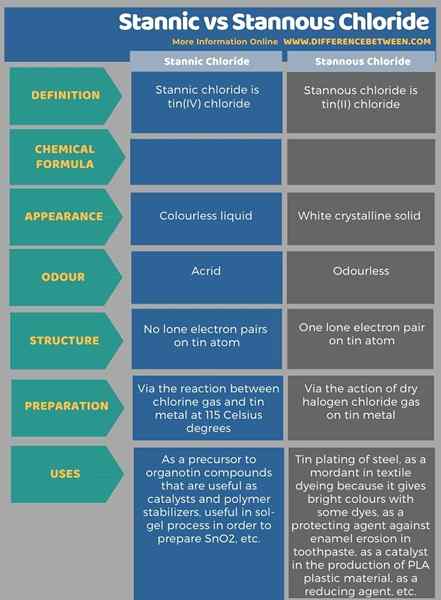
Resumen -cloruro de estannic vs estannoso
Los nombres estánicos y estannosos se refieren a la lata del elemento químico que tiene dos estados de oxidación diferentes. La diferencia clave entre el cloruro estánico y estannoso es que el cloruro estánico tiene el estado de oxidación +4 de estaño, mientras que el cloruro estannoso tiene el estado de oxidación +2 de estaño.
Referencia:
1. "Cloruro estannoso."Cloruro estannoso - una descripción general | Temas de ciencias, disponibles aquí.
Imagen de cortesía:
1. "Pentahidrato de cloruro de estaño (IV)" (dominio público) a través de Commons Wikimedia
2. "Estructura SNCL2" de HBF878 - Trabajo propio (CC0) a través de Commons Wikimedia


