Diferencia entre el modelo de Atom Thomson y Rutherford

Diferencia clave: Thomson vs Rutherford Modelo de Atom
La diferencia clave entre Thomson y Rutherford de Atom es que El modelo Thomson de Atom no contiene ningún detalle sobre el núcleo mientras El modelo de Atom de Rutherford explica sobre el núcleo de un átomo. J.J. Thomson fue el primero en descubrir la partícula subatómica llamada electrón en 1904. El modelo que propuso fue nombrado "modelo de budín de ciruela del átomo". Pero en 1911, a Ernest Rutherford se le ocurrió un nuevo modelo para el átomo después de su descubrimiento del núcleo atómico en 1909.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el modelo Thomson de Atom?
3. ¿Qué es el modelo Rutherford de Atom?
4. Comparación de lado a lado - Thomson vs Rutherford Modelo de Atom en forma tabular
5. Resumen
¿Qué es el modelo Thomson de Atom??
El modelo Thomson de Atom se llama Modelo de budín de ciruela porque afirma que el átomo parece un pudín de ciruela. Los únicos detalles conocidos sobre el átomo en ese momento fueron,
- Los átomos están compuestos de electrones
- Los electrones son partículas cargadas negativamente
- Los átomos se cargan neutralmente
Dado que los electrones se cargan negativamente, Thomson sugirió que debería haber una carga positiva para neutralizar la carga eléctrica del átomo. El modelo Thomson de Atom explica que los electrones están incrustados en un material sólido cargado positivamente que es de forma esférica. Esta estructura parece un pudín con ciruelas incrustadas y fue nombrada modelo de budín de ciruela de átomo. Esto demostró la suposición de que establece un átomo se carga neutralmente ya que este modelo establece que las cargas negativas de electrones se neutralizan por la carga positiva de la esfera sólida. Aunque este modelo demostró que los átomos están cargados neutralmente, fue rechazado después del descubrimiento del núcleo.

Figura 01: Modelo Thomson de Atom
¿Qué es el modelo Rutherford de Atom??
Según el modelo Rutherford de Atom, el llamado modelo de budín de ciruela de Thomson era incorrecto. El modelo de Atom de Rutherford también se llama modelo nuclear porque proporciona detalles sobre el núcleo de un átomo.
El famoso experimento llamado "Experimento de lámina de oro Rutherford" condujo al descubrimiento del núcleo. En este experimento, las partículas alfa fueron bombardeadas a través de una lámina de oro; Se esperaba que pasen directamente a través de la lámina de oro. Pero en lugar de una penetración recta, las partículas alfa se convirtieron en diferentes direcciones.
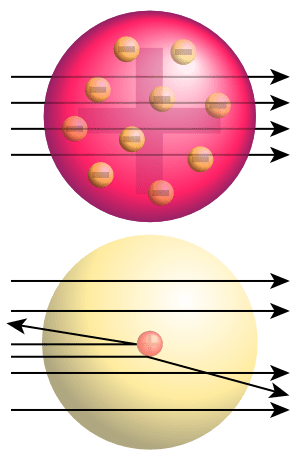
Figura 02: Experimento de aluminio de Rutherford Gold Arriba: Resultados esperados (penetración recta) Abajo: Resultados observados (desviación de algunas partículas)
Esto indicó que hay algo sólido con una carga positiva en esa lámina de oro que causa una colisión con partículas alfa. Rutherford nombró este núcleo positivo como el núcleo. Luego sugirió el modelo nuclear para el átomo; Estaba compuesto por un núcleo cargado positivamente y electrones cargados negativamente que rodean el núcleo. También sugirió que los electrones están en orbitales alrededor del núcleo en ciertas distancias. Este modelo también se llama modelo planetario Porque Rutherford sugirió que los electrones se encuentran alrededor del núcleo similar a los planetas ubicados alrededor del sol.
Según este modelo,
- El átomo está compuesto por un centro cargado positivamente que se llama núcleo. Este centro contenía la masa del átomo.
- Los electrones se encuentran fuera del núcleo en orbitales en una distancia considerable.
- El número de electrones es igual al número de cargas positivas (más tarde llamadas protones) en el núcleo.
- El volumen del núcleo es insignificante en comparación con el volumen del átomo. Por lo tanto, la mayor parte del espacio en el átomo está vacío.
Sin embargo, este modelo de átomo de Rutherford también fue rechazado porque no podía explicar por qué los electrones y las cargas positivas en el núcleo no se sienten atraídas entre sí.

Figura 03: Modelo Rutherford de Atom
¿Cuál es la diferencia entre el modelo de Atom Thomson y Rutherford??
Thomson vs Rutherford Modelo de Atom | |
| El modelo de átomo Thomson es el modelo que establece que los electrones están integrados en un material sólido cargado positivamente que es esférico de forma. | El modelo de Atom de Rutherford es el modelo que explica que hay un núcleo en el centro del átomo y los electrones se encuentran alrededor del núcleo. |
| Núcleo | |
| El modelo Thomson de Atom no da ningún detalle sobre el núcleo. | El modelo Rutherford de Atom proporciona detalles sobre el núcleo de un átomo y su ubicación dentro del átomo. |
| Ubicación de electrones | |
| Según el modelo Thomson de Atom, los electrones están integrados en un material sólido. | Rutherford Model dice que los electrones se encuentran alrededor del núcleo. |
| Orbitales | |
| El modelo Thomson de Atom no da detalles sobre los orbitales. | El modelo Rutherford de Atom explica sobre los orbitales y que los electrones se encuentran en estos orbitales. |
| Masa | |
| El modelo Thomson de Atom explica que la masa de un átomo es la masa de sólido cargado positivamente donde los electrones están integrados. | Según el modelo Rutherford de átomo, la masa de un átomo se concentra en el núcleo del átomo. |
Resumen -Thomson vs Rutherford Modelos de Atom
Los modelos Thomson y Rutherford de Atom fueron los primeros modelos para explicar la estructura de un átomo. Después del descubrimiento del electrón por J.J. Thomson, propuso un modelo para explicar la estructura del átomo. Más tarde, Rutherford descubrió el núcleo e introdujo un nuevo modelo usando electrones y núcleo. La principal diferencia entre el modelo de Atom Thomson y Rutherford es que el modelo Thomson de Atom no contiene ningún detalle sobre el núcleo, mientras que el modelo de Atom Rutherford explica sobre el núcleo de Atom.
Descargar la versión PDF de Thomson vs Rutherford Models of Atom
Puede descargar la versión PDF de este artículo y usarla para fines fuera de línea según las notas de la cita. Descargue la versión PDF aquí Diferencia entre Thomson y Rutherford Modelo de Atom.
Referencia:
1."Modelo de Rutherford del átomo: definición y diagrama." Estudiar.comunicarse. norte.d. Web. Disponible aquí. 06 de junio de 2017.
2. Brescia, Frank. Fundamentos de la química: una introducción moderna (1966). Elsevier, 2012. Imprimir.
3. Goldsby, Kenneth. Química. 12ª ed. Nueva York: McGraw-Hill, 2015. Imprimir.
Imagen de cortesía:
1. "Atom de pudín de ciruela" (dominio público) a través de Commons Wikimedia
2. "Rutherford Atom" por propio trabajo (CrearJoder XD XD) (CC BY-SA 3.0) a través de Commons Wikimedia
3. "Rutherford Gold Foil Resultados" por el usuario: trabajo propio de FastFission (dominio público) a través de Commons Wikimedia


